
【题目】已知![]() 碳在
碳在![]() 氧气中燃烧至反应物耗尽,共放出
氧气中燃烧至反应物耗尽,共放出![]() 的热量.已知单质碳的燃烧热为
的热量.已知单质碳的燃烧热为![]() ,则
,则![]() 与
与![]() 反应生成
反应生成![]() 的反应热
的反应热![]() 为( )
为( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【答案】C
【解析】
碳在氧气中燃烧,氧气不足发生反应2C+O2![]() 2CO,氧气足量发生反应C+O2
2CO,氧气足量发生反应C+O2![]() CO2;
CO2;
3.6g碳的物质的量为![]() =0.3mol,6.4g的氧气的物质的量为
=0.3mol,6.4g的氧气的物质的量为![]() =0.2mol,n(C):n(O2)=3:2,介于2:1与1:1之间,所以上述反应都发生;
=0.2mol,n(C):n(O2)=3:2,介于2:1与1:1之间,所以上述反应都发生;
令生成的CO为Xmol,CO2为Ymol,
根据碳元素守恒有X+Y=0.3,根据氧元素守恒有X+2Y=0.2×2,联立方程,解得X=0.2,Y=0.1;
单质碳的燃烧热为YkJ/mol,所以生成0.1mol二氧化碳放出的热量为0.1mol×YkJ/mol=0.1YkJ,
所以生成0.2molCO放出的热量为XkJ-0.1YkJ;
由于碳燃烧为放热反应,所以反应热△H的符号为“-”,故1molC与O2反应生成CO的反应热△H=-![]() =-(5X-0.5Y)kJ/mol,故答案为C。
=-(5X-0.5Y)kJ/mol,故答案为C。


科目:高中化学 来源: 题型:
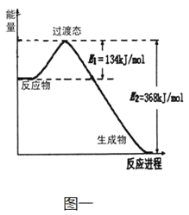
【题目】20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
(1)图一是NO2和CO反应生成CO2和NO 过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________。在反应体系中加入适宜的催化剂(正催化剂),E1和E2的变化是:E1_______,E2_____(填“增大”、“减小”或“不变”),对反应热有无影响?________,原因是_______。
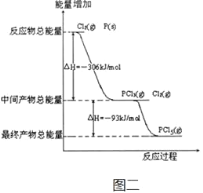
(2)图二是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程与能量关系图(图中的△H表示生成1mol产物的数据)。根据图二回答下列问题:
①PCl5(g)分解成PCl3(g)和Cl2(g)的热化学方程式_______。
②P(s)和Cl2(g)分两步反应生成1molPCl5(g)的△H1与P(s)和Cl2(g)一步反应生成1molPCl5(g)的△H2关系是:△H2______△H1(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属镁,其流程如下图所示:
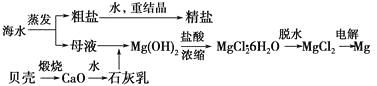
(1)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。__________________________
(2)实验室将粗盐制成精盐的过程中,溶解、过滤、蒸发三个步骤的操作都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
①溶解:________________。
②过滤:__________________________。
③蒸发:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知煤的近代结构模型如图所示。
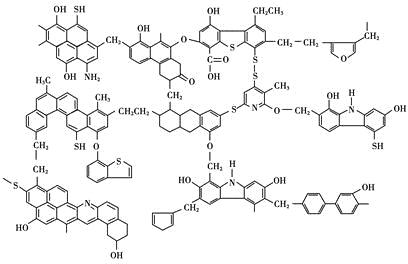
回答下列问题:
(1)从煤的结构模型来看,煤是工业上获得____________的重要来源。
(2)我国大约70%的煤是直接用于燃烧的。从煤的结构模型来看,在提供热量的同时产生大量的____________、____________等气体物质,造成严重的大气污染。
(3)“型煤”技术不仅可以减少87%的废气排放量,烟尘排放量也可减少80%,致癌物苯并[α]芘的排放量也减少,同时节煤20%~30%。“型煤”技术的原理是利用固硫剂在燃烧过程中生成稳定的硫酸盐。某“型煤”生产厂利用石灰石作固硫剂,试用化学方程式表示其固硫过程________________、________________。
(4)为了解决煤燃烧所造成的污染问题和提高煤的利用价值,煤资源的综合利用方法还有____________、____________、____________等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于我国煤储藏量相对比石油和天然气丰富,能源消费以煤为主。将原煤作为燃料燃烧,既严重污染环境,效率又不高,因而国家大力提倡煤的综合利用。实施“煤变油”,其原理之一是先将煤与水蒸气制得水煤气(一氧化碳和氢气),再催化合成甲醇或烃类等液态能源。
(1)用一氧化碳和氢气合成甲醇的化学方程式是______________________________________。
(2)用一氧化碳和氢气合成烃(CnHm)的化学方程式是__________________________。
(3)气化和液化的优点是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 稀醋酸与稀氢氧化钠溶液发生中和反应的热化学方程式为CH3COOH (aq) + NaOH (aq) = CH3COONa(aq) + H2O(l) ΔH=![]() 57.3kJ/mol
57.3kJ/mol
B. 在101kPa时1mol物质燃烧时的反应热叫做该物质的燃烧热
C. 未来氢气作为新能源的其中一个优点是充分燃烧的产物不污染环境
D. 升高温度或加入催化剂,可以改变化学反应的反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温恒容的密闭容器中,放入一定量的甲醇,发生反应:![]() .以下可以作为该反应达到平衡状态的判断依据为( )
.以下可以作为该反应达到平衡状态的判断依据为( )
A.容器内气体密度保持不变B.气体的平均相对分子质量保持不变
C.![]() 的体积分数保持不变D.
的体积分数保持不变D.![]() 与
与![]() 的物质的量之比保持
的物质的量之比保持![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素X、Y、Z和 W在元素周期表中的位置如下图所示, 其最外层电子数之和为21。下列说法中正确的是
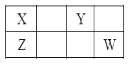
A. 单质W可由海水作原料获得
B. Y 的非金属性比 X的强,所以Y的氢化物一定比 X的更稳定
C. 工业上常利用单质 X与含 Z氧化物的矿石在高温下反应制备高纯 Z
D. X的氢化物可以与 W的单质发生反应,但是不能与 W 的氢化物发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com