
����Ŀ������ͼ��ʾװ���н��а��Ĵ�����ʵ�飺������ƿ�ڵ�Ũ��ˮ�в���ͨ������������ȵIJ�˿����ƿ�в��ӽ�Һ�档��Ӧ�����У��ɹ۲쵽ƿ���к���ɫ�����������˿ʼ�ձ��ֺ��ȡ������й�˵���������(����)

A. ��Ӧ����Һ�к���NO3-
B. ��Ӧ����Һ��c(H��)����
C. ʵ��������л��Ϸ�Ӧ����
D. ʵ�������NH3H2O�ĵ��볣�������ܷ����仯

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ��H2R�������ε���Һ�У�H2R��HR-��R2-�ֱ�����������ռ�����ʵ�������(��)����ҺpH�仯��ϵ����ͼ��ʾ������������������
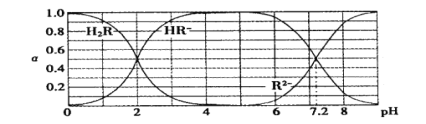
A��H2R�Ƕ�Ԫ���ᣬ��Ka1=1��10-2
B������Һǡ�ó�����ʱ��c( Na + )=2c ( R2- ) + c( HR- )
C��NaHR����Һ��ˮ��������ڵ�������
D����Na2R��NaHR��0.1 mol�Ļ����Һ��pH=7.2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ����ʻ�Ӧ�þ���ȷ����
A����������Ϊ������������������������оƬ
B��ͭ�Ľ��������Ա�������ں��������װ����ͭ���Լ����丯ʴ
C��Zn���л�ԭ�Ժ͵����ԣ�������п�̸ɵ�صĸ�������
D��Ũ���������ˮ�ԣ������ڸ���NH3��SO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2015���Ͼ������Ǻϳ���������κ͵��ʵĻ���ԭ�ϣ��ش��������⣺
��1������ˮ��Һ�������ԣ���ԭ��Ϊ �������ӷ���ʽ��ʾ����0��1 mol��L-1�İ�ˮ�м���������NH4Cl���壬��Һ��PH ������ߡ����͡�������������������������Һ�е�NH4+��Ũ�� �������С������
��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
��3����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ��������1molN2�� ����H= kJ��mol-1��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����мס��ҡ�����ƿ�������������ˮ��Ũ�Ⱦ�Ϊ0.1 mol��L��1������ڼ�ƿ�м���������NaHCO3����(n mol)������ƿ�м���������NaHSO3����(n mol)����ƿ���䡣Ƭ�̺ס��ҡ�����ƿ��Һ��HClO�����ʵ���Ũ�ȵĴ�С��ϵ��(��Һ����仯���Բ���)�� ��
A. �ף���>�� B. ��>��>�� C. ��>�ף��� D. ��>��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ�ClNO�����л��ϳ��е���Ҫ�Լ�����ҵ�Ͽ���NO��Cl2�ϳɣ��ش��������⣺
(1)һ�������£����������������ڴ����еĺ������������ʱ�������������ȣ��漰�Ȼ�ѧ����ʽ��ƽ�ⳣ�����±���
��� | �Ȼ�ѧ����ʽ | ƽ�ⳣ�� |
�� | 2NO2(g)+NaCl(s) | K1 |
�� | 4NO2(g)+2NaCl(s) | K2 |
�� | 2NO(g)+ Cl2(g) | K3 |
��H3=_________���æ�H1����H2��ʾ����K3=__________����K1��K2 ��ʾ��
(2)300��ʱ����һ�ܱ������з�����Ӧ��2ClNO(g) ![]() 2NO(g)+ Cl2(g)��������Ӧ���ʱ���ʽΪv��=k��cn(ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
2NO(g)+ Cl2(g)��������Ӧ���ʱ���ʽΪv��=k��cn(ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
��� | c(ClNO)/mol��L-1 | v��/mol��L-1��s-1 |
�� | 0.30 | 3.60��10-9 |
�� | 0.60 | 1.44��10-8 |
�� | 0.90 | 3.24��10-8 |
/p>
��n=________��k=___________���ﵽƽ�������Сѹǿ�����������ƽ����������_______�����������С�����䡱����
(3)25��ʱ�������Ϊ2L�Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��0.08mol NO��0.04mol Cl2������Ӧ��2NO(g)+Cl2(g) ![]() 2ClNO(g) ��H
2ClNO(g) ��H
������Ӧ��ʼ��ƽ��ʱ�¶���ͬ����÷�Ӧ������ѹǿ��p����ʱ�䣨t���ı仯��ͼ������a��ʾ����H________0���>������<����ȷ��������������������ͬ�����ı�ijһ����ʱ�������ѹǿ��p����ʱ�䣨t���ı仯��ͼ������b��ʾ����ı��������___________��
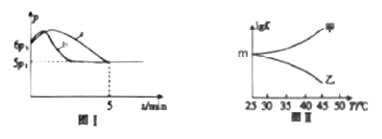
��ͼ���Ǽס���ͬѧ���������Ӧƽ�ⳣ���Ķ���ֵ��lgK�����¶ȵı仯��ϵ��������ȷ��������____����ס����ҡ�����mֵΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ұ��ṩ�����ݣ��ж��ڵ�Ũ�ȵ�NaClO��NaHCO3�����Һ�У�������Ũ�ȵĹ�ϵ��ȷ���ǣ�
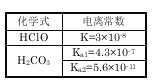
A��c(HCO3��)��c(ClO-)��c(OH��)
B��c(ClO-)��c(HCO3-)��c(H��)
C��c(ClO-)+c(HClO)=c(HCO3-)+c(H2CO3)
D��c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������γɵľ����У�����������ͬ���ǣ� ��
A.������SiC
B.C60��Mg
C.NaCl��HCl
D.SO2��SiO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com