
【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂,工业上可用NO与Cl2合成,回答下列问题:
(1)一定条件下,氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及热化学方程式和平衡常数如下表:
序号 | 热化学方程式 | 平衡常数 |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+ Cl2(g) | K3 |
则ΔH3=_________(用ΔH1、ΔH2表示);K3=__________(用K1、K2 表示)
(2)300℃时,在一密闭容器中发生反应:2ClNO(g) ![]() 2NO(g)+ Cl2(g),其正反应速率表达式为v正=k·cn(ClNO)。测得速率和浓度的关系如下表:
2NO(g)+ Cl2(g),其正反应速率表达式为v正=k·cn(ClNO)。测得速率和浓度的关系如下表:
序号 | c(ClNO)/mol·L-1 | v正/mol·L-1·s-1 |
① | 0.30 | 3.60×10-9 |
② | 0.60 | 1.44×10-8 |
③ | 0.90 | 3.24×10-8 |
/p>
则n=________;k=___________;达到平衡后,若减小压强,则混合气体的平均分子量将_______(填“增大”、“减小”或“不变”)。
(3)25℃时,向体积为2L且带气压计的恒容密闭容器中通入0.08mol NO和0.04mol Cl2发生反应:2NO(g)+Cl2(g) ![]() 2ClNO(g) ΔH
2ClNO(g) ΔH
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图Ⅰ曲线a所示,则ΔH________0(填“>”、“<”或“不确定”);若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图Ⅰ曲线b所示,则改变的条件是___________。
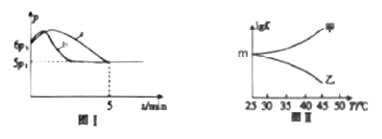
②图Ⅱ是甲、乙同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是____(填“甲”或“乙”);m值为_______________。
【答案】 2△H1-△H2 K12/K2 2 4.0×10-8 减小 < 加入催化剂 乙 2
【解析】(1)本题考查热化学反应方程式的计算以及化学平衡常数,2×①-②得出△H3=2△H1-△H2;K1=c(ClNO)/c2(NO2),K2=c(Cl2)×c2(NO)/c4(NO2),K3=c2(ClNO)//[c2(NO)×c(Cl2)]因此K3=K12/K2;(2)本题考查化学反应速率的计算,以及影响化学平衡的因素,把①②数值代入v正的表达式,3.6×10-9=k×0.3n,1.44×10-8=k×0.6n,两式相比,求出n=2,从①②③中任选一组数值代入v正的表达式,解得k=4×10-8;减小压强,平衡向正反应方向移动,组分都是气体,则气体质量不变,气体的物质的量增大,根据M=m/n,则平均摩尔质量减小;(3)本题考查影响化学平衡的因素,①由图1分析可知,随着反应的进行压强先增大后减小,5min达到平衡,推出开始因反应是放热,随反应进行,温度升高,压强增大,达到一定程度,因反应物浓度减小,随反应正向进行,压强反而减小,到压强不再改变时,说明反应达到平衡,即△H<0;化学反应速率加快,但平衡不移动,因此改变的条件是加入催化剂;②本题考查化学平衡常数的计算温度升高,平衡向逆反应方向移动,K减小,lgK减小,故曲线乙正确;
2NO(g)+Cl2(g) ![]() 2ClNO(g)
2ClNO(g)
起始浓度:0.04 0.02 0
变化: 2x x 2x
平衡: 0.04-x 0.02-x 2x 因为等温等容,因此压强之比等于物质的量之比,即0.06/(0.06-x)=6/5,解得x=0.01,根据平衡常数的定义,K=c2(ClNO)/[c2(NO)×c(Cl2)]=0.022/(0.01×0.022)=100,即lgK=2。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
【题目】FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为( )
A. 1︰7 B. 1︰6 C. 2︰11 D. 16︰25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是( )
A.Na、Mg、Al的还原性依次减弱
B.I、Br、Cl的非金属性性依次增强
C.C,N,O 的原子半径依次增大
D.P,S,Cl的最高正化合价依次升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是( )

A. 反应后溶液中含有NO3-
B. 反应后溶液中c(H+)增大
C. 实验过程中有化合反应发生
D. 实验过程中NH3H2O的电离常数不可能发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016江苏卷】下列图示与对应的叙述不相符合的是( )
A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,下列说法正确的是

A. 0-t1时,原电池的负极是铜片
B. 0-t1时,正极的电极反应式是2H++2e-=H2↑
C. t1时刻,电流方向发生变化的原因是Al 在浓硝酸中发生钝化,氧化膜阻止了Al进一步反应
D. tl时刻后,电子从铝经过导线流向铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 2.0gH218O与D2O的混合物中所含中子数为NA
B. 50mL18mol·L-1浓硫酸与足量铜供热,转移电子数为0.9NA
C. 0.1molCl2通入含0.1molFeBr2溶液中,被氧化的溴离子数为0.2NA
D. 标准状况下,2.24LNO和足量O2反应生成物中含有NO2分子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com