
| A、2Na+2H2O═2NaOH+H2↑ |
| B、2F2+2H2O═4HF+O2↑ |
| C、SO2+H2O═H2SO3 |
| D、Cl2+H2O═HCl+HClO |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、3种溶液pH的大小顺序是 ③>②>① |
| B、若分别滴加25mL和上述溶液等浓度的盐酸后,pH最大的是① |
| C、若将3种溶液稀释相同倍数,pH变化最大的是② |
| D、若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体的分散质粒子直径在1 nm~100nm之间 |
| B、胶体粒子有吸附性 |
| C、胶体粒子不能穿过半透膜,能通过滤纸空隙 |
| D、胶体粒子能够产生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝片与稀盐酸反应 |
| B、灼热的碳与CO2反应 |
| C、Ba(OH)2?8H2O与NH4Cl固体反应 |
| D、甲烷在氧气中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol苯分子中含有碳碳双键的数目为3NA |
| B、2.3g甲苯和丙三醇(C3H8O3)的混合物中,含氢原子数目为0.2NA |
| C、1mol-OH中电子数目为10NA |
| D、标准状况下,2.24 L溴乙烷中含共价键数目为0.7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.02×1023就是阿伏加德罗常数 |
| B、0.012 kg 12C含有的碳原子数就是阿伏加德罗常数的值 |
| C、含有阿伏加德罗常数个粒子的物质的量是1 mol |
| D、1 mol NH3所含原子数约是2.408×1024 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④⑤ | B、③④ |
| C、②④⑥ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NaH中氢离子结构示意图为: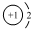 | ||||
B、NH4I的电子式: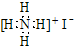 | ||||
C、质子数是82,中子数是122的铅原子:
| ||||
D、CO2的比例模型: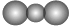 |
查看答案和解析>>
科目:高中化学 来源: 题型:
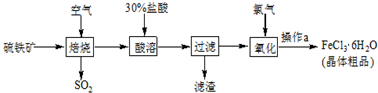
| 压强/KPa 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com