
【题目】为探究实验室制乙烯及乙烯和溴水的加成反应。甲同学设计了如图所示的实验装置,并进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的。
乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左 右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在170℃超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:

(1)写出甲同学实验中两个反应的化学方程式:_____________、___________________________。
(2)乙同学观察到的黑色物质是_____________,刺激性气体是_____________。乙同学认为刺激性气体的存在就不能认为溴水褪色是乙烯的加成反应造成的。原因是(用化学方程表示):________。
(3)丙同学根据甲乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO存在,他设计了如下过程(该过程可把实验中产生的有机产物除净):发现最后气体经点燃是蓝色火焰,确认有一氧化碳。

①设计装置a的作用是____________________
②浓溴水的作用是_______________________,稀溴水的作用是____________________。
【答案】CH3CH2OH ![]() CH2=CH2↑ + H2O CH2=CH2 + Br2
CH2=CH2↑ + H2O CH2=CH2 + Br2 ![]() Br-CH2CH2-Br C SO2 Br2 + SO2 + 2H2O = 2HBr + H2SO4 安全装置,防倒吸 吸收乙烯、二氧化硫气体 检验乙烯、二氧化硫气体是否除净
Br-CH2CH2-Br C SO2 Br2 + SO2 + 2H2O = 2HBr + H2SO4 安全装置,防倒吸 吸收乙烯、二氧化硫气体 检验乙烯、二氧化硫气体是否除净
【解析】
(1)实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃;溴水中的溴与乙烯发生加成反应;
(2)浓硫酸具有强氧化性,能氧化乙醇;二氧化硫和溴发生氧化还原反应;
(3)①造成倒吸,是由于装置内的大气压与外面的大气压有一定的差值;
②浓溴水能和乙烯、二氧化硫反应。
(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应方程式为:CH3CH2OH![]() CH2=CH2↑+H2O;溴水中的溴与乙烯发生加成反应,反应方程式:CH2=CH2+Br2→CH2BrCH2Br,
CH2=CH2↑+H2O;溴水中的溴与乙烯发生加成反应,反应方程式:CH2=CH2+Br2→CH2BrCH2Br,
故答案为:CH3CH2OH![]() CH2=CH2↑+H2O;CH2=CH2+Br2→CH2BrCH2Br。
CH2=CH2↑+H2O;CH2=CH2+Br2→CH2BrCH2Br。
(2)乙同学仔细观察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,浓硫酸具有强氧化性,能氧化乙醇,把乙醇氧化成碳,同时自身被还原成二氧化硫;二氧化硫和溴发生氧化还原反应生成氢溴酸和硫酸:SO2+Br2+2H2O=H2SO4+2HBr,故答案为:C;SO2;SO2+Br2+2H2O=H2SO4 +2HBr。
(3)①乙烯易溶于溴水中,装置内的大气压与外面的大气压有一定的差值,设计装置a可防止浓溴水倒吸到制乙烯的反应容器中,故答案为:安全装置,防倒吸。
②溴水与二氧化硫发生氧化还原反应,溴被二氧化硫中+4价的硫还原成-1价的溴,+4价的硫被溴氧化成+6价的硫,溴水褪色;乙烯和溴水中的溴发生加成反应,溴水褪色,可检验乙烯的存在,二氧化硫和溴发生氧化还原反应生成氢溴酸和硫酸,可检验二氧化硫的存在,故答案为:吸收乙烯、二氧化硫气体;检验乙烯、二氧化硫是否除尽。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是
A. 17g H2O2中含有非极性键的数目为NA
B. 常温常压下,17g甲基(-14CH3)所含的中子数为9NA
C. 在含CO32-总数为NA的Na2CO3溶液中,Na+总数为2NA
D. 13. 8g NO2与足量水反应,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.Na2S2O3溶液与稀H2SO4反应:S2O32-+6H+=2S↓+3H2O
B.在海带灰的浸出液中滴加H2O2得到I2:2I+H2O2+2H+=I2+O2↑+2H2O
C.向 NH4Al(SO4)2溶液中加入Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
D.Fe与稀硝酸反应,当n(Fe)∶n(HNO3)=1∶2时:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲溶液加入(或通入)物质乙(乙物质为气体或溶液),生成沉淀的质量与消耗乙的质量关系曲线符合图的是

A.向Na[Al(OH)4]溶液中通入二氧化碳
B.向Na[Al(OH)4]溶液中滴加盐酸
C.向澄清石灰水中通入二氧化碳
D.向Al2(SO4)3溶液中滴加NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)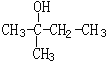 的系统命名:______________________它的H-NMR谱中有________个峰,峰的面积比为___________________
的系统命名:______________________它的H-NMR谱中有________个峰,峰的面积比为___________________
(2)写出 2,3-二甲基-4-乙基已烷结构简式_________________CH3CH2CH2CHO 的键线式___________________________________________________________
(3)写出CH3CH2OH催化氧化的化学方程式:__________________CH3CH2Br制取乙醇的化学方程式:______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如图,下列有关说法正确的是

A.该流程中,原料A可以是盐酸,也可以是氢氧化钠溶液
B.步骤2 中要发生的反应有:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=[Al(OH)4] -、H++OH-=H2O
C.滤液3中的主要离子有碳酸根、钠离子、氯离子
D.工业上冶炼铝用氧化铝不用氯化铝的原因是,氧化铝是电解质,氯化铝是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质:①Ar ②Na2O2 ③AlCl3 ④HClO ⑤N2 ⑥MgF2 ⑦NH4Cl
(1)只存在共价键的是___,不存在化学键的是_____,离子化合物有_______
(2)由离子键和极性键构成的物质是__________
(3)N2的电子式为_____ HClO的电子式为________NH4Cl的电子式为___________
(4)用电子式表示MgF2的形成过程___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol·L-1的氢氧化钠溶液,生成的沉淀跟加入的氢氧化钠溶液的体积关系如图(横坐标体积单位是mL,纵坐标质量单位是g)。
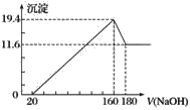
(1)合金中镁的质量是__________。
(2)所用盐酸的物质的量浓度是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含苯酚的工业废水的处理流程如图所示。
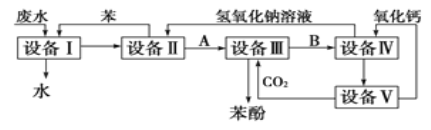
(1)流程图设备Ⅰ中进行的是________操作(填写操作名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是________(填化学式,下同)。由设备Ⅲ进入设备Ⅳ的物质B是________。
(3)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和________。通过________(填操作名称)操作,可以使产物相互分离。
(4)图中,能循环使用的物质是________、________、NaOH和CaO(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com