
��ͭ��CuFeS2����������������ͭ����ͭ���չ������������ķ�Ӧ�Ƚϸ��ӣ�������Ҫ��Ӧ֮һ�Ļ�ѧ����ʽΪ2CuFeS2��O2
 ��2FeS��SO2������ƽ���������й��ڸ÷�Ӧ��˵��������ǣ���������
��2FeS��SO2������ƽ���������й��ڸ÷�Ӧ��˵��������ǣ���������
| A�������е�����ӦΪCuS |
| B���÷�Ӧ�IJ��ֲ�����������Ṥҵ |
| C����Ӧ��SO2���������������ǻ�ԭ���� |
| D����Ӧ������1 mol SO2���ɣ���һ����4 mol���ӷ���ת�� |
 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����б仯�У���Ҫ������ʵ�����������ʵ�ֵ���
| A��HCl��H2 | B��CO2��CO | C��Fe2O3��Fe | D��Br-��Br 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������β������װ���г��������·�Ӧ��4CO+2NO2=4CO2+N2�����жԸ÷�Ӧ��˵������ȷ����
| A���÷�Ӧ�����û���Ӧ |
| B���÷�Ӧ����������CO����ԭ����NO2 |
| C���÷�Ӧ����14 g N2ʱ��ת��8 mol e- |
| D���÷�Ӧ�ܼ�������β���Ի�������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ʵ�ϣ�������������һ������������Na2O2��Ӧ���ҷ�Ӧ���й��ɣ���Na2O2��SO2=Na2SO4,2Na2O2��2SO3=2Na2SO4��O2���ݴ�����Ϊ���з�Ӧ����ʽ�в���ȷ����(����)
| A��Na2O2��N2O3=NaNO2��NaNO3 |
| B��Na2O2��2NO2=2NaNO2��O2 |
| C��Na2O2��N2O4=2NaNO3 |
| D��2Na2O2��2Mn2O7=4NaMnO4��O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ���� ����������
A�����ݷ�ӦCu��H2SO4 CuSO4��H2�����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ CuSO4��H2�����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ |
| B���ڷ�ӦCaH2��2H2O=Ca��OH��2��2H2���У�ˮ�������� |
| C����Ӧ3NO2��H2O=2HNO3��NO���������ͻ�ԭ�������ʵ���֮����3��1 |
| D����Cl2��������ǿ��I2�������ԣ������û���ӦI2��2NaClO3=2NaIO3��Cl2���ܷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����Fe2+��I-��Br-����Һ��ͨ��������������Һ�и������ӵ����ʵ����仯��ͼ��ʾ���й�˵������ȷ���ǣ� ��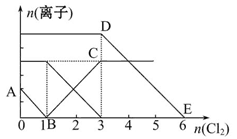
| A���߶�BC����Fe3+���ʵ����ı仯��� |
| B��ԭ�����Һ��c��FeBr2��="6" mol/L |
| C����ͨ��Cl2 2 molʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D��ԭ��Һ��n��Fe2+����n��I-����n��Br-��=2��1��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������(Ti)������Խ������Ϊ��������֮��ġ���������������ҵ���Խ��ʯΪԭ����ȡTi�ķ�ӦΪ
(1)aTiO2��bCl2��cC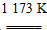 aTiCl4��cCO
aTiCl4��cCO
(2)TiCl4��2Mg Ti��2MgCl2
Ti��2MgCl2
���ڷ�Ӧ(1)��(2)�ķ�������ȷ����
��TiCl4�ڷ�Ӧ(1)���ǻ�ԭ����ڷ�Ӧ(2)����������
��C��Mg�ڷ�Ӧ�о�Ϊ��ԭ����������ԭ��Ӧ����ÿ����19.2 g Ti����Ӧ(1)��(2)�й�ת��4.8 mol e������a��1��b��c��2
A���٢ڢܡ������� B���ڢۢ� C���ۢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ȡm gþ���Ͻ���һ��Ũ�ȵ�ϡ������ǡ����ȫ�ܽ�(����Ļ�ԭ����ֻ��NO)����Ӧ��Ļ����Һ�еμ�b mol��L��1 NaOH��Һ�����μӵ�V mLʱ���õ���������ǡ��Ϊ���ֵn g���������йظ�ʵ���˵������ȷ����(����)��
�ٳ�����OH��������Ϊ(n��m)g
��ǡ���ܽ����Һ�е�NO3�������ʵ���Ϊ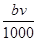 mol
mol
�۷�Ӧ������ת�Ƶĵ�����Ϊ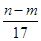 mol
mol
�ܱ�״��������NO�����Ϊ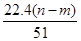 L
L
����Ͻ�Ӧ����������ʵ���Ϊ(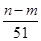 ��
��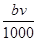 )mol
)mol
| A��5�� | B��4�� | C��3�� | D��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������������Ӧ��
��Cl2+FeI2=FeCl2+I2
��2Fe2++Br2=2Fe3++2Br��
��Co2O3+6HCl=2CoCl2+Cl2��+3H2O
����˵����ȷ���ǣ� ��
| A����Ӧ�٢ڢ��е���������ֱ���I2��Fe3+��CoCl2 |
| B���������Ϸ���ʽ���Եõ������ԣ�Cl2>Fe3+>Co2O3 |
| C���ڷ�Ӧ���е�1 mol Co2O3�μӷ�Ӧʱ��2 mol HCl������ |
| D�����������õ�Cl2+FeBr2 =FeCl2+Br2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com