
【题目】某校化学兴趣小组探究![]() 与
与![]() 溶液的反应,所用装置如下图所示
溶液的反应,所用装置如下图所示![]() 夹持仪器已略去
夹持仪器已略去![]() 。
。
![]() 实验室配制和保存
实验室配制和保存![]() 溶液应滴加少许______于试剂瓶中。
溶液应滴加少许______于试剂瓶中。
![]() 实验过程中需要配制
实验过程中需要配制![]()
![]() 溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管、______。
溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管、______。
![]() 该小组同学向5mL
该小组同学向5mL![]()
![]() 溶液中通入足量的
溶液中通入足量的![]() ,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是______。
,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是______。
![]() 该小组同学在
该小组同学在![]() 中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象,最终溶液呈浅绿色。
中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象,最终溶液呈浅绿色。
(查阅资料)![]() 离子在溶液中呈红棕色且具有较强的还原性,能被
离子在溶液中呈红棕色且具有较强的还原性,能被![]() 氧化为
氧化为![]() 与
与![]() 溶液反应生成红棕色
溶液反应生成红棕色![]() 离子的离子方程式是______;
离子的离子方程式是______;![]() 与
与![]() 在溶液中反应的离子方程式是______。
在溶液中反应的离子方程式是______。
![]() 为了安全起见,还可以在A、B装置之间加一个______装置。
为了安全起见,还可以在A、B装置之间加一个______装置。

![]() 若实验中用5mL一定浓度的浓
若实验中用5mL一定浓度的浓![]() 与适量Cu片充分反应,实验结束后,测得产生
与适量Cu片充分反应,实验结束后,测得产生![]() 的体积在标准状况下为672mL,向已冷却的A试管溶液中加入
的体积在标准状况下为672mL,向已冷却的A试管溶液中加入![]() 的NaOH溶液30mL时,恰好使
的NaOH溶液30mL时,恰好使![]() 完全沉淀。则所用浓
完全沉淀。则所用浓![]() 浓度为______。
浓度为______。![]() 忽略过程中溶液的体积变化
忽略过程中溶液的体积变化![]()
【答案】稀盐酸 100mL的容量瓶 先无现象,后生成白色沉淀 ![]()
![]() 防倒吸
防倒吸 ![]()
【解析】
![]() 氯化铁溶液是强酸弱碱盐的溶液,铁离子水解生成氢氧化铁和盐酸;
氯化铁溶液是强酸弱碱盐的溶液,铁离子水解生成氢氧化铁和盐酸;
![]() 据配制一定物质的量浓度的溶液的步骤选择需要的仪器,计算、称量、溶解、冷却转移、洗涤转移、定容摇匀、静置得到;
据配制一定物质的量浓度的溶液的步骤选择需要的仪器,计算、称量、溶解、冷却转移、洗涤转移、定容摇匀、静置得到;
![]() 溶液中通人足量的
溶液中通人足量的![]() ,溶液最终呈浅绿色,为
,溶液最终呈浅绿色,为![]() 溶液,溶液显酸性;
溶液,溶液显酸性;
![]() 与
与![]() 溶液反应生成红棕色
溶液反应生成红棕色![]() 离子,
离子,![]() 离子可以将
离子可以将![]() 还原为
还原为![]() ,根据氧化还原反应特征书写离子方程式;
,根据氧化还原反应特征书写离子方程式;
![]() 间需要连接一个安全瓶,防止B中液体倒吸如A;
间需要连接一个安全瓶,防止B中液体倒吸如A;
![]() 的体积在标准状况下为672mL,物质的量为
的体积在标准状况下为672mL,物质的量为![]() ,根据电子得失守恒:
,根据电子得失守恒:![]() ,则
,则![]() ,完全沉淀
,完全沉淀![]() 需
需
要NaOH的物质的量为![]() ,
,![]() 为
为![]() ,即
,即![]() 为
为![]() ,而A试管溶液中加入
,而A试管溶液中加入![]() 的NaOH溶液30mL,即
的NaOH溶液30mL,即![]() ,说明反应后
,说明反应后![]() 过量,过量的
过量,过量的![]() 为
为![]() ,根据硫守恒可知5mL一定浓度的浓
,根据硫守恒可知5mL一定浓度的浓![]() 中含有
中含有![]() 共
共![]() ,最后根据
,最后根据![]() 来解答。
来解答。
![]() 实验室配制和保存
实验室配制和保存![]() 溶液应滴加少许稀盐酸抑制其水解,
溶液应滴加少许稀盐酸抑制其水解,
故答案为:稀盐酸;
![]() 配制
配制![]() 溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管、100mL的容量瓶,
溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管、100mL的容量瓶,
故答案为:100mL的容量瓶;
![]() 溶液显酸性,滴入NaOH溶液时,开始无现象,然后产生白色沉淀,
溶液显酸性,滴入NaOH溶液时,开始无现象,然后产生白色沉淀,
故答案为:开始无现象,然后产生白色沉淀;
![]() 与
与![]() 溶液反应生成红棕色
溶液反应生成红棕色![]() 离子反应的离子方程式为:
离子反应的离子方程式为:![]() ,
,![]() 离子可以将
离子可以将![]() 还原为
还原为![]() ,则由氧化还原反应有升必有降,离子方程式为:
,则由氧化还原反应有升必有降,离子方程式为:![]() ;
;
故答案为:![]() ;
;![]() ;
;
![]() 为了安全起见,还可以在A、B装置之间加一个防倒吸的装置,
为了安全起见,还可以在A、B装置之间加一个防倒吸的装置,
故答案为:防倒吸;
![]() 的体积在标准状况下为672mL,物质的量为
的体积在标准状况下为672mL,物质的量为![]() ,根据电子得失守恒:
,根据电子得失守恒:![]() ,则
,则![]() ,完全沉淀
,完全沉淀![]() 需
需
要NaOH的物质的量为![]() ,
,![]() 为
为![]() ,即
,即![]() 为
为![]() ,而A试管溶液中加入
,而A试管溶液中加入![]() 的NaOH溶液30mL,即
的NaOH溶液30mL,即![]() ,说明反应后
,说明反应后![]() 过量,过量的
过量,过量的![]() 为
为![]() ,根据硫守恒可知5mL一定浓度的浓
,根据硫守恒可知5mL一定浓度的浓![]() 中含有
中含有![]() 共
共![]() ,其物质的量浓度为
,其物质的量浓度为![]() ;
;
故答案为:![]() 。
。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】常温下将0.1000mol·L-1的AgNO3标准溶液分别滴加到20mL浓度均为0.1000mol·L-1的NaCl和NaBr溶液中,混合溶液的pAg [-lgc(Ag+)]与滴定百分数(滴定所用标准溶液体积相对于滴定终点时所用标准溶液体积的百分数)的变化关系如图所示。下列叙述错误的是
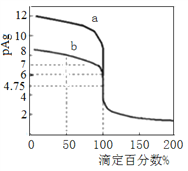
A. 曲线a代表滴定NaBr溶液
B. Ksp(AgCl) =1×10-9.5
C. 滴定至50%时,NaCl溶液中c(Na+) >c(NO3-)>c(Ag+)>c(H+)
D. 滴定至100%时,c(H+) +c(Ag+) = c(Br-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将金属M的样品2.5g放入50g 19.6%的硫酸溶液中,恰好完全反应(样品中的杂质既不溶于硫酸,也不与其发生反应),生成硫酸盐。实验测知,此硫酸盐中硫、氧元素的质量分数之和为80 %。试求:
(1)原金属样品中,金属M的质量分数_____
(2)M的相对原子质量__________
(3)反应所得的硫酸盐溶液中溶质的质量分数___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下HF的电离常数Ka=3.3×10-4 mol·L-1,CaF2的溶度积常数Ksp=1.46×10-10(mol·L-1)3。在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是( )
A.该温度下,0.31 mol·L-1的HF溶液的pH=2
B.升高温度或增大浓度,HF的电离平衡常数都将增大
C.两溶液混合不会产生沉淀
D.向饱和的CaF2溶液中加水后,c(Ca2+)一定比加水前减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是一种重要的金属资源,工业上制取镁单质主要是电解法。
(1)电解法制取镁单质的反应方程式是:___。
(2)电解原料无水氯化镁可由海水制备。主要有以下步骤:①在一定条件下脱水干燥;②海水中加熟石灰;③加盐酸;④过滤;⑤蒸发浓缩冷却结晶。其步骤先后顺序是___(步骤可重复使用),
(3)上述步骤①中“一定条件下”具体是指:___,其目的是___。
(4)已知某温度下Mg(OH)2的Ksp=6.4×l012,当溶液中c(Mg2+)≤1.0×105mol·L1可视为沉淀完全,则此温度下应保持溶液中c(OH-)≥___mol·L1。
(5)将饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,可看到白色沉淀溶解溶液变澄清。反应原理可能有两方面,请分别用离子方程式表示:
①____;
②____。
要验证①②谁是Mg(OH)2溶解的主要原因,可选取___代替NH4Cl溶液作对照实验。
A.NH4NO3 B.(NH4)2SO4 C.CH3COONH4 D.NH4HCO3
(6)镁电池是近年来科学技术研究的热点之一。一种“镁—次氯酸盐”电池的总反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-。其工作时正极的电极反应式:___;用此镁电池给铅蓄电池充电,下列说法中正确的是___。
A.镁电池正极与铅蓄电池正极相连
B.电子从Pb电极转移到镁电池负极
C.充电后,铅蓄电池两极质量均减小,理论上镁电池消耗24gMg,阴、阳极的质量变化之比为3︰2
D.充电后,镁电池和铅蓄电池的pH均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法正确的是
A.pH相等的两溶液:c(CH3COO-)=c(Cl-)
B.等浓度的盐酸和醋酸中和相同物质的量的NaOH时,盐酸的体积小
C.同pH值时,稀释相同倍数后,醋酸溶液的pH值大
D.等pH值的盐酸和醋酸与铁粉反应,产生气体的速率盐酸快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 蛋白质、纤维素、蔗糖、![]() 、淀粉都是高分子化合物
、淀粉都是高分子化合物
B. 蔗糖在人体内水解的产物只有葡萄糖
C. 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用
D. 石油、煤、天然气、可燃冰都是化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中常用FeS作为沉淀剂除去工业废水中的Pb2+,反应原理为FeS(s)+Pb2+(aq) ![]() PbS(s)+Fe2+(aq),下列有关叙述错误的是( )
PbS(s)+Fe2+(aq),下列有关叙述错误的是( )
A.达到平衡时,c(Pb2+)=c(Fe2+)
B.Ksp(FeS)大于Ksp(PbS)
C.该反应的平衡常数K=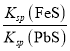
D.溶液中加入少量Na2S固体后,c(Fe2+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,几种常见弱酸的Ka如下表所示[已知草酸(H2C2O4)是一种二元弱酸]:
弱酸 | H2C2O4 | CH3COOH | HCN | H2CO3 |
Ka | K1=5.6×10-2 K2=5.4×10-5 | 1.8×10-5 | 6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
(1)25 ℃时,0.1 mol·L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3溶液的pH由大到小的顺序是________________________,中和等体积等pH的CH3COOH和HCN溶液消耗NaOH的物质的量________(填“前者大”或“后者大”)。
(2)KHC2O4溶液呈酸性。向10 mL 0.01 mol·L-1的H2C2O4溶液滴加0.01 mol·L-1KOH溶液V(mL),回答下列问题:
①当V<10 mL时,反应的离子方程式为________________________________。
②当V=10 mL时,溶液中HC2O![]() 、C2O
、C2O![]() 、H2C2O4、H+的浓度从大到小的顺序为_____________________。
、H2C2O4、H+的浓度从大到小的顺序为_____________________。
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O![]() )+c(HC2O
)+c(HC2O![]() );当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O
);当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O![]() )+c(HC2O
)+c(HC2O![]() )+c(H2C2O4);则a________(填“<”“=”或“>”)b。
)+c(H2C2O4);则a________(填“<”“=”或“>”)b。
④当V=20 mL时,再滴入NaOH溶液,则溶液中n(K+)/n(C2O![]() )的值将________(
)的值将________(
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com