
【题目】常温下将0.1000mol·L-1的AgNO3标准溶液分别滴加到20mL浓度均为0.1000mol·L-1的NaCl和NaBr溶液中,混合溶液的pAg [-lgc(Ag+)]与滴定百分数(滴定所用标准溶液体积相对于滴定终点时所用标准溶液体积的百分数)的变化关系如图所示。下列叙述错误的是
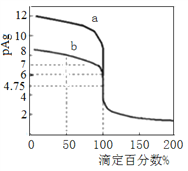
A. 曲线a代表滴定NaBr溶液
B. Ksp(AgCl) =1×10-9.5
C. 滴定至50%时,NaCl溶液中c(Na+) >c(NO3-)>c(Ag+)>c(H+)
D. 滴定至100%时,c(H+) +c(Ag+) = c(Br-)+c(OH-)
【答案】C
【解析】A、根据图中信息可知,由pAg [-lgc(Ag+)]的定义,AgBr的溶度积较小,故pAg较大,曲线a代表滴定NaBr溶液,选项A正确;B、当滴定百分数为100%时,pAg=4.75,说明c(Ag+)=c(Cl-)=10-4.75,Ksp(AgCl) = c(Ag+)c(Cl-)=1×10-9.5, 选项B正确;C、滴定至50%时,pAg=8, c(Ag+)=10-8,若不考虑银离子水解c(H+)=10-7,NaCl溶液中c(H+)>c(Ag+),选项C错误;D、滴定至100%时c(NO3-)= c(Na+),根据电荷守恒有c(H+) +c(Ag+)+ c(Na+) = c(Br-)+c(OH-)+ c(NO3-),故c(H+) +c(Ag+) = c(Br-)+c(OH-),选项D正确。答案选C。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】![]() 时,向100mL
时,向100mL![]()
![]() 溶液中滴加
溶液中滴加![]() NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图
NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图![]() 视为二元强酸)。下列说法错误的是 ( )
视为二元强酸)。下列说法错误的是 ( )

A.a点时溶液的![]()
B.c点时离子浓度大小顺序为:![]()
C.de段上的点均满足关系式:![]()
D.a点到b点的过程中,溶液的导电能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)![]() Y(g)+Z(s),下列选项不能作为反应达到平衡标志的是
Y(g)+Z(s),下列选项不能作为反应达到平衡标志的是
A. 反应容器中压强不再变化 B. 混合气体的密度不再变化
C. 混合气体的平均相对分子质量不再变化 D. Z的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在某密闭容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示。下列叙述中,正确的是
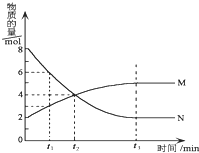
A.该反应的化学方程式为![]()
B.若![]() ,则反应开始至
,则反应开始至![]() 时间段M 的反应速率为
时间段M 的反应速率为![]()
C.![]() 时正逆反应速率相等,反应达到平衡状态
时正逆反应速率相等,反应达到平衡状态
D.![]() 时正反应速率等于逆反应速率
时正反应速率等于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬及其化合物具有广泛应用。请回答下列问题:
(1)![]() 与
与![]() 的化学性质相似。向
的化学性质相似。向![]() 溶液中加入过量NaOH溶液,反应的离子方程式为______;加热
溶液中加入过量NaOH溶液,反应的离子方程式为______;加热![]() 溶液,灼烧固体,所得固体的成分是______。
溶液,灼烧固体,所得固体的成分是______。
(2)![]() 和
和![]() 在溶液中可相互转化
在溶液中可相互转化![]() 室温下,初始浓度为
室温下,初始浓度为![]() 的
的![]() 溶液中
溶液中![]() 随
随![]() 的变化如图所示。
的变化如图所示。
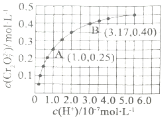
①下列可判断反应达平衡状态的是______![]() 填标号
填标号![]() 。
。
A.溶液的pH不再变化
B.![]()
C.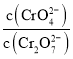 为定值
为定值
②A点![]() 点的逆反应速率大小为
点的逆反应速率大小为![]() 逆
逆![]() ______
______![]() 逆
逆![]() 填:“
填:“![]() ”、“=”或“
”、“=”或“![]() ”
”![]() 。
。
③由图得出,溶液酸性增强,![]() 的平衡转化率______
的平衡转化率______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() ;
;![]() 时,该反应的平衡常数为______。
时,该反应的平衡常数为______。
(3)化学分析中采用![]() 为指示剂,以
为指示剂,以![]() 标准溶液滴定溶液中的
标准溶液滴定溶液中的![]() ,利用
,利用![]() 与
与![]() 生成砖红色沉淀,指示到达滴定终点。硝酸银标准液应盛放在______
生成砖红色沉淀,指示到达滴定终点。硝酸银标准液应盛放在______![]() 填:“酸式”、“碱式”
填:“酸式”、“碱式”![]() 滴定管中。
滴定管中。
(4)常温下,铬酸![]() ,
,![]() ,
,![]() 溶液中离子浓度由大到小的顺序为______。
溶液中离子浓度由大到小的顺序为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知:CO2(g)+H2(g) H2O(g) +CO(g) ΔH1 = + 41.1 kJmol-1
CO(g)+2H2(g) CH3OH(g) ΔH2=-90.0 kJmol-1
写出CO2催化氢化合成甲醇的热化学方程式:___________________________________________。
(2)为提高CH3OH产率,理论上应采用的条件是_______(填字母)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),下图为不同投料比[n(H2)/n(CO2)]时某反应物X平衡转化率变化曲线。
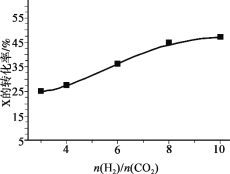
反应物X是_______(填“CO2”或“H2”)。
(4)250℃、在体积为2.0L的恒容密闭容器中加入6mol H2、2mol CO2和催化剂,10min时反应达到平衡,测得c(CH3OH) = 0.75 mol· L-1。
①化学平衡常数K = _______。
②催化剂和反应条件与反应物转化率和产物的选择性有高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
实验编号 | 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
A | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
B | 543 | Cu/ZnO纳米片 | 11.9 | 72.7 |
C | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
D | 553 | Cu/ZnO纳米片 | 12.0 | 70.6 |
根据上表所给数据,用CO2生产甲醇的最优选项为_______(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在湿法炼锌的电解循环溶液中,较高浓度的![]() 会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去
会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去![]() 。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是

A. ![]() 的数量级为
的数量级为![]()
B. 除![]() 反应为Cu+Cu2++2
反应为Cu+Cu2++2![]() =2CuCl
=2CuCl
C. 加入Cu越多,Cu+浓度越高,除![]() 效果越好
效果越好
D. 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgc(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]。下列说法不正确的是( )

A. Ksp[Cu(OH)2]的数量级为10-20
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(Fe2+)∶c(Cu2+)=104.6∶1
C. 除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO
D. 向Z点对应的饱和溶液中加入少量NaOH固体,可转化为Y点对应的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:

(1)滴定盐酸的曲线是图__________(填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________( ![]() )。
)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________mol/L。
(4)若同pH同体积的下列溶液:①醋酸溶液;②盐酸溶液分别用氢氧化钠中和,所需氢氧化钠物质的量较大的是 _______________(填序号)。
Ⅱ.重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0,ρ=1 g/mL)中含有
Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
难溶电解质 | AgI | AgOH | Ag2S |
Ksp | 8.3×1012 | 5.6×108 | 6.3×1050 |
难溶电解质 | PbI2 | Pb(OH)2 | PbS |
Ksp | 7.1×109 | 1.2×1015 | 3.4×1028 |
(1)你认为往废水中加入________(填字母序号),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=_____。
(3)如果用食盐处理只含Ag+的废水,测得处理后的废水(ρ=1 g/mL)中NaCl的质量分数为0.117%,若环境要求排放标准为c(Ag+)低于1×108mol/L,问该工厂处理后的废水中Ag+是否符合排放标准? _______已知Ksp(AgCl)=1.8×1010。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com