
【题目】甘氨酸亚铁[(NH2CH2COO)2Fe,M=204g/mol]是一种补铁强化剂,广泛用于缺铁性贫血的预防和治疗。某化学实验小组利用FeCO3与甘氨酸反应制备甘氨酸亚铁,实验过程如下:
已知:①甘氨酸亚铁易溶于水,难溶于酒精。②甘氨酸具有两性,易溶于水,微溶于酒精:柠檬酸易溶于水和酒精,具有强酸性和强还原性。
I.制备FeCO3:
实验小组将足量的废铁屑和500mL1.0mol·L-1稀硫酸反应,再与200mL1.0mol·L-1NH4HCO3溶液充分混合,装置如图,反应结束后过滤并洗涤沉淀。
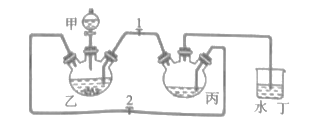
(1)仪器甲的名称为__。
(2)丙中发生反应的离子方程式为__。
(3)实验时先打开止水夹2,关闭止水夹1,加入药品,塞上塞子,待丁中产生大量气泡后,关闭止水夹2,打开止水夹1,观察到的现象为__。
II.制备(NH3CH2COO)2Fe:
将步骤I得到的沉淀全部转移到仪器B,同时加入200mL1.0mol·L-1甘氨酸溶液和适量柠檬酸。通入氮气,通过A向B中加入适量氢氧化钠溶液调节pH为6,充分反应。
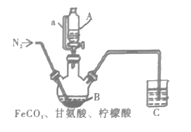
(4)仪器a的作用是__。
(5)实验过程前通入氮气的目的是__,C的导管插入液面下的作用是__。
(6)柠檬酸的作用是__。
(7)反应结束后,将B中液体蒸发浓缩,加入___(填试剂名称),过滤、洗涤并干燥得15.3g甘氨酸亚铁,则其产率是__%(假设上述各步反应均完全)。
【答案】分液漏斗 Fe2++2HCO3-=FeCO3↓+CO2↑+H2O 乙内有气泡产生,液体沿长导管进入丙,丙中产生沉淀 平衡气压,便于液体流下 排尽装置内的空气,防止氧化二价铁 便于吸收尾气,同时防止空气进入B中 促进FeCO3溶解和防止Fe2+被氧化 乙醇 75.0
【解析】
根据实验装置可知,将甲中盛有稀硫酸,乙中放置足量的废铁屑,二者反应生成FeSO4,再通过产生的氢气加压,流入丙装置与200mL1.0mol·L-1NH4HCO3溶液充分混合,产生FeCO3,最后与甘氨酸反应生成甘氨酸亚铁。柠檬酸具有强酸性可以提供氢离子,具有强还原性,可以抗氧化;由于甘氨酸亚铁易被氧化,反应过程中要隔绝空气,甘氨酸亚铁难溶于酒精,故可用酒精洗涤。
I (1)观察装置,可知仪器甲的名称为分液漏斗;
(2)丙中发生的反应为硫酸亚铁与碳酸氢铵反应生成碳酸亚铁沉淀,同时生成二氧化碳,离子方程式为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
(3)关闭止水夹2,打开止水夹1,乙中继续反应产生氢气,形成压强,从而将乙中液体压入装置丙,观察到的现象是乙内有气泡产生,液体沿长导管进入丙,丙中产生沉淀;
II (4)仪器a上下连通,作用是平衡气压,使液体顺利流下;
(5)亚铁离子具有还原性,易被空气中的氧气氧化,实验前通入氮气,排尽装置内的空气,防止氧化二价铁;将C中导管没入液面以下,可以充分吸收尾气,同时防止空气中的氧气进入B装置将亚铁离子氧化;
(6)根据题中的已知信息,柠檬酸具有强酸性和强还原性,合成过程加入柠檬酸的可促进FeCO3溶解和防止亚铁离子被氧化;
(7)依题意,甘氨酸亚铁难溶于酒精,加入乙醇可降低溶解度,使其结晶析出;稀硫酸和铁屑过量,碳酸氢铵的物质的量=0.2L×1.0mol·L-1=0.2mol,产生0.1mol的碳酸亚铁,根据铁原子守恒,0.2mol甘氨酸和0.1mol碳酸亚铁理论上生成0.1mol甘氨酸亚铁,理论上可产生甘氨酸亚铁的质量:204g·mol-1×0.1mol=20.4g,产品的质量为15.3g,则产率=![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
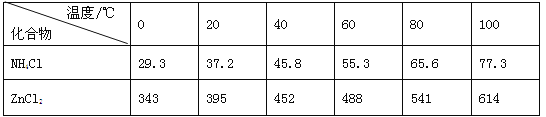
【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为___,电池反应的离子方程式为___。
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn___g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过___分离回收;滤渣的主要成分是MnO2、___和_______,欲从中得到较纯的MnO2,最简便的方法是___,其原理是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是我国科学家研制的一种新型化学电池,成功实现了废气的处理和能源的利用(H2R和R都是有机物)。下列说法不正确的是( )
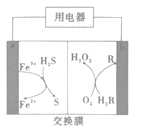
A.电池工作时,电子从电极b流出
B.负极区,发生反应2Fe3++H2S=2Fe2++S+2H+
C.电池工作时,负极区要保持呈酸性
D.电路中每通过2mol电子,理论上可处理标准状况下H2S22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年全球气候变暖,造成北极冰川大面积融化,其罪魁之一就是CO2,如何吸收大气中的CO2,变废为宝,是当今化学研究的主题之一。
I.二甲醚可用作溶剂、冷冻剂喷雾剂等,科学家提出利用CO2和H2合成二甲醚,反应原理为2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) H
CH3OCH3(g)+3H2O(g) H
(1)已知:①H2O(g)+CO(g)![]() CO2(g)+H2(g) △H1=+42kJ/mol
CO2(g)+H2(g) △H1=+42kJ/mol
②CH3OCH3(g)+H2O(g)![]() 2CH3OH(g) H2=+24.52kJ/mol
2CH3OH(g) H2=+24.52kJ/mol
③CH3OH(g)![]() CO(g)+2H2(g) H3=+90.73kJ/mol
CO(g)+2H2(g) H3=+90.73kJ/mol
则H=__kJ/mol。
(2)一定温度下,在一个2L的密闭容器中充入2molCO2和6molH2发生上述反应,经过5min反应达到平衡,此时容器中压强与起始压强之比为3:4,则用CH3OCH3表示的平均反应速率为__,H2的转化率为___;此时若向体系中再加入2molCO2和1.5molH2O(g),平衡__移动(填正向、逆向、不)。
(3)对于恒温恒容条件下进行的反应①,下列说法能说明反应已达平衡的是__。
A.混合气体密度不发生改变
B.混合气体的平均相对分子质量不再发生改变
C.v(CO)正=v(H2)逆
D.n(CO)与n(H2)的比值不变
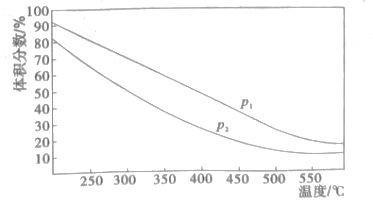
(4)一定温度下,密闭容器中进行的反应③,测得平衡时混合物中某物质的体积分数在不同压强下随温度的变化如图所示,则纵坐标表示的物质是__,压强P1_P2(填>、<)。
II.工业锅炉长期煮烧会形成锅垢(主要成分CaSO4、Mg(OH)2),必须定期除去。
(5)CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO32-=CaCO3+SO42-,室温下,该反应的化学平衡常数为__(室温下,Ksp(CaCO3)=3×10-9,Ksp(CaSO4)=9×10-6)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A. 小苏打溶液呈弱碱性:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
B. 测0.1mol/L氨水的pH为11:NH3·H2O![]() NH4++OH-
NH4++OH-
C. pH=5的硫酸稀释1000倍,pH约等于7:H2O![]() H++OH-
H++OH-
D. 用Na2CO3处理水垢中CaSO4:CaSO4(s)+CO32-(aq)![]() SO42-(aq)+CaCO3(s)
SO42-(aq)+CaCO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2FeCl2+Cl2=2FeCl3。现有铁粉、氯气、氧化铁和盐酸四种物质,试用三种方法制取FeCl3(用化学方程式表示)。
(1)___________________。
(2)__________________。
(3)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到实验目的且符合操作要求的是

A. I可用于制备并检验氢气的可燃性
B. II可用于除去CO2中的HCl
C. 用Ⅲ来配制一定物质的量浓度的NaOH溶液
D. 用IV中操作制备氢氧化亚铁并观察其颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+ ![]() O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x_____________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是__________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
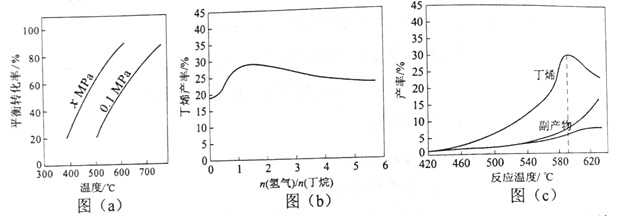
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com