
一系列物质:NaCl、Cl2、NaClO、Cl2O5、HClO4是按某一规律排列的,下列组合中也完全照此规律排列的是( )
A、Na2CO3 C CO2 CO NaHCO3
B、Na2S S SO2 Na2SO3 Na2SO4
C、NH4Cl N2 NaNO2 NO2 HNO3
D、P2O5 H3PO4 Na3PO4 Na2HPO4 NaH2PO4
科目:高中化学 来源: 题型:
只给出下列甲和乙中对应的量,不能求出物质的量的是 ( )
| A | B | C | D | |
| 甲 | 物质的粒子数 | 标准状况下的气体摩尔体积 | 固体的体积 | 溶液中溶质的物质的量浓度 |
| 乙 | 阿伏加德罗常数 | 标准状况下的气体体积 | 固体的密度 | 溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,H2(g)+CO2(g)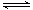 H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=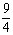 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.一定温度下,反应MgCl2(l)=Mg(l) + Cl2(g)的 △H>0 △S>0
B.“NO2球”浸泡在冷水中,颜色变浅:2NO2(g) 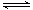 N2O4(g)
N2O4(g)  H<0
H<0
C.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
D.对于反应2H2O2=2H2O+O2↑, 加入MnO2或升高温度都能加快O2的生成速率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列的分离方法正确的是( )
A.用萃取的方法除去花生油中的水份
B.用过滤的方法除去NaCl溶液中含有的少量淀粉
C.用酒精萃取碘水中的碘
D.用蒸馏的方法除去水中的不挥发的杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液氯离子的物质的量浓度与50 mL 1 mol/LAlCl3溶液中氯离子的物质的量浓度相等的是( )
A.50 mL3 mol/L氯酸钠溶液
B.75 mL 1mol/L氯化钙溶液
C.150 mL 3 mol/L氯化钾溶液
D.50 mL 3 mol/L氯化镁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,1体积水溶解336体积氯化氢,所得溶液密度为1.1g/cm3,溶液中气体的物质的量浓度和溶质的质量分数分别为( )
A.10.7mol/L 35.4% B.14.8 mol/L 28.8%
C.14.8 mol/L 35.4% D.10.7mol/L 28.8%
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属,且与R同周期。下列叙述不正确的是 ( )
A.离子半径大小:R3+<X+< M2-
B.Y与M组成的化合物是光化学烟雾的原因之一
C.将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生
D.M氢化物的熔沸点高于Z氢化物的熔沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有______个。
②LiBH4由Li+和BH4-构成,BH4 -呈正四面体构型。LiBH4中不存在的作用力有______(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为______。
(2) 金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+______H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:

M是______(填元素符号)。
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有______种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com