
【题目】400℃时,将一定量的SO2和14molO2压入一个盛有催化剂的10L密闭容器中进行反应:2SO2+O22SO3。已知2min时,容器中剩余2molSO2和12molO2。试计算:
(1)SO2的起始物质的量浓度__________________。
(2)2min内SO3的反应速率____________________。
【答案】0. 6 mol·L-1 0. 2 mol·L-1·min-1
【解析】
先计算出氧气的浓度的变化量,根据变化量之比等于化学计量数之比计算出SO2 和SO3的浓度的变化量,再用三段法进行计算。
根据c=![]() ,开始时容器内有14molO2,O2的物质的量浓度为1. 4 mol·L-1,2min时容器中剩余2molSO2和12molO2,,2min时容器中剩余SO2和O2物质的量浓度分别为:0. 2 mol·L-1,1. 2 mol·L-1,设SO2的起始物质的量浓度为x,根据变化量之比等于化学计量数之比,写出该反应的三段式如下:
,开始时容器内有14molO2,O2的物质的量浓度为1. 4 mol·L-1,2min时容器中剩余2molSO2和12molO2,,2min时容器中剩余SO2和O2物质的量浓度分别为:0. 2 mol·L-1,1. 2 mol·L-1,设SO2的起始物质的量浓度为x,根据变化量之比等于化学计量数之比,写出该反应的三段式如下:

SO2的起始物质的量浓度x=0. 2 mol·L-1+0. 4 mol·L-1=0. 6 mol·L-1;2min内SO3的反应速率v=![]() =0. 2 mol·L-1·min-1,答案为:0. 6 mol·L-1;0. 2 mol·L-1·min-1。
=0. 2 mol·L-1·min-1,答案为:0. 6 mol·L-1;0. 2 mol·L-1·min-1。


科目:高中化学 来源: 题型:
【题目】借助太阳能将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如下图所示。下列说法不正确的是
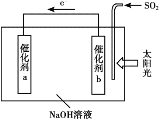
A. 该装置可将太阳能转化为化学能
B. 催化剂b附近的溶液pH增大
C. 吸收1mol SO2,理论上能产生1mol H2
D. 催化剂a表面发生的反应为:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯轻质CaCO3广泛应用于橡胶、塑料、油漆等行业。一种以磷石膏(主要成分为CaSO4,含少量SiO2和Al2O3)为原料制备轻质高纯CaCO3的流程如图:

下列说法错误的是( )
A.“转化”时发生反应的离子方程式为CaSO4+2NH3+CO2+H2O=CaCO3+2NH4++SO42-
B.“转化”时应先通入CO2,再通入NH3
C.实验室“过滤”时用到的玻璃仪器有玻璃棒、漏斗、烧杯
D.“浸取”过程中会有NH3生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种常见物质的转化关系如图所示(部分反应物及产物略去),其中W、M、X含有某种相同的元素。下列说法错误的是( )

A.若X为O2,则W可能为二氧化碳
B.若X为Al(OH)3,则Y可能为稀硫酸
C.若X为Fe,则Y可能为稀硝酸
D.若X为NaHCO3,则M可能为二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型二次电池反应原理为M+3Cn(MCl4)+4MC14-![]() 4M2C17-+3Cn(M代表金属,Cn代表石墨)。装置如图所示。下列说法正确的是
4M2C17-+3Cn(M代表金属,Cn代表石墨)。装置如图所示。下列说法正确的是
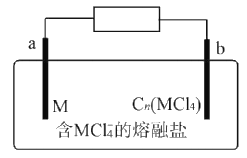
A. 放电时,MCl4-向b极迁移
B. 放电时,a极反应为M-3e-+7MCl4-=4M2Cl7-
C. 充电时,阳极反应式为Cn+MCl4-+e-=Cn(MCl4)
D. 电路上每转移lmol电子最多有3 mol Cn(MCl4)被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向密闭容器中充入等物质的量的NO和CO,发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。当上述化学反应达到平衡时,下列叙述正确的是( )
N2(g)+2CO2(g)。当上述化学反应达到平衡时,下列叙述正确的是( )
A.CO2和CO的物质的量一定相等
B.NO和CO2的物质的量一定相等
C.反应物的转化率达到了该条件下的最大限度
D.平衡时混合物的总物质的量一定等于反应开始前混合物的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向体积为2L的恒容密闭容器中通入2molN2和6molH2,在一定条件下发生反应:N2(g)+3H2(g)![]() 2NH3(g)。实验测得反应经5min后达到平衡,此时混合物的总物质的量为5.6mol,求:
2NH3(g)。实验测得反应经5min后达到平衡,此时混合物的总物质的量为5.6mol,求:
(1)平衡时NH3的浓度为___mol·L-1。
(2)0~5min内,v(H2)=___mol·L-1·min-1。
(3)反应达到平衡时,N2的转化率为___。
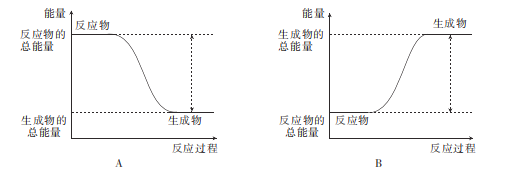
(4)下列图象中能反映该反应的能量变化的是___(填标号)。
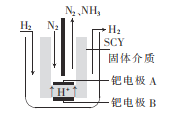
(5)若以N2和H2合成氨的反应设计如图所示的原电池,则通入N2的一极为__(填“正”或“负")极;负极的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生产聚苯乙烯的流程如下,下列叙述不正确的

A.乙苯的分子式为C8H10B.聚苯乙烯属于高分子化合物
C.lmol苯乙烯最多可与3mol H2发生加成反应D.鉴别苯与苯乙烯可用酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 120g NaHSO4晶体中含有NA个SO42-
B. 6.2 g氧化钠和7.8 g过氧化钠的混合物中含有的阴离子总数为0.2NA
C. 4.6g钠用铝箔包裹并刺小孔,与足量水充分反应生成氢气分子数为0.1NA
D. NH4Cl+NaNO2=N2↑+NaCl+2H2O,每生成0.1mol N2,转移电子数为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com