
【题目】下列各组离子在溶液中能大量共存的是
A.Na+、H+、Cl-、OH-B.Ag+、K+、Cl-、NO3–
C.Na+、H+、NO3– 、CO32-D.H+、Mg2+、SO42–、Cl-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】化学与社会、生活密切相关,下列有关物质的用途和原理分析正确的是
选项 | 物质的用途 | 原理和分析 |
A | 漂白粉可用于食品漂白 | 漂白粉能使色素褪色 |
B | Al(OH)3可中和胃酸 | Al(OH)3是两性氢氧化物,与酸发生中和反应 |
C | Na2O2常作供氧化 | Na2O2在常温下能分解放出O2 |
D | 明矾可作净水剂 | 明矾溶于水后能消毒杀菌 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铝粉与某铁的氧化物FeO2Fe2O3粉末配制成铝热剂,分成两等份.一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为( )
A.11.20L
B.15.68L
C.22.40L
D.31.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的物质,可用于制取化肥和硝酸等.已知H﹣H键、N﹣H键、N≡N键的键能分别是436kJ/mol、391kJ/mol、946kJ/mol.
(1)写出合成氨的热反应方程式 .
生成1molNH3需要吸收或放出kJ
(2)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中t1 时引起平衡移动的条件可能是 . 其中表示平衡混合物中NH3的含量最高的一段时间是 . 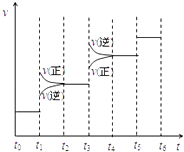
(3)温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为 .
(4)已知373K时,可逆反应平衡常数为K=0.12,若某时刻时,测得 C(N2)=1mol/L,C(H2)=3mol/L,C(NH3)=2mol/L.此刻可逆反应
A.向正方向进行
B.向逆方向进行 C处于平衡状态.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一小块钠暴露在空气中一段时间,发生的反应是
①4Na+O2═2Na2O ②2Na+O2═Na2O2
③Na2O+H2O═2NaOH ④2NaOH+CO2═Na2CO3+H2O
A. ① B. ②④ C. ①③ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有22.4L氯气和氢气的混合气体,在一密闭容器中使其反应,冷却后将此气体通入足量的氢氧化钠溶液中,共消耗1.5molNaOH,则原混合气体中氯气和氢气的体积比为
A. 2:1 B. 1:1 C. 1:2 D. 3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学常见物质,它们在一定条件下有如下转化关系(副产物已略去)。
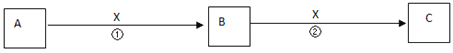
(1)若X是氧气,则A不可能______________A.CB.Si C.NaD.Mg
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生了不溶于稀HNO3的白色沉淀,则B的化学式为__________;C溶液在贮存时应加入少量X,理由是(用离子方程式表示)___________ 。检验B溶液中阳离子的操作方法是_________________。
(3)若X是氢氧化钠溶液,A、B、C均为含铝元素的化合物,则反应②的离子方程式为________________
(4)若X为盐酸,A、B、C均不含铝元素,且反应②有无色无味气体生成,则反应①的离子方程式为___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质的说法,正确的是
A. 金属导电,属于电解质 B. 乙酸是有机物,属于非电解质
C. 只有在水溶液中能够导电的物质才属于电解质 D. NaCl和Al2O3在熔融状态下均导电,都属于电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com