
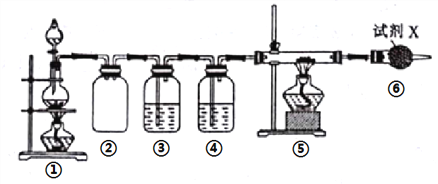
【题目】短周期元素A、B、C、D、E、F的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,A和D同主族,B和C相邻,F的最高价氧化物对应的水化物为无机含氧酸中的最强酸。E与B可构成化合物E3B2,且该物质遇水发生水解反应。已知利用如下装置以制备E3B2,装置①用于制备B单质。下列说法错误的是( )
A. E与B的简单离子的电子层结构相同,且离子半径B>E
B. ③、④、⑥中依次盛装的试剂可以是NaOH溶液浓H2SO4、碱石灰
C. A、B、C三种元素组成的化合物可能与F的最高价氧化物对应的水化物反应
D. 实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝
【答案】B
【解析】短周期元素A、B、C、D、E、F的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,则A为H元素,B为N元素;A和D同主族,则D为Na元素;B和C相邻,C为O元素;F的最高价氧化物对应的水化物为无机含氧酸中的最强酸,F为Cl元素。E与B可构成化合物E3B2,且该物质遇水发生水解反应,E为+2价金属,为Mg元素;根据装置图,在装置⑤中制备Mg3N2,装置①用于制备N2,装置②为安全瓶,③④用于除去氮气中杂质并干燥,装置⑥防止空气中的水蒸气进入装置⑤。A. 电子层结构相同的离子,核电荷数越大,离子半径越小,Mg与N的简单离子的电子层结构相同,离子半径B>E,故A正确;B. 饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气,NaNO2+NH4Cl![]() NaCl+N2↑+2H2O,氮气中的杂质主要是空气中的氧气,氧气能够与镁反应,需要除去,用NaOH溶液不能除去,故B错误;C. A、B、C三种元素组成的化合物可能为氨水,能够与高氯酸反应,故C正确;D. Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓,氨气的水溶液显碱性,可以使试管口湿润的红色石蕊试纸变蓝,故D正确;故选B。
NaCl+N2↑+2H2O,氮气中的杂质主要是空气中的氧气,氧气能够与镁反应,需要除去,用NaOH溶液不能除去,故B错误;C. A、B、C三种元素组成的化合物可能为氨水,能够与高氯酸反应,故C正确;D. Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓,氨气的水溶液显碱性,可以使试管口湿润的红色石蕊试纸变蓝,故D正确;故选B。


科目:高中化学 来源: 题型:
【题目】硒(Se)、碲(Te)为VIA族元素,是当今高新技术新材料的主要成分之一,电解精炼铜的阳极泥主要成分为Cu2Te、Ag2Se和少量金属单质及其他化合物,工业上从其中回收碲、硒的一种工艺流程如下:

已知:
I.Se 单质难溶于水。TeO2微溶于水,易溶于较浓的强酸和强碱;
II.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
III.25℃时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
(1)Se的氢化物的电子式是_______________。0.1mol/L的H2TeO3电离度(当弱电解质在溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来总分子数的百分数叫做电离度) 约为_____________________。
(2) 加入浓硫酸焙烧前常将阳极泥中大块颗粒先粉碎,其目的是_______________________。
(3) SeO2 与SO2在冷却后通入水中反应的化学方程式_________________________________。反应后分离出Se单质的操作①为_________________(填操作名称)。
(4)焙砂中碲以TeO2形式存在,与足量NaOH溶液反应后得到的溶液①,其溶质的主要成分为_______(填化学式,过量的NaOH除外)。工业上也可以通过电解溶液①得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为__________________________________。
(5)向溶液①中加入硫酸时控制溶液的pH 为4.5~5.0,生成TeO2沉淀,如果H2SO4过量,将导致碲的回收率__________(填“偏高”、“偏低”或“无影响”)。
(6)将纯净的TeO2先溶于盐酸得到四氯化碲,然后再将SO2通入到溶液中得到Te单质,请写出由四氯化碲得到Te单质的离子方程式________________________________。
(7)上述流程中可循环利用的物质_______________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是
A.最高化合价为+2B.原子半径比钠的大
C.单质与水的反应比钠更剧烈D.最高价氧化物对应的水化物碱性比钠的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构简式如图所示,下列说法错误的是( ) 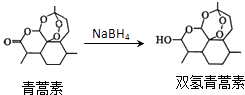
A.青蒿素易溶于苯,难溶于水
B.由青蒿素制备双氢青蒿素的反应属于 还原反应
C.青蒿素可与NaOH溶液在一定条件下发生水解反应
D.双氢青蒿素的同分异构体不可能有芳香族化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据以下装置回答相关问题 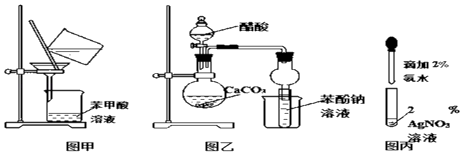
(1)图甲是一套进行操作的装置,可以除去粗苯甲酸中所含的杂质.
(2)利用图乙装置来证明醋酸、碳酸、苯酚酸性的相对强弱时,实验过程中,苯酚钠溶液中所出现的实验现象是 . 该实验中存在的缺陷是未除去(填化学式下同)中可能混有的
(3)图丙是做乙醛的银镜反应前配制银氨溶液的实验操作图.配制过程中,试管内发生变化的现象是 . 配好银氨溶液后,向其中加入乙醛进行银镜反应时,为了获得良好的实验效果,对试管采用的加热方式是 . 乙醛发生银镜反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且Y原子核外p电子比s电子多5个。
(1)Z基态原子的核外电子排布式为__________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯(![]() )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1mol丙烯分子中含有σ键与π键数目之比为_______。
②苯分子中碳原子轨道的杂化类型为__________。
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为_______个。
(3)W、X、Y三种元素的电负性由小到大顺序为__________。(请用元素符号回答)
(4)ZY3熔点为1152℃,熔融状态下能够导电,据此可判断ZY3晶体属于__________(填晶体类型)。
(5)ZX2晶体的晶胞结构如图,每个Z原子周围最近的X 原子数目为__________。若该化合物的相对分子质量为M,晶胞边长为acm,阿伏加德罗常数为NA,则该晶体的密度为_________g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10mol/LKOH溶液滴定10.00mL0.10mol/LH2C2O4(二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).请回答: 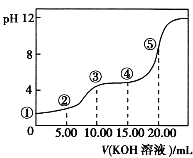
(1)点①所示溶液中,Kw= .
(2)点②所示溶液中的电荷守恒式为 .
(3)点③所示溶液中所有离子的浓度由大到小的顺序为 .
(4)点④所示溶液中的物料守恒式为0.10mol/L= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超临界状态下的CO2流体溶解性与有机溶剂相似,可提取中药材的有效成分,工艺流程如下。下列说法错误的是
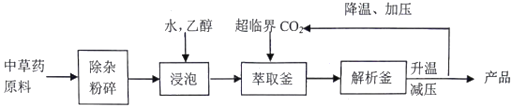
A. 浸泡时加入乙醇有利于中草药有效成分的浸出
B. 高温条件下更有利于超临界CO2萃取
C. 升温、减压的目的是实现CO2与产品分离
D. CO2流体萃取中药材具有无溶剂残留、绿色环保等优点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com