
【题目】电化学在日常生活中用途广泛,图①是镁-次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O72-的工业废水的处理。下列说法正确的是( )

A. 图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B. 图②的电解池中,有0.084g阳极材料参与反应,阴极会有336mL的气体产生(标况)
C. 图①中发生的还原反应是:Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
D. 若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀
【答案】C
【解析】A.图②中惰性电极为阴极,Fe电极为阳极,则Cr2O72-离子向金属铁电极移动,与亚铁离子发生氧化还原反应生成的金属阳离子与惰性电极附近的OH-结合转化成Cr(OH)3除去,故A错误;B.图②的电解池中,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-=H2↑,则n(Fe)=![]() =0.0015mol,阴极气体在标况下的体积为0.0015mol×22.4L/mol =0.0336L=33.6mL,故B错误;C.该原电池中,镁作负极,负极上镁失电子发生氧化反应,负极反应为Mg-2e-=Mg2+,电池反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl-,正极上次氯酸根离子得电子发生还原反应,则总反应减去负极反应可得正极还原反应为Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓,故C正确;D.由电子守恒可知,Mg~2e-~Fe2+,由原子守恒可知Fe2+~Fe(OH)3↓,则n(Mg)=
=0.0015mol,阴极气体在标况下的体积为0.0015mol×22.4L/mol =0.0336L=33.6mL,故B错误;C.该原电池中,镁作负极,负极上镁失电子发生氧化反应,负极反应为Mg-2e-=Mg2+,电池反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl-,正极上次氯酸根离子得电子发生还原反应,则总反应减去负极反应可得正极还原反应为Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓,故C正确;D.由电子守恒可知,Mg~2e-~Fe2+,由原子守恒可知Fe2+~Fe(OH)3↓,则n(Mg)=![]() =0.15mol,理论可产生氢氧化铁沉淀的质量为0.15mol×107g/mol=16.05g,故D错误;故选C。
=0.15mol,理论可产生氢氧化铁沉淀的质量为0.15mol×107g/mol=16.05g,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】已知氮元素及其化合物的转化关系如下图所示,回答下列问题。

(1)①~④各步转化中,属于氮的固定的是_______(填序号)。
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
① 化学方程式是_______。
② 干燥氨气不可选用的试剂是________(填字母)。
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)工业上用氨气制备NO的化学方程式是_______。
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
① 水吸收法。结合化学方程式说明用水吸收NO2的缺陷________。
② NaOH溶液吸收法。发生的反应有:2NaOH + NO + NO2 = 2NaNO2+ H2O,NaOH + NO2—________ + NaNO2 +H2O(填化学式,不需要配平方程式)。
③ 用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:(α 表示尾气里NO、NO2中NO2的含量)

i.根据上图得知_______(填字母)。
a. NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测溶液pH可研究反应过程。用盐酸分别滴定Na2CO3、 NaHCO3溶液,测得pH随加入盐酸体积的变化如下图所示(曲线②从B1点开始滴定)。下列判断不正确的是

A. 曲线①表示用盐酸滴定Na2CO3的过程
B. B、C1点均满足:c(Na+)+c(H+)=2c(CO32-)+c(HCO3ˉ)+c(OHˉ)
C. 曲线①、②说明Na2CO3与盐酸的反应分步进行
D. BC段和B1C1段发生的主要反应均是HCO3ˉ+H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒和镍及其化合物是重要合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的核外电子排布式为________,其排布时能量最高电子所占据能级的原子轨道有________个伸展方向。
(2)VO2+可与多种物质形成配合物,与氧同周期且第一电离能比氧大的主族元素有____(写元素符号)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______,与CN-互为等电子体的一种分子的化学式为__________。
(4)三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF3、H2O2等为主要原料来制取。
①H2O2分子中O原子的杂化方式为________。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为__________。

(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2所示,该晶胞中S2-的配位数为____。
(6)镧镍合金是重要储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为___________。
②该镧镍合金储氢后氢气的密度为________(用NA表示阿伏加德罗常数的数值)g.cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA
B.14g分子式为CnH2n的链烃中含有的C-H键的数目为2NA
C.室温时,1.0 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
D.Fe与水蒸气反应生成22.4L氢气,转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究(NH4)2 SO4 和 NH4HSO4混合物样品组成,称取四份该样品分别逐滴加入相同 浓度的 NaOH 溶液 40.0 mL,加热并完全反应,产生 NH3的体积(已折算成标准状况,
不考虑NH3在水中的溶解)如下表:
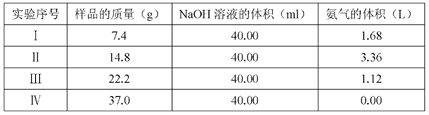
(1)样品中(NH4)2 SO4和NH4HSO4的物质的量之比为_____________。
(2)NaOH 溶液的物质的量浓度为_________________________(精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解槽的叙述不正确的是( )
A. 是电能转变成化学能的装置B. 与电源正极相连的是阳极
C. 阴极失去电子,发生氧化反应D. 参与电解的阳离子移向阴极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com