
 C(g),△H体系中B的百分含量和时间t的关系,下列对△H的数值和表示300℃时的变化曲线的说法正确的是
C(g),△H体系中B的百分含量和时间t的关系,下列对△H的数值和表示300℃时的变化曲线的说法正确的是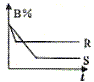
| A.△H<0,R曲线 | B.△H>0,R曲线 |
| C.△H<0,S曲线 | D.△H>0,S曲线 |
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源:不详 题型:实验题
| 反应时间t/h | 1 | 4 | 9 | 16 | 25 |
| MgO层厚y/nm | 0.05a | 0.20a | 0.45a | 0.18a | 1.25a |
| NiO层厚y′/nm | B | 2b | 3b | 4b | 5b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(NH2)2(s)+H2O(g)。将体积比为14:13的NH3与CO2的混合气体置于密闭容器中,若反应达到平衡后增大压强,混合气体的平均相对分子质量 ( )
CO(NH2)2(s)+H2O(g)。将体积比为14:13的NH3与CO2的混合气体置于密闭容器中,若反应达到平衡后增大压强,混合气体的平均相对分子质量 ( )| A.变小 | B.增大 |
| C.不变 | D.可能增大、减小,也可能不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Z(g),压强一定时,测得在平衡时Z的体积分数为0.4。?
2Z(g),压强一定时,测得在平衡时Z的体积分数为0.4。?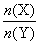 的取值范围为_______。
的取值范围为_______。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
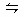 b B(g)+c C(g),在温度不变的条件下,再充入一定量的A 物质,重新达到平衡时,下列判断中正确的是( )
b B(g)+c C(g),在温度不变的条件下,再充入一定量的A 物质,重新达到平衡时,下列判断中正确的是( )| A.若a=b+c时,B的物质的量分数变大 |
| B.若a=b+c时,B的物质的量分数不变 |
| C.若a>b+c时,A的转化率不变 |
| D.若a<b+c时,A的转化率变小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
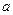 mol A和
mol A和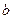 mol B在一个容积可变的容器中发生反应:A(g)+2B(g)
mol B在一个容积可变的容器中发生反应:A(g)+2B(g) 2C(g),一段时间后达到平衡,生成
2C(g),一段时间后达到平衡,生成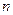 mol C。则下列说法中正确的是 ( )
mol C。则下列说法中正确的是 ( )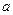 :
: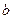
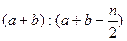
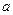 mol A和2
mol A和2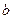 mol B,则达平衡时生成2n mol C
mol B,则达平衡时生成2n mol C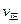 (A)=2
(A)=2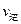 (B)时,可确定反应达平衡
(B)时,可确定反应达平衡查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
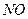 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的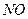 和
和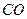 转变成
转变成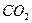 和
和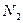 ,化学方程式如下:
,化学方程式如下:

 为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
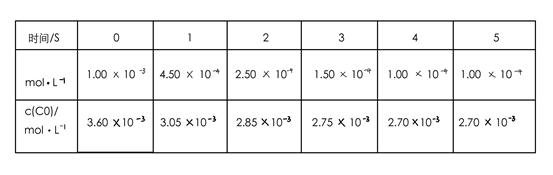

 请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响): (1)在上述条件下反应能够自发进行,则反应的
(1)在上述条件下反应能够自发进行,则反应的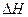 0(填写“>”、“<”、“=”。
0(填写“>”、“<”、“=”。 (2)前2s内的平均反应速率v(N2)=_____________。
(2)前2s内的平均反应速率v(N2)=_____________。 (3)在该温度下,反应的平衡常数K= 。
(3)在该温度下,反应的平衡常数K= 。 (4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
| A.选用更有效的催化剂 | B.升高反应体系的温度 | C.降低反应体系的温度 | D.缩小容器的体积 |
 (5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。

 ①请在上表格中填入剩余的实验条件数据。
①请在上表格中填入剩余的实验条件数据。 ②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。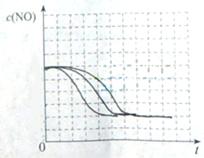
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH3的生成速率与H2的生成速率相等 |
| B.单位时间内生成nmolN2同时生成3nmolN2 |
| C.N2、H2、NH3的浓度不再变化 |
| D.N2、H2、NH3分子数之比为1:3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com