

 Cu2+ + 2NO2↑+ 2H2O 或
Cu2+ + 2NO2↑+ 2H2O 或
 3Cu2+ + 2NO↑+ 4H2O Au、Pt
3Cu2+ + 2NO↑+ 4H2O Au、Pt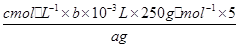 × 100% c
× 100% c
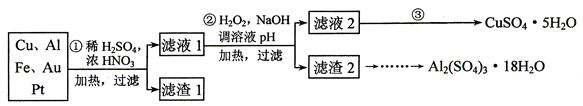
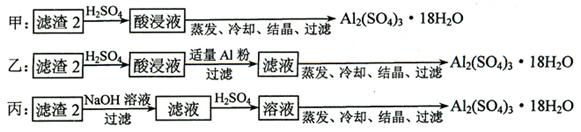
 Cu2+ + 2NO2↑+ 2H2O。由于浓硝酸和硫酸都不能溶解Au或Pt,所以滤渣是1的主要成分为Au、Pt。
Cu2+ + 2NO2↑+ 2H2O。由于浓硝酸和硫酸都不能溶解Au或Pt,所以滤渣是1的主要成分为Au、Pt。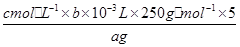 × 100% 。根据表达式可知,如果未干燥锥形瓶,是不会影响实验结果的。若滴定终点时滴定管尖嘴中产生气泡,则消耗标准液的体积将减少,测定结果偏低;如果未除净可与EDTA反应的干扰离子,则消耗标准液的体积将偏大,测定结果偏高,因此答案选C。
× 100% 。根据表达式可知,如果未干燥锥形瓶,是不会影响实验结果的。若滴定终点时滴定管尖嘴中产生气泡,则消耗标准液的体积将减少,测定结果偏低;如果未除净可与EDTA反应的干扰离子,则消耗标准液的体积将偏大,测定结果偏高,因此答案选C。

科目:高中化学 来源:不详 题型:填空题
| A.萃取分液法 | B.加热分解 | C.蒸发结晶法 | D.分液法 E.渗析法 F.蒸馏法 G.过滤法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
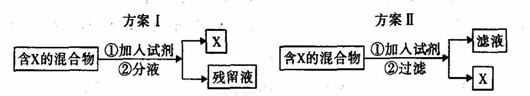
| A.若含X的混合物为混有少量氯气的液溴,可通过方案I进行分离,加入试剂为适量溴化钠溶液 |
| B.若含X的混合物为FeCl3和CuCl2,可通过方案I进行分离,加入试剂为过量铁粉 |
| C.若含X的混合物为碘水,可通过方案I进行分离,加入试剂为CC14液体,充分振荡后液体分层,上层为紫红色的X的CC14溶液 |
| D.若含X的混合物为SiO2和Al2O3,可通过方案II进行分离,加入试剂为过量NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有① | B.只有③ | C.①和③ | D.②和③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.萃取 | B.升华 | C.蒸发 | D.分液 E.蒸馏 F.过滤 |
| 分离或提纯的物质 | 分离方法 |
| 分离BaSO4和BaCl2溶液 | |
| 分离食盐和碘 | |
| 分离花生油和水 | |
| 从碘水中提取碘单质 | |
| 用自来水制取蒸馏水 | |
| 从溶液中获得硫酸钠晶体 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
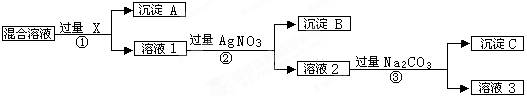
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com