
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
| 4 |
 ,
, .
.


科目:高中化学 来源: 题型:
| A、Na+、Ca2+、HCO3-、Cl- |
| B、Fe3+、NH4+、SCN-、NO3- |
| C、Al3+、K+、Cl-、NO3- |
| D、Cu2+、NO3-、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、M、G五种短周期主族元素,原子序数依次增大.X元素的气态氢化物水溶液呈碱性;Y、M同主族,可形成MY2、MY3两种分子;元素Z和G可形成1:1的离子化合物.请回答下列问题:
X、Y、Z、M、G五种短周期主族元素,原子序数依次增大.X元素的气态氢化物水溶液呈碱性;Y、M同主族,可形成MY2、MY3两种分子;元素Z和G可形成1:1的离子化合物.请回答下列问题:| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
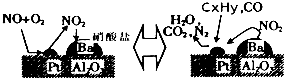
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,有机物F是丁子香酚的一种同分异构体,是有机化工原料,用于合成药物的中间体.某校兴趣小组设计方案合成F,如图所示:
,有机物F是丁子香酚的一种同分异构体,是有机化工原料,用于合成药物的中间体.某校兴趣小组设计方案合成F,如图所示: 试回答下列问题:
试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com