
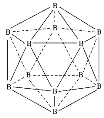
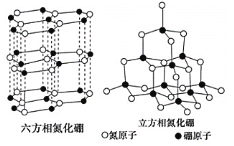
【题目】晶体硼熔点为1873K,其结构单元为正二十面体,结构如图所示。氮化硼(BN)有多种相结构,例如六方相氮化硼与立方相氮化硼,结构如图所示,六方相氮化硼与石墨相似,具有层状结构;立方相氮化硼是超硬材料。回答下列问题:
(1)基态硼原子有___种不同能量的电子,第二周期中,第一电离能介于硼元素与氮元素之间的元素有___种。
(2)晶体硼为___(填晶体类型),结构单元由___个硼原子构成,共含有___个B-B键。
(3)关于氮化硼两种晶体的说法,正确的是___。
a.立方相氮化硼含有σ键和π键
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体均为分子晶体
d.两种晶体中的B-N键均为共价键
(4)NH4BF4是合成氮化硼纳米管的原料之一,1molNH4BF4含有___mol配位键。
【答案】3 3 原子晶体 12 30 bd 2
【解析】
(1)基态硼原子的电子排布式为1s22s22p1,电子位于1s、2s、2p三个能量不同的能级上;同周期元素,从左到右,第一电离能呈增大的趋势,由于全充满和半充满的缘故,ⅡA族和ⅤA族元素第一电离能大于相邻元素;
(2)由晶体硼熔点为1873K可知,晶体硼为熔沸点高、硬度大的原子晶体;在硼原子组成的正二十面体结构中,每5个面共用一个顶点,每个面拥有这个顶点的![]() ,每2个面共用一个B-B键,每个面拥有这个B-B键的
,每2个面共用一个B-B键,每个面拥有这个B-B键的![]() ;
;
(3)a. 由图可知,立方相氮化硼中N原子和B原子之间只存在单键;
b.由图可知,六方相氮化硼层间为分子间作用力,分子间作用力小;
c. 由图可知, 立方相氮化硼为空间网状结构,属于原子晶体;
d. 非金属元素之间易形成共价键;
(4)NH4BF4是由NH4+和BF4—构成,NH4+中N原子和其中一个H原子之间存在配位键、BF4—中B原子和其中一个F原子之间存在一个配位键。
(1)基态硼原子的电子排布式为1s22s22p1,电子位于1s、2s、2p三个能量不同的能级上,则有3种不同能量的电子;同周期元素,从左到右,第一电离能呈增大的趋势,由于全充满和半充满的缘故,ⅡA族和ⅤA族元素第一电离能大于相邻元素,则介于硼元素与氮元素之间的有Be、C、O三种元素,故答案为:3;3;
(2)由晶体硼熔点为1873K可知,晶体硼为熔沸点高、硬度大的原子晶体;在硼原子组成的正二十面体结构中,每5个面共用一个顶点,每个面拥有这个顶点的![]() ,每个等边三角形拥有的顶点为
,每个等边三角形拥有的顶点为![]() ,20个等边三角形拥有的顶点为
,20个等边三角形拥有的顶点为![]() ×20=12;每2个面共用一个B-B键,每个面拥有这个B-B键的
×20=12;每2个面共用一个B-B键,每个面拥有这个B-B键的![]() ,每个等边三角形占有的B-B键为
,每个等边三角形占有的B-B键为![]() ,20个等边三角形拥有的B-B键为
,20个等边三角形拥有的B-B键为![]() ×20=30,故答案为:12;30;
×20=30,故答案为:12;30;
(3)a. 由图可知,立方相氮化硼中N原子和B原子之间只存在单键,则立方相氮化硼中含有σ键,不存在π键,故错误;
b.由图可知,六方相氮化硼层间为分子间作用力,分子间作用力小,导致其质地软,故正确;
c. 由图可知, 立方相氮化硼为空间网状结构,属于原子晶体,故错误;
d. 非金属元素之间易形成共价键,所以N原子和B原子之间存在共价键,故正确;
bd正确,故答案为:bd;
(4)NH4BF4是由NH4+和BF4—构成,NH4+中N原子和其中一个H原子之间存在配位键、BF4—中B原子和其中一个F原子之间存在一个配位键,所以含有2个配位键,则1mol NH4BF4含有2mol配位键,故答案为:2。


科目:高中化学 来源: 题型:
【题目】某温度下,C和H2O(g)在密闭容器里发生下列反应:
①C(s)+H2O(g)![]() CO(g)+H2(g), ②CO(g)+H2O(g)
CO(g)+H2(g), ②CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,c(H2)=1.9 mol·L-1,c(CO)=0.1 mol·L-1。则下列叙述正确的有
A. CO在平衡时转化率为10%
B. 平衡浓度c(CO2)=c(H2)
C. 平衡时气体平均相对分子质量约为23.3
D. 其他条件不变时,缩小体积,H2O(g)的转化率随之降低
查看答案和解析>>
科目:高中化学 来源: 题型:
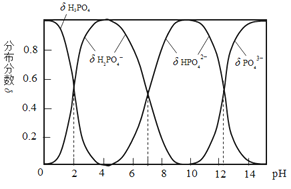
【题目】磷酸(H3PO4)是一种中强酸,常温下,H3PO4水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓度的分数)与pH的关系如图,下列说法正确的是( )
A.H3PO4的电离方程式为:H3PO4![]() 3H++ PO43
3H++ PO43
B.pH=2时,溶液中大量存在的微粒有:H3PO4、H2PO4、HPO42、PO43
C.滴加NaOH溶液至pH=7,溶液中c(Na+)= c(H2PO4)+2c(HPO42)+3c(PO43)
D.滴加少量Na2CO3溶液,3Na2CO3+2H3PO4 =2Na3PO4+3H2O+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应H2(g)+I2(g)2HI(g)在一定的条件下反应混合物中各组分的浓度(mol·L-1)与时间t(min)的变化曲线如图所示,根据图示,回答
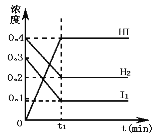
(1)时间t1的意义是_________
(2)在时间0至t1的间隔里,v(H2) =________________
(3)此平衡状态下,H2的转化率为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,将浓度均为0.1mol/L的HA溶液Va mL和BOH溶液Vb mL混合,保持Va+Vb=100mL,生成物BA易溶于水。Va、Vb与混合液pH的关系如下图。下列叙述错误的是

A.HA一定是弱酸
B.BOH可能是强碱
C.z点时,水的电离被促进
D.x、y、z点时,溶液中都存在c(A-)+c(OH-)=c(B+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2可用于防腐剂、消毒剂,也是一种重要的冷冻介质。实验室可用如图所示装置制备SO2,并用纯净SO2进行相关实验。
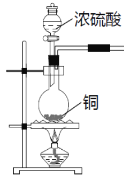
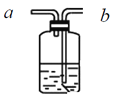
(1)上述方法制备的SO2中,往往因伴有硫酸小液滴而呈白雾状。除去白雾可在制备装置后连接下图所示装置,该装置中的试剂是__________,气体从_______口(填“a”或“b”)进。
(2)检验SO2常用的试剂是__________________,利用了SO2的_________性。
(3)将SO2通入0.1mol/L Ba(NO3)2溶液中,得到白色沉淀,该沉淀的化学式为___________。
分别用煮沸和未煮沸过的蒸馏水配制Ba(NO3)2和BaCl2溶液,进行如下实验:
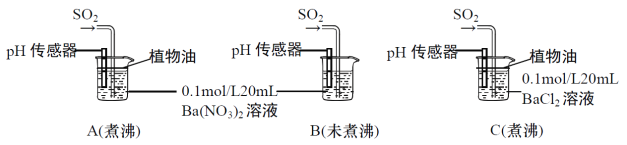
(4)实验A、C中,煮沸蒸馏水及使用植物油的目的是_________________________________。
(5)实验C中,没有观察到白色沉淀,但pH传感器显示溶液呈酸性,原因是__________________。(用方程式表示)
(6)实验B中出现白色沉淀比实验A快很多。由此得出的结论是___________________________。若实验A、B中通入足量的SO2后,溶液pH:A_________B(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确认乙酸、碳酸和硅酸的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液)。

(1)锥形瓶内装有某种可溶性正盐固体(含有3种酸的酸根的其中一种),此固体为________,分液漏斗中所盛试剂是___。
(2)装置B中所盛试剂的名称是________,试剂的作用是__________。
(3)装置C中出现的现象是__________________。
(4)由实验可知三种酸的酸性大小顺序为________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、N2中的几种,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )

A.NO2、N2B.NO、CO2
C.NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将一根较纯的铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重。下列关于此现象的说法错误的是( )
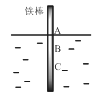
A.该腐蚀过程属于电化腐蚀
B.铁棒AB段电极反应为O2 + 2H2O+ 4e-→ 4OH-
C.铁棒AB段是负极,BC段是正极
D.产生此现象的根本原因是铁棒所处化学环境的不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com