
【题目】下列电离方程式书写错误的是
A. MgCl2=Mg2++2Cl B. NaOH=Na++O2+H+
C. HCl=H+ +Cl D. K2SO4=2K++SO42
科目:高中化学 来源: 题型:
【题目】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
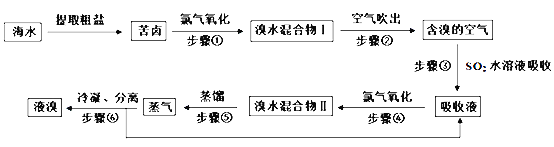
(1)步骤①获得Br2的离子反应方程式为:_________________________。
(2)步骤③所发生反应的化学方程式为:_________________________。在该反应中,氧化剂是______________(填化学式);若反应中生成2molHBr,则转移电子数约为_____________个。
(3)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是:_______________。
(4)步骤②通入热空气或水蒸气吹出Br2,利用了溴的________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(5)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸乙酯具有抗炎作用且有治疗自身免疫性疾病的潜力,其合成路线及部分反应机理如图所示:
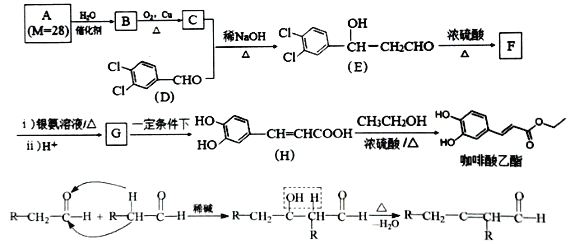
回答下列问题:
(1)B中官能团的名称是______________________。
(2)E→F反应类型为______________________。
(3)D分子中位于同一平面上的原子最多有___________个。
(4)F的结构简式为______________________。
(5)H→咖啡酸乙酯的化学方程式为____________________________________________。
(6)芳香族化合物M是H的同分异构体,1molM与足量碳酸氢钠溶液反应生成2molCO2,M的三取代基结构有___________种;M的两取代基同分异构体核磁共振氢谱为5组峰,峰面积比为1:2:2:2:1,其结构简式为______________________。
(7)设计以甲醛、C为原料合成C5H12O4(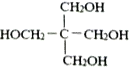 )的路线(无机试剂任选)。___________________________。
)的路线(无机试剂任选)。___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2.3 g钠投入38.8 g水中,发生化学反应。假设水蒸发损失1 g,所得溶液中溶质的质量分数为( )
A. 4.6% B. 7.7% C. 10.0% D. 8.0%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的 ΔH=—99kJ·mol-1。请回答下列问题:

(1)图中A、C分别表示________、_________,E的大小对该反应的反应热有无影响?_______。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________,理由是_________________________。
(2)图中△H=____________kJ·mol-1。
(3)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=_________υ(SO3)=___________。
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求写出计算过程)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D四种短周期元素的原子半径依次减小,D能分别与A,B,C形成电子总数相等的分子X、Y、Z。C原子的最外层电子排布为nsnnp2n。E的原子序数为29。
(1)A,B,C的第一电离能由小到大的顺序为________(用元素符号表示)。
(2)X是含有________键(填“非极性”或“极性”,下同)的________分子。
(3)A的一种氢化物的相对分子质量为26,其分子中的σ键与π键的键数之比为________。
(4)Y分子的空间构型为__________,其中心原子采取________杂化。
(5)一种由B,C组成的化合物与AC2互为等电子体,其化学式为________。
(6)Y是一种易液化的气体,请简述其易液化的原因_________。
(7)写出E2+的电子排布式___________________,并写出E2+在Z中通入足量Y得到深蓝色溶液的离子反应方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示的过程中的能量变化情况,判断下列说法正确的是

A. H2(g)转化为氢原子是一个放热过程
B. 1molH2和1molCl2的总能量比2molHCl的总能量低
C. 1 个 HCl(g)分子中的化学键断裂时需要吸收431.8 kJ能量
D. 2HCl(g)= H2(g)+Cl2(g)的反应热ΔH=+184.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究黑色固体 X(仅含两种元素)的组成和性质,设计并完成如下实验:
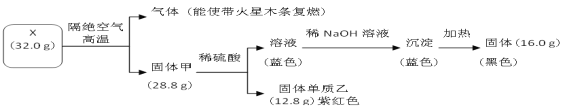
(1)X的化学式是________________。
(2)写出固体甲与稀硫酸反应的离子方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车排放的尾气是大气污染气体之一。如何减少污染气体的排放是科学家研究的热门课题。请回答下列问题:
使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6 mol NO、8 mol CO充入10 L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6 mol NO、8 mol CO充入10 L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。

(1)该反应的化学平衡常数K=____。NO的平衡转化率=______。
(2)15 min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是____(填标号)。
a.缩小容器体积 b.增加CO2的量 c.体积不变通入少量氩气 d.加入催化剂
(3)当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是____(填标号)。
A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大
D.温度不变,增大压强,平衡常数增大
(4)以下说法中能判断反应2NO(g)+2CO(g)![]() N2 (g)+2CO2 (g)达到平衡的是____(填标号)。
N2 (g)+2CO2 (g)达到平衡的是____(填标号)。
A.反应物和生成物的物质的量相等
B.单位时间内生成1 mol NO同时生成1 mol CO2
C.混合气体压强不再发生变化
D.NO的浓度不再变化
(5)向反应容器中再分别充入下列气体,能使NO转化率增大的是____(填标号)。
A.O2 B.N2 C.CO D.NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com