
【题目】咖啡酸乙酯具有抗炎作用且有治疗自身免疫性疾病的潜力,其合成路线及部分反应机理如图所示:
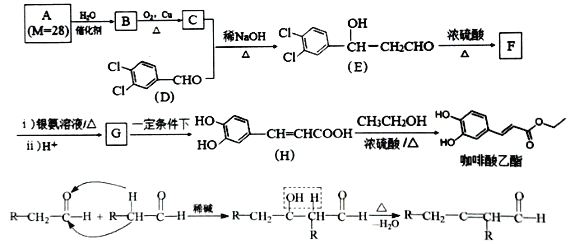
回答下列问题:
(1)B中官能团的名称是______________________。
(2)E→F反应类型为______________________。
(3)D分子中位于同一平面上的原子最多有___________个。
(4)F的结构简式为______________________。
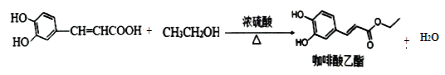
(5)H→咖啡酸乙酯的化学方程式为____________________________________________。
(6)芳香族化合物M是H的同分异构体,1molM与足量碳酸氢钠溶液反应生成2molCO2,M的三取代基结构有___________种;M的两取代基同分异构体核磁共振氢谱为5组峰,峰面积比为1:2:2:2:1,其结构简式为______________________。
(7)设计以甲醛、C为原料合成C5H12O4(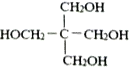 )的路线(无机试剂任选)。___________________________。
)的路线(无机试剂任选)。___________________________。
【答案】羟基 消去反应 14 ![]()
 6
6 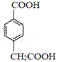
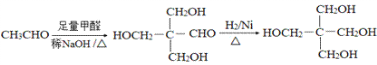
【解析】
A的相对分子质量是28,A是乙烯,与水加成生成B是乙醇,催化氧化生成C是乙醛,C与D发生醛基的加成反应生成E,E在浓硫酸的作用下发生消去反应生成F为![]() ,F发生银镜反应并酸化后生成G为
,F发生银镜反应并酸化后生成G为![]() ,G发生水解反应生成H,H与乙醇发生取代反应生成咖啡酸乙酯。
,G发生水解反应生成H,H与乙醇发生取代反应生成咖啡酸乙酯。
(1)根据上述分析可知,B为乙醇,故所含官能团是:羟基;
本题答案为:羟基。
(2)E→F是E在浓硫酸的作用下发生的消去反应;
本题答案为:消去反应。
(3)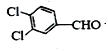 分子中,醛基和苯环均是平面形结构,则D分子中位于同一平面上的原子最多有14个;
分子中,醛基和苯环均是平面形结构,则D分子中位于同一平面上的原子最多有14个;
本题答案为:14。
(4)F是E在浓硫酸的作用下,发生的消去反应,F的结构简式为:![]() ;
;
本题答案为:![]() 。
。
(5)H和乙醇发生酯化反应,生成咖啡酸乙酯和水,其化学方程式为: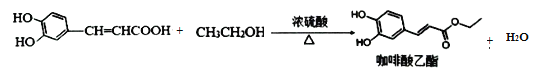 ;
;
本题答案为: 。
。
(6)芳香族化合物M是H的同分异构体,1molM与足量碳酸氢钠溶液反应生成2 mol CO2,说明含有2个羧基,且苯环外只能用3个碳原子,如果苯环上有3个取代基,应该是2个羧基和1个甲基,以羧基为参照,若两个羧基 在临位则有两种结构,若两个羧基在间位则有三种结构,若两个羧基在对位则只有一种结构,可能共有6种结构满足对M的要求,M的两取代基,如果是两个取代基,应该是-COOH和-CH2COOH,其中核磁共振氢谱为5组峰,峰面积比为1∶2∶2∶2∶1的结构简式为![]() ;
;
本题答案为:6,、![]() 。
。
(7)根据已知信息结合逆推法可知以甲醛、C(乙醛)为原料合成C5H12O4的路线为: ;
;
本题答案为: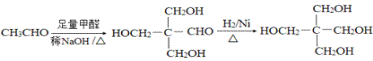 。
。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】根据如图海水综合利用的工业流程图,判断下列说法正确的是
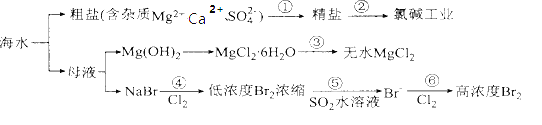
已知:MgCl26H2O受热生成Mg(OH)Cl和HCl气体等.
A.过程①加入的药品顺序为:Na2CO3溶液→BaCl2溶液→NaOH溶液→过滤后加盐酸
B.过程②通过氧化还原反应可产生1种单质
C.在过程③中将MgCl26H2O直接灼烧得到MgCl2
D.在过程④、⑥反应中每氧化0.2molBr-需消耗标准状况下2.24LCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3 kJ·mol1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol1
B. 甲烷的标准燃烧热ΔH=-890.3 kJ·mol1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol1
C. 已知:500℃、30MPa下,N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
D. CO(g)的燃烧热是283.0kJ·mol1,则2CO2(g) ===2CO(g)+O2(g)反应的△H=+566.0 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是
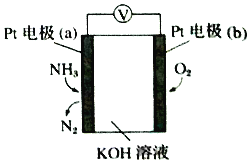
A. O2在电极b上发生还原反应
B. 溶液中OH-向电极a移动
C. 正极的电极反应式为O2+4e-+4H+=2H2O
D. 负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是肉制品生产中最常使用的一种食品添加剂,某化学兴趣小组利用氮氧化物与过氧化钠反应制备亚硝酸钠并进行一系列实验探究。
查阅资料:
①SO2+Na2O2=Na2SO4,NO2和NO能与Na2O2发生类似反应。
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+且有无色气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸。
I.制备亚硝酸钠

(1)装置A用恒压滴液漏斗,相比普通分液漏斗,显著的优点是______________________。
(2)上述装置按气流方向连接的顺序为:A→___________→___________→___________→C(填仪器编号,且都是左进右出)。
(3)如果没有B装置,D中发生反应的化学方程式为_________________________________。(有几个就写几个,填化学方程式)。
(4)C装置的作用是_________________________________(用离子方程式表示)。
Ⅱ.测定产品纯度,实验步骤:
①准确称量5.000g产品配成250mL溶液。
②从步骤①配制的溶液中移取25.00mL注入锥形瓶中。
③用0.1000mol/L酸性KMnO4溶液滴定至终点
④重复以上操作3次,消耗酸性KMnO4溶液的平均体积为20.00mL
(5)达到滴定终点的现象是____________________________________________。产品中NaNO2的纯度为___________%。
(6)设计实验证明HNO2的酸性比碳酸强_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.小苏打溶液中加入烧碱溶液:![]()
B.氯化铝溶液中加入过量氨水:![]()
C.向氯化亚铁溶液中加入氯水:![]()
D.氢氧化钡溶液与稀硫酸混合Ba2++OH-+SO42-+H++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写错误的是
A. MgCl2=Mg2++2Cl B. NaOH=Na++O2+H+
C. HCl=H+ +Cl D. K2SO4=2K++SO42
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常见的混合物分离或提纯的基本装置如下:
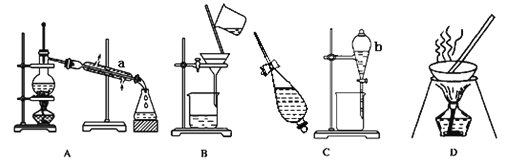
(1)写出仪器名称:a___________,b__________。
(2)从海带提取碘的操作如下,除特殊说明外,请在空白处填上装置中的序号:将干海带进行灼烧,海带灰中含有较多KI,将海带灰溶于水,然后__________得到澄清滤液;向滤液中加入硫酸和H2O2混合溶液,得到棕褐色含有单质碘的水溶液。该反应的离子方程式为:__________________。向碘的水溶液中加入适量CCl4,进行___________操作将上下两层溶液分开。将含有碘的CCl4溶液置于蒸馏烧瓶内进行___________操作,可以粗略从CCl4溶液中分离出碘。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com