
【题目】水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3。某化学兴趣小组用某浓度的Na2CO3溶液处理一定量的CaSO4固体,测得所加Na2CO3溶液体积与溶液中-lgc(CO32-)的关系如下。
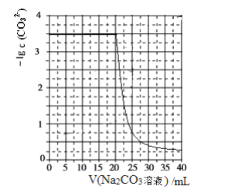
已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是( )
A. 曲线上各点的溶液满足关系式:c(Ca2+)·c(SO42-)=Ksp(CaSO4)
B. CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq) K=3×103
CaCO3(s)+SO42-(aq) K=3×103
C. 该Na2CO3溶液的浓度为1mol/L
D. 相同实验条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则上图曲线整体向上平移1个单位即可
【答案】D
【解析】
A. CaSO4的溶度积表达式Ksp(CaSO4)= c(Ca2+)·c(SO42-),A项正确;
B. CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq)的化学平衡常数
CaCO3(s)+SO42-(aq)的化学平衡常数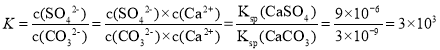 ,B项正确;
,B项正确;
C. 依据上述B项分析可知,CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq) K=3×103,每消耗1mol CO32-会生成1mol SO42-,在CaSO4完全溶解前溶液中的c(SO42-)等于Na2CO3溶液的浓度,设Na2CO3溶液的浓度为1mol/L,则c(SO42-)=1mol/L,根据
CaCO3(s)+SO42-(aq) K=3×103,每消耗1mol CO32-会生成1mol SO42-,在CaSO4完全溶解前溶液中的c(SO42-)等于Na2CO3溶液的浓度,设Na2CO3溶液的浓度为1mol/L,则c(SO42-)=1mol/L,根据![]() 可得溶液中c(CO32-)=
可得溶液中c(CO32-)=![]() ,-lg c(CO32-)=3.5,与图像相符,C项正确;
,-lg c(CO32-)=3.5,与图像相符,C项正确;
D. 依据题意可知,起始CaSO4的物质的量为0.02mol,相同实验条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则消耗碳酸钠的体积为10mL,在CaSO4完全溶解前溶液中的c(SO42-)=2mol/L,根据![]() 可得溶液中c(CO32-)=
可得溶液中c(CO32-)=![]() ,-lg c(CO32-)=3.2,图像中的横纵坐标都要改变,D项错误;
,-lg c(CO32-)=3.2,图像中的横纵坐标都要改变,D项错误;
答案选D。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】周期表中前20号元素W、X、Y、Z的原子序数依次增大,W、X、Y三种元素所在周期序数之和等于7,这四种元素可组成中学常见的离子化合物ZYWX,其常用于检测溶液中的某种金属阳离子;W、X、Y组成一种共价化合物分子(X![]() W—Y—Y—W
W—Y—Y—W![]() X),该分子中每个原子最外层都达到8电子稳定结构。下列推断正确的是( )
X),该分子中每个原子最外层都达到8电子稳定结构。下列推断正确的是( )
A.W的氢化物的熔点一定比X的低
B.Z2Y是只含一种化学键的离子化合物
C.Y的氧化物对应的水化物一定是强酸
D.简单离子的半径大小:Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的合金及其配合物用途非常广泛。已知![]() 比
比![]() 的氧化性更强,在水溶液中不能大量存在.
的氧化性更强,在水溶液中不能大量存在.
(1)![]() 的核外电子排布式为_____________。
的核外电子排布式为_____________。
(2)无水![]() 的熔点为
的熔点为![]() 、沸点为
、沸点为![]() ,
,![]() 熔点为
熔点为![]() 、沸点为
、沸点为![]() .
.![]() 属于_______晶体,
属于_______晶体,![]() 属于_____晶体。
属于_____晶体。
(3)![]() 可用于激光起爆器等,可由
可用于激光起爆器等,可由![]() 、
、![]() 、
、![]() 共反应制备.
共反应制备.
①![]() 的空间构型为______________________。
的空间构型为______________________。
②![]() 的化学式为
的化学式为![]() ,与
,与![]() (III)形成配位键的原子是_____
(III)形成配位键的原子是_____
已知![]() 的结构式是
的结构式是![]()
③![]() 可以
可以![]() (双聚氰胺)为原料制备,
(双聚氰胺)为原料制备,![]() 双聚氯胺分子中含
双聚氯胺分子中含![]() 键的数目为___________。
键的数目为___________。
(4)![]() 与
与![]() 作用可生成
作用可生成![]() ,其结构如图所示,该分子中
,其结构如图所示,该分子中![]() 原子的杂化方式为_____________________________。
原子的杂化方式为_____________________________。

(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为______。已知![]() 为阿伏加德罗常数的数值,则该晶胞的密度为______(用含
为阿伏加德罗常数的数值,则该晶胞的密度为______(用含![]() 、
、![]() 、
、![]() 的代数式表示)
的代数式表示)![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中的28号元素Ni有重要的用途,它有良好的耐高温、耐腐蚀、防锈功能,在电池、催化剂方面也有广泛应用。工业上以硫化镍矿(含少量杂质硫化铜、硫化亚铁)为原料制备并精制镍的基本流程如下:

已知:电极电位(E)能体现微粒的氧化还原能力强弱,如:
H2-2e-=2H+ E=0.00V Cu-2e-=Cu2+ E=0.34V
Fe-2e-=Fe2+ E=-0.44V Ni-2e-=Ni2+ E=-0.25V
(1)镍在周期表中的位置为_______________________________。
(2)高镍矿破碎细磨的作用______________________________________。
(3)焰色反应实验可以用光洁无锈的镍丝代替铂丝蘸取化学试剂灼烧,原因是______________________。
(4)造渣除铁时发生的化学反应方程式___________________________________(产物以氧化形式表示)。
(5)电解制粗镍时阳极发生的主要电极反应式_____________________________________。
(6)工业上由NiSO4溶液制得Ni(OH)2后,再滴加NaC1O溶液,滴加过程中发生反应的离子方程式为_________________________________________________________。
(7)电解精炼镍的过程需控制pH为2~5,试分析原因______________________________,阳极泥的成分为________________(写名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M、N是合成某功能高分子材料的中间产物,下列关于M、N说法正确的是( )
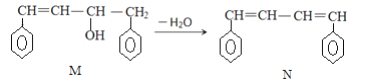
A. M、N都属于烯烃,但既不是同系物,也不是同分异构体
B. M、N分别与液溴混合,均发生取代反应
C. M、N分子均不可能所有原子共平面
D. M、N均可发生加聚反应生成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为2CH3OH+3O2+4KOH==2K2CO3+6H2O。下列说法正确的是( )

A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应为CH3OH - 6e- +2H2O=CO32- +8H+
C.甲池中消耗280mL(标准状况下)O2,此时乙池中银极增重1.6g
D.反应一段时间后,向丙池中加入一定量盐酸,一定能使NaCl溶液恢复到原浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素A、B、C、D和E的原子序数依次增大。A、B、C、D四种元素核电荷数均小于20,A、B同主族;B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1;E是周期表中(除放射性元素外)第一电离能最小的元素。回答下列问题:
(1)写出下列元素的符号:A 、E 。
(2)C元素的价电子排布图为: ;
该排布遵循的原理主要有: (答完整得分)。
(3)C、D元素形成的化合物主要有: (填化学式,答完整得分);其中相对分子质量较小的分子为 分子(填“极性”或“非极性”),该分子的空间构型为 ,中心原子的杂化方式是 。
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为 ;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于 形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中![]() 和
和![]() 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。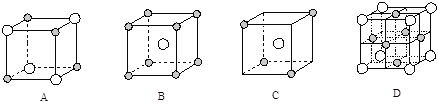
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关盐类水解的说法中,不正确的是( )。
A. 盐类的水解过程破坏了纯水的电离平衡
B. 盐类的水解是酸碱中和反应的逆反应
C. 盐类水解后的溶液不一定显中性
D. ![]() 溶液中,
溶液中, ![]() 是
是![]() 的两倍
的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积的关系如图,下列说法正确的是( )
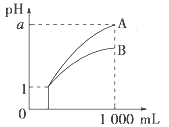
①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A. ①④ B. ②③ C. ①③ D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com