
����Ŀ����ͼ��ʾ���׳ص��ܷ�ӦʽΪ2CH3OH+3O2+4KOH==2K2CO3+6H2O������˵����ȷ���ǣ� ��

A���׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҡ������ǻ�ѧ��ת�����ܵ�װ��
B���׳�ͨ��CH3OH�ĵ缫��ӦΪCH3OH - 6e- +2H2O=CO32- +8H+
C���׳�������280mL����״���£�O2����ʱ��������������1.6g
D����Ӧһ��ʱ����������м���һ����������һ����ʹNaCl��Һ�ָ���ԭŨ��
���𰸡�C
��������
����A���׳���ȼ�ϵ�أ��ǻ�ѧ��ת��Ϊ���ܵ�װ�ã��ң����ǵ����ǽ�����ת��Ϊ��ѧ�ܵ�װ����A������B��ȼ�ϵ���У������Ǽ״�����ʧ���ӵ�������Ӧ���ڼ��Ե�����µĵ缫��ӦΪ��CH3OH-6e-+2H2O+8OH-��CO32-+8H2O��B����C���׳��и��ݵ缫��Ӧ��O2+2H2O+4e-=4OH-������280ml�������Ϊ0.0125mol��O2��ת��0.05mol���ӡ��ҵ�������缫��ԭ����е����������������ص�������������ӦΪCu��2e����Cu������������ת���غ��֪����ͭ��0.025mol��������1.6��C��ȷ��D�����Ե缫�������ʳ��ˮ�����������ơ���������������Ӧһ��ʱ�����������ͨ��һ�����Ȼ�������������ʹNaCl��Һ�ָ���ԭŨ����D��������ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼��þ(������FeCO3)Ϊԭ����ȡ����þ���壬���ⶨMg2+��������ԭ����ȫ����һ������ϡ�����У���������H2O2���ð�ˮ������Һ��pH�����ú���ˣ���ȥ����������Һ�ᾧ������þ���塣
��1��30.00mL 5.00 mol��L1��ϡ�����������ܽ�ԭ�ϵ�����Ϊ___________��
��2���Ӱ�ˮ����pH�ٽ�Fe3+ˮ�⣬Fe3+ˮ�����ӷ���ʽΪ___________��
��3����֪��Ksp[Fe(OH)3]��1.0��1039��Ksp[Mg(OH)2]��1.0��1012�������£�����Һ��c(Mg2��)��0.01mol��L1����ʹ��Һ�е�c(Fe3��)��1��106mol��L1���������ҺpH��ΧΪ___________��
��4�����������з����ⶨ�ᾧ����þ��Mg2+�ĺ�����
��֪������pHΪ9~10ʱ��Mg2+��Zn2+������EDTA(H2Y2)�γ������
����pHΪ5~6ʱ��Zn2+������EDTA��Ӧ�����ܽ�Mg2+��EDTA�γɵ�������е�Mg2+���û��������� Zn2+ +MgH2Y��ZnH2Y+Mg2+
����1��ȷ��ȡ�õ�������þ����1.50g���������EDTA�����100mL pH9~10֮����ҺA
����2��ȷ��ȡ25.00mL��ҺA����ƿ�У���0.10mol��L1Zn2+����Һ�ζ����ζ����յ㣬����Zn2+����Һ�����Ϊ20.00mL
����3��ȷ��ȡ25.00mL��ҺA����һֻ��ƿ�У�����pH��5~6����0.10mol��L1Zn2+����Һ�ζ����ζ����յ㣬����Zn2+����Һ�����Ϊ30.00mL��
����ýᾧ����þ��Mg2+����������(������������)��___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ŵ�����һ���������ʪ�Թؽ���ҩ���ͨ�����·����ϳɣ�
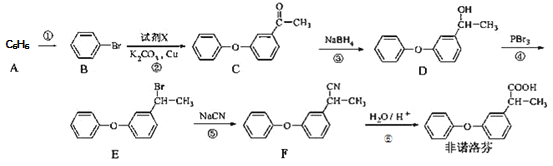
�ش���������
(1)![]() �Ļ�ѧ������_____________��
�Ļ�ѧ������_____________��![]() �к��������ŵ�����Ϊ___________��
�к��������ŵ�����Ϊ___________��
(2)������Ӧ�У���Ӧ�ٵ�������___________�����̢�����______��Ӧ
(3)��Ӧ�ڷ�������ȡ����Ӧ������һ�ֲ�����![]() ��д����
�����![]() ����
����![]() �Ļ�ѧ����ʽ______��
�Ļ�ѧ����ʽ______��
(4)�л���![]() ���ŵ�һ�Ϊͬ���칹�壬
���ŵ�һ�Ϊͬ���칹�壬![]() ��������������
��������������
I������NaHCO3��Һ��Ӧ��������FeCl3��Һ������ɫ��Ӧ
II����������6�ֲ�ͬ��ѧ�������⣬�ҷ����к�����������
![]() �Ľṹ��_____�֣�д������һ�ֲ�����Ũ��ˮ����ȡ����Ӧ��
�Ľṹ��_____�֣�д������һ�ֲ�����Ũ��ˮ����ȡ����Ӧ��![]() �Ľṹ��ʽ_________��
�Ľṹ��ʽ_________��
(5)��������֪ʶ����������Ϣ��д����![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ�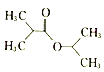 ·������ͼ(���Լ�����)_________
·������ͼ(���Լ�����)_________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ba(OH)2��һ��ǿ������ڲⶨ��Ȼ����CO2�ĺ�����
��1����д����������������Һ����CO2��������ӷ���ʽ��__________��
��2��ij����С��ͨ������ʵ������ⶨBa(OH)2��nH2O��n��ֵ��
�ٳ�ȡ5.25g�������������ʣ����100mL��Һ��������Һ���õ�����������ƽ��__________��__________��__________�ͽ�ͷ�ιܡ������ƹ����ж��ݺ���ҡ�ȡ����ã�����Һ���½����ټ���������ˮ����������Һ��Ũ�Ƚ�__________������ƫ������������������ƫС������
����30.00mL 1mol��L-1����������Ba(OH)2��Һ��Ӧ�����ĸ�Ba(OH)2��Һ100.00mL�����ʲ����ᷴӦ�������Ba(OH)2��Һ�����ʵ���Ũ��Ϊ__________��
����ȡ5.25g����������ʧȥȫ���ᾧˮ�����ʲ��ֽ⣩���Ƶ�ʣ���������Ϊ3.09g����Ba(OH)2��nH2O��n=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ���к��е�CaSO4��������Na2CO3��Һ������ʹ֮ת��Ϊ���ɡ����������CaCO3��ij��ѧ��ȤС����ijŨ�ȵ�Na2CO3��Һ����һ������CaSO4���壬�������Na2CO3��Һ�������Һ��-lgc(CO32-)�Ĺ�ϵ���¡�
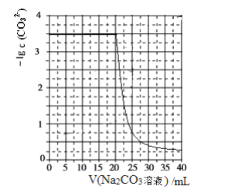
��֪Ksp(CaSO4)=9��10-6��Ksp(CaCO3)=3��10-9��lg3=0.5������˵������ȷ���ǣ� ��
A. �����ϸ������Һ�����ϵʽ��c(Ca2+)��c(SO42-)=Ksp(CaSO4)
B. CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq) K=3��103
CaCO3(s)+SO42-(aq) K=3��103
C. ��Na2CO3��Һ��Ũ��Ϊ1mol/L
D. ��ͬʵ�������£�����Na2CO3��Һ��Ũ�ȸ�ΪԭŨ�ȵ�2��������ͼ������������ƽ��1����λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к��ж�����Ⱦ������е������NOx����CO��SO2�ȣ������ཡ������������Ӱ�죬��ѧ�ڽ��������Ⱦ�з�������Ҫ���á�
��1��úȼ�ղ����������к��е����������CH4����ԭ������Ⱦ����д��CH4��NO2��Ӧ�Ļ�ѧ����ʽ_____________��
��2������β����CO��NO2������һ�������¿��Է�����Ӧ��
2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ��H=-746.8kJ��mol-1
N2(g)+2CO2(g) ��H=-746.8kJ��mol-1
4CO(g)+2NO2(g)![]() 3CO2(g)+N2(g) ��H=-1200kJ��mol-1
3CO2(g)+N2(g) ��H=-1200kJ��mol-1
��Ӧ��CO(g)+NO2(g)![]() CO2(g)+NO(g) ��H=_____kJ��mol-1
CO2(g)+NO(g) ��H=_____kJ��mol-1
��3���������������������ת��SO2(g)+NO2(g)![]() SO3(g)+NO(g)��ʵ����ƽ�ⳣ�� ���¶ȵĹ�ϵ����ͼ��ʾ���ش��������⣺
SO3(g)+NO(g)��ʵ����ƽ�ⳣ�� ���¶ȵĹ�ϵ����ͼ��ʾ���ش��������⣺

�ٸ÷�Ӧ����Ӧ�Ļ��___���������������������淴Ӧ�Ļ�ܡ�
�ڷ�Ӧ����v=V��-V��=k��xSO2��xNO2-k��xSO3��xNO��k����k���ֱ�Ϊ��������Ӧ���ʳ�����xΪ���ʵ���������T��ʱ��k��_____k������������������������=������
��T��ʱ�������Ϊ2L�������м���1molSO2(g)��1molNO2(g)��5minʱ���xSO3=0.2����ʱƽ����___����������������������Ӧ�����ƶ���![]() =___������2λС������
=___������2λС������
��4����֪��2NO(g)=N2(g)+O2(g) ��H=��180.6kJ/mol����ij��������������£�NO���Էֽ�����N2��O2���䷴Ӧ�����ɼ�Ϊ��
��һ����2NO ��N2O2 ��
�ڶ�����N2O2 ��N2+O2 ��
���б�����ȷ����____������)��
A�����л��Ϸ�Ӧ���Ƿ��ȷ�Ӧ
B��N2O2�Ǹ÷�Ӧ�ĵ��м����
C��������ʵĴ������Լ�С��Ӧ����H���ӿ췴Ӧ����
D����һ���Ļ�ܱȵڶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ǻ��۱���(SPPO)���ӽ���Ĥ��ȼ�ϵ�������й�����Ӧ��ǰ�����ϳɾ۱���(PPO)����������Ʊ�SPPO��·�����£�
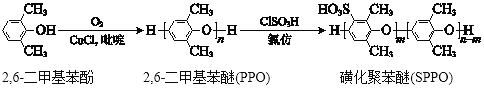
����˵������ȷ����
A. 2,6-�����������뱥����ˮ����ȡ����Ӧ
B. ������2,6-��������������ˮ
C. 2,6-����������O2����������Ӧ����PPO
D. PPO�ϳ�SPPO�ķ�Ӧ�ǣ�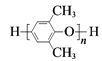 +mClSO3H
+mClSO3H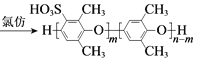 +mHCl
+mHCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��S16O2��18O2�ڸ��������·�����Ӧ2SO2+O2![]() 2SO3���ﵽ��ѧƽ�����ƽ�������к�18O����( )
2SO3���ﵽ��ѧƽ�����ƽ�������к�18O����( )
A. ֻ��SO3 B. ֻ��SO2��SO3 C. ��SO2��SO3��O2 D. ֻ��O2��SO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������ʱ���⻯Ǧ���ܶȻ�(Ksp)Ϊ7.1��10-9�����������µ⻯Ǧ������Һ��Pb2+��I-��Ũ��____________ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com