
分析 (1)由原子构成的晶体有原子晶体、稀有气体;
(2)一般非金属元素之间形成共价键,部分金属与非金属也能形成共价键;
(3)离子晶体和金属晶体中含有阳离子;离子晶体中阴阳离子构成;
(4)受热熔化需要克服共价键的物质为原子晶体;离子晶体和金属晶体在熔融时能导电.
解答 解:①水晶属于原子晶体,原子间通过共价键结合,熔融时不导电;
②干冰属于分子晶体,分子内存在共价键,熔融时不导电;
③氟化钠属于离子晶体由阴离子和阳离子构成,熔融时能电离出自由移动的离子,在熔融时能导电;
④固态氩属于单原子分子,分子内没有共价键,由原子直接构成,熔融时不导电;
⑤金属铝属于金属晶体,由金属阳离子和自由电子构成,在熔融时能导电;
⑥碳化硅属于原子晶体,原子间通过共价键结合,熔融时不导电;
⑦氢氧化钠是由氢氧根离子和钠离子构成的离子晶体,O与H之间形成共价键,在熔融时能导电;
⑧白磷属于分子晶体,分子内存在共价键,熔融时不导电;
(1)直接由原子构成的晶体是 ①④⑥;故答案为:①④⑥.
(2)含有共价键的晶体是 ①②⑥⑦⑧;故答案为:①②⑥⑦⑧.
(3)含有阳离子的晶体是 ③⑤⑦,含有阴离子的晶体是 ③⑦;故答案为:③⑤⑦;③⑦.
(4)熔化需克服共价键的晶体是 ①⑥,熔化能导电的晶体是 ③⑤⑦;故答案为:①⑥;③⑤⑦.
点评 本题考查化学键、晶体类型的判断等知识点,明确物质构成微粒是解本题关键,注意原子晶体熔化时需要克服共价键、分子晶体熔化时克服分子间作用力,注意二者的区别,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | NO与空气中的氧气反应生成NO2 | B. | 硝酸工厂用NH3氧化制NO | ||
| C. | N2与H2在一定条件下反应生成NH3 | D. | 由NH3制碳酸氢铵和硫酸铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 1 | 2 | 3 | 4 | 5 |
| 仪器及装置 |  |  |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋可除去热水壶内壁的水垢 | |
| B. | 75%(体积分数)的乙醇溶液常用于医疗消毒 | |
| C. | 35%-40%甲醛溶液俗称为福尔马林,可用来浸泡海产品来起到保鲜效果 | |
| D. | 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  Y表示原子半径 | B. |  Y表示元素的电负性 | ||
| C. | 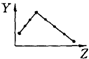 Y表示元素的最高正价 | D. |  Y表示元素的第一电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在放电时,该电池的负极材料是铅板 | |
| B. | 在充电时,铅蓄电池的负极与充电器电源的负极相连 | |
| C. | 在放电时,外电路中电流流向为:正极→外电路→负极 | |
| D. | 在充电时,阳极发生的反应为:PbSO4+2e-═Pb+SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{H_{2}SO_{4}.SO_{3}(发烟硫酸)}$
$→_{△}^{H_{2}SO_{4}.SO_{3}(发烟硫酸)}$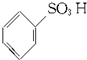
 $\stackrel{Fe,HCl,H_{2}O}{→}$
$\stackrel{Fe,HCl,H_{2}O}{→}$
 $\stackrel{NaClO}{→}$
$\stackrel{NaClO}{→}$

 C
C D
D .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com