
【题目】乙酸乙酯是无色透明有香味的液体,制备的实验装置如图所示。下列说法不正确的是( )
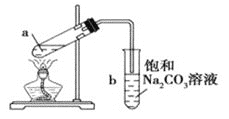
A.先在试管a中加入乙醇,然后边振荡试管边缓慢加入浓硫酸,待冷却后加入乙酸
B.浓硫酸的作用主要是催化剂和吸水剂
C.b中的饱和Na2CO3溶液可用浓NaOH溶液代替
D.试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、E的焰色反应均为黄色,其中B常用作食品的膨化剂,A与B按物质的量之比为1∶1混合并溶于足量水中,得到的溶液中只含有一种溶质。X为一种黑色固体单质,有多种同素异形体,其氧化物参与大气循环,为温室气体。G为冶炼铁的原料,G溶于盐酸中得到两种化合物,A~H之间有如下的转化关系(部分物质未写出):

(1)写出下列物质的化学式:A________;F________。
(2)B和C反应得到标准状况下的11.2 L D,则产生D的反应中,转移电子的物质的量为________ mol。
(3)写出A+B→E的离子方程式:_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把含有某一氯化物杂质的氯化钙5.55克溶于水后,与足量的硝酸银溶液反应,生成的氯化银沉淀15克,则该杂质可能是
A.氯化钠B.氯化钾
C.氯化铜D.氯化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素组成的单质X2、Y,标准状况下X2的密度为3.17gL-1,常温下,Y为浅黄色固体。Z是一种化合物,焰色反应呈浅紫色![]() 透过钴玻璃
透过钴玻璃![]() ;0.1molL-1Z的水溶液pH=13。X2、Y和Z之间有如下转化关系
;0.1molL-1Z的水溶液pH=13。X2、Y和Z之间有如下转化关系![]() 其他无关物质已略去
其他无关物质已略去![]() :
:
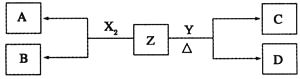
(1)写出单质X2与Z反应的离子方程式:______________________________________。
(2)已知16g单质Y完全燃烧放出148kJ热量。写出热化学方程式:________________。
(3)已知C能与较浓盐酸反应生成能使品红溶液褪色的气体
①D的化学式是:_________;D的水溶液pH>7,原因是![]() 用离子方程式表示
用离子方程式表示![]() :_____________。
:_____________。
②0.1molL-1的D溶液中各离子浓度由大到小的顺序为_______________________。
③将20mL0.5molL-1溶液逐滴加入到20mL0.2molL-1 KMnO4溶液![]() 硫酸酸化
硫酸酸化![]() 中,溶液恰好褪为无色。写出反应的离子方程式:_________________________________。
中,溶液恰好褪为无色。写出反应的离子方程式:_________________________________。
(4)①石墨和铁做电极,用隔膜电解槽电解A的溶液,阳极可产生X2。则铁做_________极。
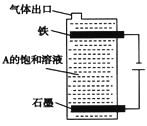
②按下图电解A的饱和溶液,写出该电解池中较长时间内发生反应的总反应方程式: ________。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2与O2发生反应的过程用模型图示如下(“﹣”表示化学键):下列说法不正确的是: ( )
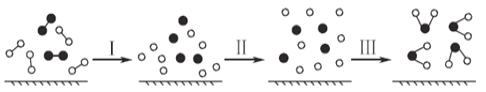
A.过程Ⅰ是吸热过程B.该反应的能量转化形式只能以热能的形式进行
C.过程Ⅲ一定是放热过程D.该反应过程所有旧化学键都断裂,且形成了新化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学配置450毫升 1mol/L的硫酸溶液
(1)应该选择________的容量瓶 A 250毫升 B 500毫升 C 1000毫升
(2)需要量取98%,ρ=1.84g/cm3浓硫酸__________毫升
(3)将所取浓硫酸逐滴加入盛有水的烧杯中,边加边搅拌
(4)将该溶液注入容量瓶
(5)在容量瓶中加水至___________处,改用__________加水至_______与刻度线相切
(6)塞好瓶塞,反复摇匀
(7)摇匀后发现,溶液体积缩小,继续加水至刻度线
(8)该同学的操作是否有不当之处,请指出(不必全部填满)
a__________________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
b____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
c_______________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
d____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S(常温下,氢硫酸的Ka1=5.7×10-8,Ka2=1.2×10-15)广泛存在于天然气、合成氨原料气、炼厂气等,生产中需脱硫处理。回答下列问题
(1)著名的 Vanviel反应为2nH2S+nCO2![]() (CH2O)n+nH2O+2nS↓,该反应能量转化形式是________。
(CH2O)n+nH2O+2nS↓,该反应能量转化形式是________。
(2)脱除天然气中H2S的工艺流程如下
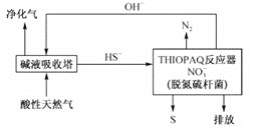
①常温下,“碱液吸收塔”中反应HS-+OH- ![]() S2-+H2O的平衡常数K=________。
S2-+H2O的平衡常数K=________。
②“ THIOPAO”反应器中,在脱氮硫杆菌的作用下,HS-氧化为S的离子方程式为________。
(3)铜(Ⅱ)沉淀及铜(Ⅱ)湿式氧化脱除硫化氢并可回收硫磺,主要步骤如下
(a)吸收H2S
(b)生成CuS沉淀
(c)CuCl2氧化CuS生成单质S和CuCl2-
(d)通O2再生
①常温下,沉淀反应之一:HS-+Cu2+![]() CuS+H+的平衡常数K= ________(已知常温下,KSP(CuS)=4×10-35)。
CuS+H+的平衡常数K= ________(已知常温下,KSP(CuS)=4×10-35)。
②CuCl2氧化CuS的离子方程式为 ________。
③通O2再生时的离子方程式为________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是
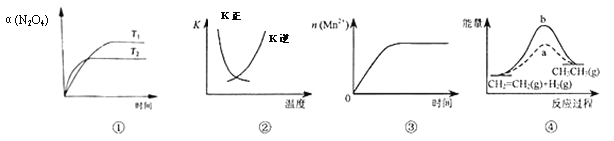
A. 图①表示N2O4(g)![]() 2NO2(g) ΔH>0,N2O4转化率随温度、时间的变化
2NO2(g) ΔH>0,N2O4转化率随温度、时间的变化
B. 图②中曲线表示反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH<0,正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)![]() CH3CH3(g) ΔH<0,使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g) ΔH<0,使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)维生素C的结构简式是___,它的分子式是____。由于它能防治坏血病,又称为____。在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有____性;在维生素C溶液中滴入少量酸性KMnO4溶液,可观察到的现象是____,说明维生素C具有____性。
(2)室内空气污染物包括CO、CO2、HCHO(甲醛)、C6H6(苯)等,在这四种污染物中,由家用燃料燃烧产生的是____;由建筑和装修产生的是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com