
【题目】2019年10月27日,国际清洁能源会议(ICCE2019)在北京开幕,一碳化学成为这次会议的重要议程。甲醇、甲醛(HCHO)等一碳化合物在化工、医药、能源等方面都有广泛的应用。
(1)甲醇脱氢法可制备甲醛(反应体系中各物质均为气态),反应生成1mol HCHO过程中能量变化如图:
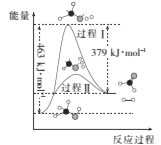
已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) H=-49.5kJ/mol
则反应CO2(g)+2H2(g)=HCHO(g)+H2O(g) H=______kJ/mol
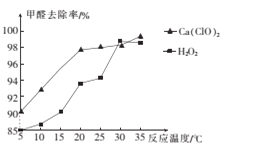
(2)氧化剂可处理甲醛污染,结合图象分析春季(水温约为15℃)应急处理被甲醛污染的水源应选择的试剂为____(填化学式)。
(3)纳米二氧化钛催化剂可用于工业上合成甲醇:CO(g)+2H2(g)CH3OH(g) H=akJ/mol
①按![]() =2投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图所示。则a ___(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是______。
=2投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图所示。则a ___(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是______。
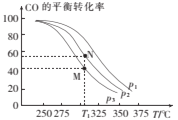
②在温度为T1℃,向某恒容密闭容器中充入H2和CO发生上述反应,起始时c(H2)=c(CO)=2.0mol/L。达到平衡时,CO的转化率为图中的M点对应的转化率,则在该温度下,对应的N点的平衡常数为______(保留3位有效数字)。
(4)工业上利用CH4(混有CO和H2)与水蒸气在一定条件下制取H2,该反应的逆反应速率表达式为v逆=kc(CO)c3(H2),k为速率常数,在某温度下测得实验数据如表所示:
CO浓度(mol/L) | H2浓度(mol/L) | 逆反应速率(mol·L-1·min-1) |
0.1 | c1 | 8.0 |
c2 | c1 | 16.0 |
c2 | 0.15 | 6.75 |
由上述数据可得该温度下,c2=_____,该反应的逆反应速率常数k=____L3mol-3min-l。
(5)用甲醇可以制备甲胺(CH3NH2),甲胺在水中的电离方程式与氨相似。25℃时,甲胺的电离常数Ka=9.25×10-7。该温度下,反应CH3NH2+H+![]() CH3NH3+的平衡常数K= ___(填数值)。
CH3NH3+的平衡常数K= ___(填数值)。
【答案】+34.5 Ca(ClO)2 < p3<p2<p1 4.17 0.2 1.0×104 9.25×107
【解析】
(1)由图可知1molCH3OH分解为1molHCHO和1molH2需要吸收能量463 kJ/mol -379 kJ/mol =84 kJ/mol,所以图示反应的热化学方程式为i:CH3OH(g)=HCHO(g)+H2(g) H=84 kJ/mol,又已知ii: CO2(g)+3H2(g)=CH3OH(g)+H2O(g) H=-49.5kJ/mol,由i+ii可得方程式CO2(g)+2H2(g)=HCHO(g)+H2O(g),根据盖斯定律可知该反应H=84 kJ·mol-1+(-49.5kJ/mol)=34.5 kJ/mol;
(2)分析图像可知,水温约为15℃时.选择Ca(ClO)2处理被甲醛污染的水源时,甲醛去除率更高;
(3)①据图可知相同压强下温度越高CO的平衡转化率越小,即温度升高平衡逆向移动,所以正反应为放热反应,所以H<0,即a<0;该反应正反应为气体体积减小的反应,所以相同温度下压强越大CO的平衡转化率越大,所以p3<p2<p1;
②平衡常数只与温度有关,温度不变则平衡常数不变,所以M点和N点平衡常数相等,M点CO的转化为40%,初始投料为2.0mol/L的H2和CO,则列三段式有:

该反应平衡常数![]() ;
;
(4)根据v逆=kc(CO)c3(H2),由表中数据可得:c13=![]() ,c2=
,c2= ,所以有
,所以有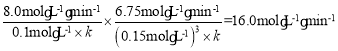 ,解得k=1.0×104L3·mol-3·min-3,带入c2的等式可得c2=0.2mol/L;
,解得k=1.0×104L3·mol-3·min-3,带入c2的等式可得c2=0.2mol/L;
(5)甲胺在水中的电离方程式与氨相似,所以其电离方程式为CH3NH2+H2O![]() CH3NH3++OH-,所以Ka=
CH3NH3++OH-,所以Ka=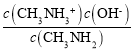 ,反应CH3NH2+H+
,反应CH3NH2+H+![]() CH3NH3+的平衡常数K=
CH3NH3+的平衡常数K=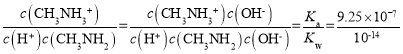 =9.25×107。
=9.25×107。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. CH2Cl2有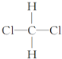 和
和 两种结构
两种结构
B. 分子式为C3H6和C5H10的物质一定互为同系物
C.  的一氯代物有5种
的一氯代物有5种
D. 1mol某烷烃完全燃绕消耗11molO2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以镍矿粉(主要成分为NiS,杂质FeS、CuS和SiO2等)为原料可制备NiCO3
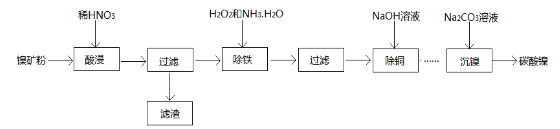
已知Ni和Fe为变价金属,常见化合价为+2价、+3价。
(1)在酸浸过程中,CuS与稀HNO3反应生成淡黄色固体,其离子方程式为___________________,滤渣的主要成分为________________________;
(2)在除FeS时,需加入过量的H2O2氧化,若用过强的氧化剂,其可能的后果是_______________;反应完全后,除去多余H2O2的简便方法是______________________;
(3)在“沉镍”工艺中,若将含Ni2+溶液缓慢加入至盛有Na2CO3溶液的反应容器中,可能会形成杂质,其原因是_______________________(用离子方程式表示)。检验碳酸镍沉淀完全的方法是__________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90。取有机物样品1.8 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。试求该有机物的分子式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1molL-1的H3PO2溶液和1molL-1的HBF4溶液,两者起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示。下列说法错误的是
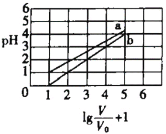
A.常温下,NaBF4溶液的pH=7
B.常温下,H3PO2的电离平衡常数约为1.1![]() 10-2
10-2
C.NaH2PO2 溶液中:c(Na+) =c( H2PO2- ) +c( HPO22-) +c(PO23-) +c( H3PO2)
D.常温下,在0≤pH≤4时,HBF4溶液满足![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2是一种白色或微黄色斜方晶体,易溶于水,微溶于乙醇。某校同学设计实验制备NaNO2并探究其性质。回答下列问题:
(1)甲组同学依据反应Na2CO3+NO+NO2=2NaNO2+CO2,并利用下列装置制备少量含NaNO2的溶液。(E中氧气稍过量)
A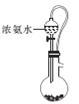 B
B![]() C
C![]() D
D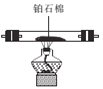 E
E![]() F
F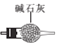
①正确的连接顺序:A—F—E— ___— ___—___ —尾气处理。(填字母)
②装置A的烧瓶中盛放的物质是____(填名称),C装置的作用是 ___。
(2)乙组同学依据反应Pb+NaNO3![]() NaNO2+PbO(难溶于水),并按下列实验流程制备NaNO2:
NaNO2+PbO(难溶于水),并按下列实验流程制备NaNO2:
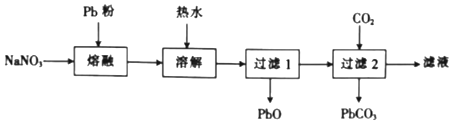
①“熔融”时用Pb粉代替铅粒的目的是____。
②由“过滤2”的滤液得到NaNO2晶体还需经过的具体操作为____、____、过滤、用乙醇洗涤后干燥。
(3)丙组同学探究NaNO2的性质,取少量乙组制得的NaNO2溶于水制得NaNO2溶液。
①取少量NaNO2溶液于试管中,滴入盐酸酸化,再加入KI和淀粉溶液,振荡,溶液变蓝,说明NaNO2具有____(填“氧化性”或“还原性”)。
②向酸性KMnO4溶液中滴入NaNO2溶液,溶液紫色逐渐褪去,发生反应的离子方程式为____(MnO4-被还原为Mn2+)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是

A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2=6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医药阿斯匹林的结构简式如图。试回答:
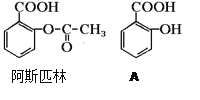
(1)阿斯匹林可看成酯类物质,口服后在胃肠作用下,阿斯匹林发生水解反应,生成A和B两种产物。其中A的结构简式如图,则阿斯匹林的分子式为:______________B的结构简式为:_______B中的官能团是:______________(名称)
⑵上述水解产物B与甲醇、浓硫酸共热反应的化学方程式为:_____________________________________________________
⑶ 甲醇在铜作催化剂时与氧气反应的化学方程式为:______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】克矽平是一种治疗矽肺病的药物,其合成路线如下(反应均在一定条件下进行):
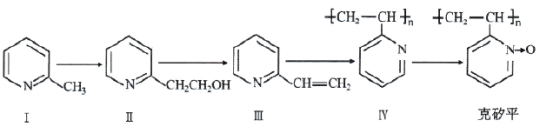
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以一定条件下与氢气发生反应生成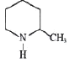 :该反应类型为______。
:该反应类型为______。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率 100%的反应,则所需另一种反应物的分子式为_____。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是_____(填字母)。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅱ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(__________)
A.乙烷 B.乙烯 C.乙醇 D.苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com