
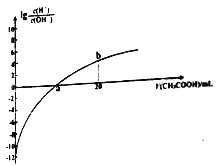
【题目】25℃时,Ka(CH3COOH)=1.7×10-5。该温度下,用0.1mol/L的醋酸溶液滴定10.00mL 0.1mol/L的MOH溶液,滴定过程中加入醋酸溶液的体积(V)与溶液中lg[c(H+)/c(OH-)]的关系如图所示(V=0时,lg[c(H+)c(OH-)]=-12)。下列说法不正确的是
A. MOH是一元强碱
B. a 点:V(CH3COOH)=10.00mL
C. b R:c(M+)>(CH3COOH)>C(H+)>c(OH-)
D. 25℃时,CH3COO-的水解平衡常数约为5.9×10-10
【答案】B
【解析】
A、由图可知,未加醋酸时,lgc(H+)/c(OH-)=-12,可知c(MOH)=0.1mol·L-1,溶液中c(OH-)=0.1mol·L-1;
B、a点lgc(H+)/c(OH-)=0,溶液为中性;
C、b点溶液中含等量的CH3COOH、CH3COOM,由lgc(H+)/c(OH-)>0可知溶液显酸性;
D、结合Kh=Kw/Ka计算。
A、由图可知,开始时lgc(H+)/c(OH-)=-12,且c(MOH)=0.1mol·L-1,溶液中c(OH-)=0.1mol·L-1,则MOH为强碱,故A正确;
B、a 点对应的lgc(H+)/c(OH-)=0,即c(H+)=c(OH-),溶液呈中性,由于醋酸是弱酸,当与一元强碱等体积等浓度反应时溶液呈弱碱性,所以当溶液呈中性时,醋酸溶液的体积大于10.00 mL,故B错误;
C、b点的溶液中,溶质为等物质的量浓度的醋酸CH3COOH和醋酸盐CH3COOM,由于醋酸电离程度很小,所以溶液中c(H+)<c(M+),正确的关系为c(CH3COO-)>c(M+)>(CH3COOH)>c(H+)>c(OH-),故C正确;
D、25℃时,Ka(CH3COOH)=1.7×10-5,Kw=1.0×10-14,所以CH3COO-的水解平衡常数Kh=1.0×10-14/1.7×10-5=(10/17)×10-9=5.9×10-10,故D正确;
故选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列实验基本操作或实验注意事项中,主要是基于实验安全考虑的是
A. 可燃性气体的验纯 B. 滴管不能交叉使用
C. 容量瓶在使用前进行检漏 D. 实验剩余的药品不能放回原试剂瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) + O2(g) ![]() 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
甲 | 乙 | 丙 | ||
起始物质的量 | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
n(O2) / mol | 0.24 | 0.24 | 0.48 | |
SO2的平衡转化率 / % | 80 | α1 | α2 | |
A. 甲中反应的平衡常数小于乙
B. 平衡时,丙中c(SO3)是甲中的2倍
C. 该温度下,平衡常数值为400
D. 平衡时,甲中O2的转化率大于乙中O2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25C时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n随时间1的变化如图1所示,已知反应达到平衡后,降低温度,A的转化率将增大。

(1)根据图1数据。写出该反应的化学方程式:_____________;此反应的平衡常数表达式为K=_________,从反应开始到第一次平衡时的平均速率v(A)为________。
(2)在5~7min内,若K值不变,则此处曲线变化的原因是_________。
(3)图2表示此反应的反应速率v和时间t的关系,t3、t5、t6时刻各改变一个且互不相同的条件,各阶段的平衡常数如下表所示。K1、K2、K3、K4之间的关系为________(用“>”“<”或“=”连接)。A的转化率最大的一段时间是___________。
t2~t3 | t4~t5 | t5~t6 | t7~t8 |
K1 | K2 | K3 | K4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度的升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H___0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为___molL﹣1s﹣1。

(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020molL﹣1s﹣1的平均速率降低,经10s又达到平衡。T___100℃(填“大于”或“小于”),判断理由是_______________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___(填“正反应”或“逆反应”)方向移动。
(4)在2NO2N2O4的可逆反应中,下列状态一定属于平衡状态的是(____)
A.N2O4和NO2的分子数比为1:2 B.N2O4和NO2的浓度相等
C.平衡体系的颜色一定不再改变D.单位时间有1molN2O4变为NO2的同时,有2molNO2变为N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超导材料为具有零电阻及磁性的物质,以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Ox。现欲合成0.5 mol此高温超导物,依化学计量数比例需取Y2O3、BaCO3和CuO的物质的量分别为( )
A. 0.50 mol、0.50 mol、0.50 mol B. 0.25 mol、1.0 mol、1.5 mol
C. 0.50 mol、1.0 mol、1.5 mol D. 1.0 mol、0.25 mol、0.17 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲被誉为“现代工业、国防与尖端技术的维生素”,工业上常用铜阳极泥(主要成分是Cu2Te,含Ag、Au等杂质)为原料提取碲并回收金属其工艺流程如下:
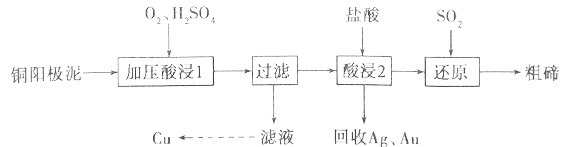
已知:TeO2是两性氧化物,微溶于水,易溶于较浓的强酸和强碱。回答下列问题:
(1)“加压酸浸1”过程中将碲元素转化成TeO2,应控制溶液的pH为4.5~5.0,酸度不能过高,原因是__________________________,其中“加压”的目的是______________________。写出“加压酸浸1”过程中Cu2Te发生反应的化学方程式_________________________________。
(2)“酸浸2”时温度过高会使碲的浸出率降低,原因为______________________。要从Ag和Au中分离出Au,可以向回收的Ag和Au中加入的试剂是______________________。
(3)写出“还原”反应中发生的离子方程式_________________________________。
(4)工业上另一种提取碲的方法是将铜阳极泥在空气中焙烧,使碲转化成TeO2,再加NaOH碱浸,以石墨为电极电解溶液获得Te。电解过程中阴极的电极反应式为_________________________________。
(5)25℃时,向1mol/L的Na2TeO3溶液中滴加盐酸,当溶液pH值约为6时,此时溶液中c(TeO32-):c(HTeO3-)=___________(已知:H2TeO3的Ka1=1.0×10-3,Ka2=2.0×10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L恒容密闭容器中投入一定量的A、B发生反应:3A(g)+bB(g)![]() cC(g) H=-QkJ·mol-1(Q>0),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是
cC(g) H=-QkJ·mol-1(Q>0),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是
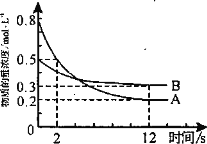
A. 2s时,A的反应速率为0.15mol·L-1·s-1
B. 图中交点时A的消耗速率等于A的生成速率
C. 化学计量数之比b ∶c = 1∶2
D. 12s内反应放出0.2QkJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于含氮化合物的性质叙述正确的是( )
A.可用铁制容器储存稀硝酸
B.实验室用排空气集气法收集NO气体
C.实验室可用氨水与硫酸铝溶液反应制取氢氧化铝
D.NO2与水发生化合反应生成硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com