
| A、用铁粉代替铁片 |
| B、提高反应温度 |
| C、用浓硫酸代替稀硫酸 |
| D、去除铁表面的铁锈 |
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
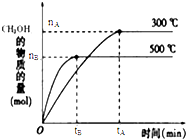 一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.
一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(OH-) |
| c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、Na+、Br-、SO42- |
| B、Fe2+、Al3+、ClO-、Cl- |
| C、Al3+、[A1(OH)4]-、Na+、Cl- |
| D、Mg2+、H+、SiO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电负性的大小顺序为Cl>S>P |
| B、由于NO3-和SO3互为等电子体,所以可以推断NO3-的空间构型为平面三角形 |
| C、根据晶格能的大小可以判断MgCl2的熔点比CaCl2高 |
| D、液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn+2HCl=H2↑+ZnCl2 | ||||
| B、CaCO3+2HCl=CO2↑+CaCl2+H2O | ||||
C、MnO2+4HCl(浓)
| ||||
| D、HCl+KOH=KCl+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com