
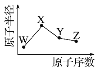
【题目】W、X、Y、Z是四种短周期主族元素,其原子半径随原子序数的变化如图。已知W是地壳中含量最高的元素;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是
A. 对应的简单离子的半径:X<W
B. 对应的简单气态氢化物的稳定性:Y>Z
C. 元素X、Z分别与W能形成多种化合物
D. Z的最高价氧化物对应的水化物具有强酸性
【答案】B
【解析】
W、X、Y、Z是四种常见的短周期元素,已知W是地壳中含量最高的元素,故W为O元素;X和Ne原子的核外电子数相差1,X为Na或F,X原子半径大于O原子,故X为Na元素;Y的单质是一种常见的半导体材料,原子序数大于Na元素,故Y为Si元素;Z的非金属性在同周期元素中最强,故Z为Cl元素,结合元素周期律分析解答。
根据上述分析,W为O元素,X为Na元素,Y为Si元素,Z为Cl元素。
A.W为O元素,X为Na元素,电子层结构相同的离子,核电荷数越大,离子半径越小,故离子半径O2->Na+,故A正确;
B.Y为Si元素,Z为Cl元素,非金属性Cl>Si,故氢化物稳定性Y(Si)<Z(Cl),故B错误;
C.X为Na元素,Z为Cl元素,W为O元素,能够形成的化合物分别有氧化钠、过氧化钠,二氧化氯,七氧化二氯等,故C正确;
D.氯的最高价氧化物对应的水化物为高氯酸,是强酸,故D正确;
答案选B。


科目:高中化学 来源: 题型:
【题目】(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_____。

(2)合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量,已知(见图):则1mol N﹣H键断裂吸收的能量约等于_____kJ。

(3)请将 Zn+2Ag+=2Ag+Zn2+设计成原电池,并画出简易装置图,并注明电极材料以及电解质溶液___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A. 1s电子云界面图是一个球面,表示在这个球面以内,电子出现的概率为![]()
B. 在能层、能级、以及电子云的伸展方向确定时,电子的运动状态才能确定下来
C. 在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析
D. 原子核外的电子就像行星围绕太阳一样绕着原子核做圆周运动
查看答案和解析>>
科目:高中化学 来源: 题型:
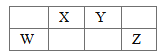
【题目】X、Y、W、Z为四种短周期主族元素,在周期表中的位置如图所示,W原子的最外层电子数与电子层数相同,下列说法正确的是
A. X是形成化合物种类最多的元素
B. W、X、Y的原子半径依次增大
C. W的最高价氧化物对应的水化物可溶于X的最高价氧化物对应的水化物的溶液
D. X的最简单气态氢化物的稳定性强于Y的最简单氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉淀法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为____________。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反应的离子方程式为_____________________。
(2)电镀厂的废水中含有的CN-有剧毒,需要处理加以排放。处理含CN-废水的方法之一是在微生物的作用下,CN-被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为_____________。
(3)电渗析法处理厨房垃极发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子):
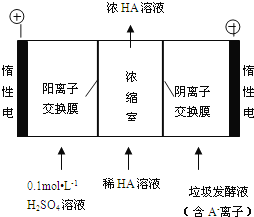
①阳极的电极反应式为________________________。
②简述浓缩室中得到浓乳酸的原理:________________________。
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8,此时进入浓缩室的OH-可忽略不计。400 mL 10 g/L 乳酸溶液通电一段时间后,浓度上升为145 g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为________L(提示:乳酸的摩尔质量为90 g/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知:氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。活泼金属硫化物与酸反应产生H2S气体。
Ⅰ、制备氢化锂:选择下图中的装置制备氢化锂(有些装置可重复使用):
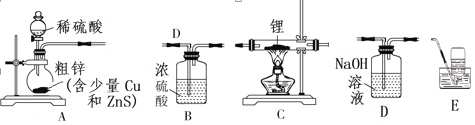
(1)装置的连接顺序(从左至右)为A→___________________________________。
(2)检查好装置的气密性,打开装置A中分液漏斗的活塞后,点燃酒精灯前需进行的实验操作是________。
Ⅱ、制备氢化铝锂
1947年,Schlesinger、Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅拌,充分反应后,经一系列操作得到LiAlH4晶体。
(3)写出氢化锂与无水三氯化铝反应的化学方程式_________________________。
Ⅲ.测定氢化铝锂产品(不含氢化锂)的纯度
(4)按下图连接好装置后,检查装置气密性的操作是:_____________________。装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是__________________。
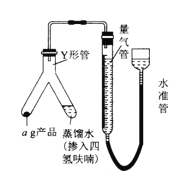
(5)在标准状况下,反应前量气管(由碱式滴定管改装而成)读数为V1 mL,反应完毕并冷却之后,量气管读数为V2 mL。该样品的纯度为_________(用含a、V1、V2的代数式表示)。如果起始读数时俯视刻度线,测得的结果将_________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化加氢可生成 3-甲基己烷的是( )
A.CH2=CHCH(CH3)CH2CH2CH3
B.CH2=C(CH3)CH2CH2CH2CH3
C.CH3C(CH2CH3)=CHCH3
D.CH3CH2CH2C(CH3)=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:(A、B均为气体)
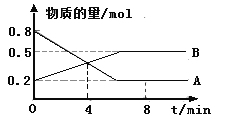
①该反应的化学方程式为____________________;
②反应开始至4 min时,B的平均反应速率为________ ;
③4 min时,反应是否达到平衡状态?________(填“是”或“否”),8 min时,v(正)________v(逆)(填“>”、“<”或“=”)。
(2)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
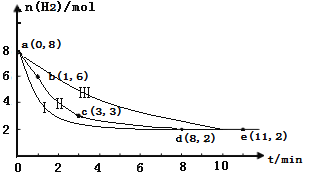
①a—b,b—c,c—d,d—e四段中,平均反应速率最大的时间段是___________ ,该时间段内CO2的平均反应速率是________。
②若在反应中加入了催化剂,则反应过程将变为图中的曲线_____ (填“Ⅰ”或“Ⅱ”或“Ⅲ”)。
③平衡时CO2的转化率是_________;反应前后容器内的压强比是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com