
【题目】氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知:氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。活泼金属硫化物与酸反应产生H2S气体。
Ⅰ、制备氢化锂:选择下图中的装置制备氢化锂(有些装置可重复使用):
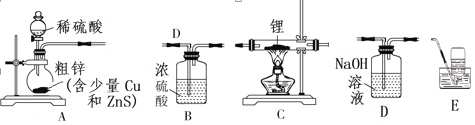
(1)装置的连接顺序(从左至右)为A→___________________________________。
(2)检查好装置的气密性,打开装置A中分液漏斗的活塞后,点燃酒精灯前需进行的实验操作是________。
Ⅱ、制备氢化铝锂
1947年,Schlesinger、Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅拌,充分反应后,经一系列操作得到LiAlH4晶体。
(3)写出氢化锂与无水三氯化铝反应的化学方程式_________________________。
Ⅲ.测定氢化铝锂产品(不含氢化锂)的纯度
(4)按下图连接好装置后,检查装置气密性的操作是:_____________________。装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是__________________。
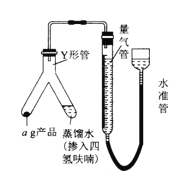
(5)在标准状况下,反应前量气管(由碱式滴定管改装而成)读数为V1 mL,反应完毕并冷却之后,量气管读数为V2 mL。该样品的纯度为_________(用含a、V1、V2的代数式表示)。如果起始读数时俯视刻度线,测得的结果将_________(填“偏高”“偏低”或“无影响”)。
【答案】D→B→C→B→E 用小试管在装置E的水槽中收集气体并验纯 4LiH+AlCl3═LiAlH4+3LiCl 向量气管中加水至左右出现液面差,静置,若液面差保持稳定,则装置气密性良好 倾斜Y形管,将蒸馏水(掺入四氢呋喃)全部注入a g产品中 19(V2-V1)/448a% 偏高
【解析】
Ⅰ.(1)氢化锂遇水能够剧烈反应,因此生成的氢气需要干燥,并除去其中混有的H2S,因此需要先通过氢氧化钠溶液除去硫化氢气体,再通过浓硫酸干燥,然后在C装置中发生反应生成氢化锂,为防止外界水蒸气进入装置,后面需要接干燥装置B,最后用排水集气法收集未反应的氢气,装置的连接顺序(从左至右)为A→D→B→C→B→E;综上所述,本题答案是:D→B→C→B→E。
(2)检查好装置的气密性,点燃酒精灯前需要首先制备氢气,并检验氢气的纯度,因此进行的实验操作为:打开装置A中分液漏斗的活塞,一段时间后,用小试管在装置E的水槽中收集气体并验纯;综上所述,本题答案是:用小试管在装置E的水槽中收集气体并验纯。
Ⅱ.(3)氢化锂与无水三氯化铝按一定比例在乙醚中混合,充分反应得到LiAlH4,反应的化学方程式为:4LiH+AlCl3═LiAlH4+3LiCl;综上所述,本题答案是:4LiH+AlCl3═LiAlH4+3LiCl。
Ⅲ.(4) 按图2装配仪器,向量气管中加水至左右出现液面差,静置,若液面差保持稳定,则装置气密性良好;检查好装置气密性并装好药品,Y形管中的蒸馏水足量,启动反应时只需要倾斜Y形管,将蒸馏水(掺入四氢呋喃)全部注入ag产品中即可;综上所述,本题答案是:向量气管中加水至左右出现液面差,静置,若液面差保持稳定,则装置气密性良好;倾斜Y形管,将蒸馏水(掺入四氢呋喃)全部注入a g产品中。
(5) 氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体为氢气,LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑,在标准状况下,反应前量气管读数为V1mL,反应完毕并冷却之后,量气管读数为V2mL,则生成的氢气为(V2- V1) mL,根据方程式,LiAlH4的物质的量为(V2- V1)×10-3/(4×22.4)mol,则样品的纯度为:[38×(V2- V1)×10-3/(4×22.4)]/a×100%=![]() ;如果起始读数时俯视刻度线,导致V1偏小,结果偏高;综上所述,本题答案是:.
;如果起始读数时俯视刻度线,导致V1偏小,结果偏高;综上所述,本题答案是:. ![]() ;偏高。
;偏高。


科目:高中化学 来源: 题型:
【题目】某晶体中含有极性共价键,关于该晶体说法错误的是( )
A.不可能是离子晶体
B.不可能是单质分子构成的晶体
C.可能是分子晶体
D.可能具有较高的熔沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是最宝贵的资源之一。下列表述正确的是( )
A.40℃时,纯水的pH=7
B.温度升高,纯水中的c(H+)增大,c(OH-)减小
C.水的电离程度很小,纯水中主要存在形态是水分子
D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种短周期主族元素,其原子半径随原子序数的变化如图。已知W是地壳中含量最高的元素;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是
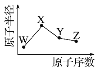
A. 对应的简单离子的半径:X<W
B. 对应的简单气态氢化物的稳定性:Y>Z
C. 元素X、Z分别与W能形成多种化合物
D. Z的最高价氧化物对应的水化物具有强酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下:

(1)A的分子式是C7H8,其结构简式是________________________。
(2)试剂a是____________________。
(3)反应③的化学方程式:_________________________________________________。
(4)E的分子式是C6H10O2。E中含有的官能团:_________________________。
(5)反应④的反应类型是____________________________。
(6)反应⑤的化学方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是![]()
![]()
![]() 杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
![]() 同一周期从左到右,元素的第一电离能、电负性都是越来越大
同一周期从左到右,元素的第一电离能、电负性都是越来越大
![]() 分子中键能越大,表示分子拥有的能量越高
分子中键能越大,表示分子拥有的能量越高
![]() 所有的配合物都存在配位键
所有的配合物都存在配位键
![]() 所有含极性键的分子都是极性分子
所有含极性键的分子都是极性分子
![]() 熔融状态下能导电的化合物一定是离子化合物
熔融状态下能导电的化合物一定是离子化合物
![]() 所有的原子晶体都不导电
所有的原子晶体都不导电
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关乙烯分子中的化学键描述正确的是
A. 碳原子的三个sp2杂化轨道与其它原子形成三个σ键
B. 每个碳原子的未参加杂化的2p轨道形成σ键
C. 每个碳原子的sp2杂化轨道中的其中一个形成π键
D. 碳原子的未参加杂化的2p轨道与其它原子形成σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种酸性“二甲醚(CH3OCH3)直接燃料电池”具有启动快、能量密度高、效率好等优点,其电池原理如图所示。下列有关该电池的说法不正确的是
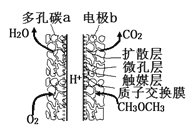
A. 多孔碳a能增大气固接触面积,提高反应速率,该电极为负极
B. 电极b上发生的反应为:CH3OCH3-12e-+3H2O=2CO2+12H+
C. H+由b电极向a电极迁移
D. 二甲醚直接燃料电池能量密度( kW·h·kg-1)约为甲醇(CH3OH)直接燃料电池能量密度的1.4倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习中常用类推方法,下列类推正确的是![]()
![]()
A. ![]() 为直线形分子,
为直线形分子,![]() 也为直线形分子
也为直线形分子
B. 固态![]() 是分子晶体,固态
是分子晶体,固态![]() 也是分子晶体
也是分子晶体
C. ![]() 中N原子是
中N原子是![]() 杂化,
杂化,![]() 中B原子也是
中B原子也是![]() 杂化
杂化
D. ![]() 能溶于NaOH溶液,
能溶于NaOH溶液,![]() 也能溶于NaOH溶液
也能溶于NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com