
【题目】化学学习中常用类推方法,下列类推正确的是![]()
![]()
A. ![]() 为直线形分子,
为直线形分子,![]() 也为直线形分子
也为直线形分子
B. 固态![]() 是分子晶体,固态
是分子晶体,固态![]() 也是分子晶体
也是分子晶体
C. ![]() 中N原子是
中N原子是![]() 杂化,
杂化,![]() 中B原子也是
中B原子也是![]() 杂化
杂化
D. ![]() 能溶于NaOH溶液,
能溶于NaOH溶液,![]() 也能溶于NaOH溶液
也能溶于NaOH溶液
【答案】D
【解析】A项,SO2为V形分子;B项,SiO2属于原子晶体;C项,BCl3中B原子为sp2杂化;D项,Al(OH)3和Be(OH)2都属于两性氢氧化物,都能溶于NaOH溶液。
A项,CO2中中心原子C上的孤电子对数为![]() (4-2
(4-2![]() 2)=0,σ键电子对数为2,价层电子对数为0+2=2,VSEPR模型为直线形,由于C上没有孤电子对,CO2为直线形分子,SO2中中心原子S上的孤电子对数为
2)=0,σ键电子对数为2,价层电子对数为0+2=2,VSEPR模型为直线形,由于C上没有孤电子对,CO2为直线形分子,SO2中中心原子S上的孤电子对数为![]() (6-2
(6-2![]() 2)=1,σ键电子对数为2,价层电子对数为1+2=3,VSEPR模型为平面三角形,由于S上有一对孤电子对,SO2为V形分子,A项错误;B项,固体CS2是分子晶体,固体SiO2属于原子晶体,B项错误;C项,NCl3中中心原子N上的孤电子对数为
2)=1,σ键电子对数为2,价层电子对数为1+2=3,VSEPR模型为平面三角形,由于S上有一对孤电子对,SO2为V形分子,A项错误;B项,固体CS2是分子晶体,固体SiO2属于原子晶体,B项错误;C项,NCl3中中心原子N上的孤电子对数为![]() (5-3
(5-3![]() 1)=1,σ键电子对数为3,价层电子对数为1+3=4,NCl3中N为sp3杂化,BCl3中中心原子B上的孤电子对数为
1)=1,σ键电子对数为3,价层电子对数为1+3=4,NCl3中N为sp3杂化,BCl3中中心原子B上的孤电子对数为![]() (3-3
(3-3![]() 1)=0,σ键电子对数为3,价层电子对数为0+3=3,BCl3中B为sp2杂化,C项错误;D项,Be和Al在元素周期表中处于对角线,根据“对角线规则”,Be(OH)2与Al(OH)3性质相似,两者都属于两性氢氧化物,都能溶于NaOH溶液,Al(OH)3、Be(OH)2与NaOH溶液反应的化学方程式分别为Al(OH)3+NaOH=NaAlO2+2H2O、Be(OH)2+2NaOH=Na2BeO2+2H2O,D项正确;答案选D。
1)=0,σ键电子对数为3,价层电子对数为0+3=3,BCl3中B为sp2杂化,C项错误;D项,Be和Al在元素周期表中处于对角线,根据“对角线规则”,Be(OH)2与Al(OH)3性质相似,两者都属于两性氢氧化物,都能溶于NaOH溶液,Al(OH)3、Be(OH)2与NaOH溶液反应的化学方程式分别为Al(OH)3+NaOH=NaAlO2+2H2O、Be(OH)2+2NaOH=Na2BeO2+2H2O,D项正确;答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知:氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。活泼金属硫化物与酸反应产生H2S气体。
Ⅰ、制备氢化锂:选择下图中的装置制备氢化锂(有些装置可重复使用):
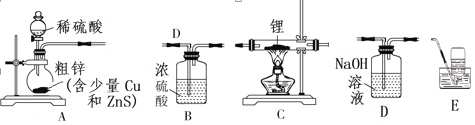
(1)装置的连接顺序(从左至右)为A→___________________________________。
(2)检查好装置的气密性,打开装置A中分液漏斗的活塞后,点燃酒精灯前需进行的实验操作是________。
Ⅱ、制备氢化铝锂
1947年,Schlesinger、Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅拌,充分反应后,经一系列操作得到LiAlH4晶体。
(3)写出氢化锂与无水三氯化铝反应的化学方程式_________________________。
Ⅲ.测定氢化铝锂产品(不含氢化锂)的纯度
(4)按下图连接好装置后,检查装置气密性的操作是:_____________________。装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是__________________。
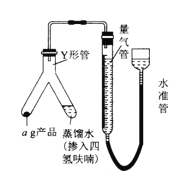
(5)在标准状况下,反应前量气管(由碱式滴定管改装而成)读数为V1 mL,反应完毕并冷却之后,量气管读数为V2 mL。该样品的纯度为_________(用含a、V1、V2的代数式表示)。如果起始读数时俯视刻度线,测得的结果将_________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如下图,下列说法正确的是( )

A. 脱硝的总反应为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
B. NH3催化还原NO为吸热反应
C. 过程1中NH3断裂非极性键
D. 过程中NO为氧化剂,Fe2+为还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:(A、B均为气体)
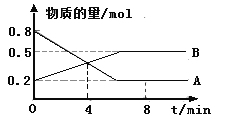
①该反应的化学方程式为____________________;
②反应开始至4 min时,B的平均反应速率为________ ;
③4 min时,反应是否达到平衡状态?________(填“是”或“否”),8 min时,v(正)________v(逆)(填“>”、“<”或“=”)。
(2)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
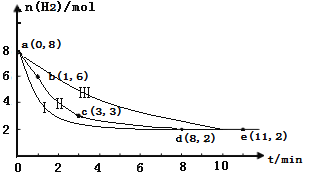
①a—b,b—c,c—d,d—e四段中,平均反应速率最大的时间段是___________ ,该时间段内CO2的平均反应速率是________。
②若在反应中加入了催化剂,则反应过程将变为图中的曲线_____ (填“Ⅰ”或“Ⅱ”或“Ⅲ”)。
③平衡时CO2的转化率是_________;反应前后容器内的压强比是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一混合溶液,只可能含有以下离子中的若干种:K+、![]() 、Cl-、Mg2+、Ba2+、
、Cl-、Mg2+、Ba2+、![]() 、
、![]() ,现取三份100 mL该溶液进行如下实验:
,现取三份100 mL该溶液进行如下实验:
(1)向第一份溶液中加入AgNO3溶液时有沉淀产生;
(2)向第二份溶液中加入足量NaOH溶液并加热后,收集到气体0.06 mol;
(3)向第三份溶液中加入足量BaCl2溶液后,所得沉淀经洗涤、干燥、称量为8.24 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,以下推测正确的是( )
A. K+可能存在 B. 100 mL溶液中含0.01 mol ![]()
C. Cl可能存在 D. Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知AgI胶体微粒能吸附I-。在10mL0.01mol·L-1KI溶液中,滴入8~10滴(1滴约0.1mL)0.01mol·L-1AgNO3溶液后,将溶液装入半透膜袋中并浸泡在蒸馏水里,过一段时间后,水中含有数目最多的离子是
A.K+B.K+、NO3-C.I-D.Ag+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
![]()
A. 气体摩尔体积就是![]()
B. 非标准状况下,1mol任何气体的体积不可能为![]()
C. 标准状况下![]() 任何物质都含有约
任何物质都含有约![]() 个分子
个分子
D. ![]() 和
和![]() 的混合气体在标准状况下的体积约
的混合气体在标准状况下的体积约![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com