
【题目】以NA代表阿伏加德罗常数,下列说法正确的是( )
A.常温常压下,32gO2含2NA个原子
B.标准状况下,11.2LH2O含有的原子数目为1.5NA
C.1mol的Cl﹣含有NA个电子
D.0.5mol/L的NaCl溶液中Cl﹣的个数为0.5 NA
科目:高中化学 来源: 题型:
【题目】下列说法不能用元素周期律解释的是( )
A.浓硫酸的氧化性强于稀硫酸
B.与冷水反应的速率:Na>Mg
C.向淀粉KI溶液中滴入氯水,溶液变蓝
D.原子半径:Al>Si>P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合物0.1mol完全燃烧得0.16mol二氧化碳和3.6克水.下列说法正确的是( )
A.一定有甲烷
B.一定是甲烷和乙烯
C.可能有乙烷
D.一定有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上从海水中提取溴的主要反应是:C12+2Br-=2Cl-+Br2 。下列说法错误的是
A. 海水中溴元素主要以形式Br-存在B. 上述反应属于离子反应
C. 该反应中氧化剂是Br-D. 上述反应属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是( ) 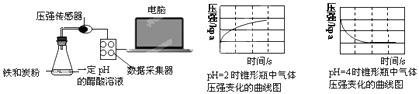
A.溶液pH≤2时,生铁发生析氢腐蚀
B.生铁的腐蚀中化学腐蚀比电化学腐蚀更普遍
C.在酸性溶液中生铁可能发生吸氧腐蚀
D.两溶液中负极反应均为:Fe﹣2e﹣═Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属A、B和气体甲、乙、丙及物质C、D、F、F,它们之间的转化发生如下反应,(图中有些反应的产物和反应条件没有全部标出),黄绿色气体溶于水后的溶液有漂白性且能杀菌消毒,其中物质F的水溶液呈黄色,物质E在氧化剂作用下很容易转化为物质F,F能与物质C的溶液反应生成红褐色沉淀.
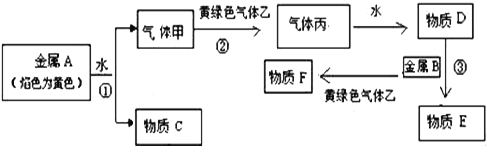
请回答下列问题:
(1)物质F的化学式为______.
(2)①写出金属A与水反应的化学方程式:______.
②写出黄绿色气体乙和水反应的离子化学方式:______.
③实验室制备黄绿色气体的化学方程式:___________.
(3)金属单质A投入到下列溶液中既有气体,又有沉淀出现的是______
A、氯化钠溶液 B、碳酸钠溶液 C、硫酸铜溶液 D、氯化铵溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨的热化学方程式为N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJ/mol.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分数为φ,下列说法中正确的是( ) 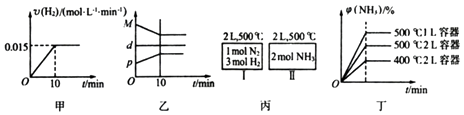
A.若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示
B.反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙
C.如图丙所示,容器I和II达到平衡时,NH3的体积分数为φ,则容器I放出热量与容器II吸收热量之和为92.4kJ
D.若起始加入物料为1 mol N2 , 3 mol H2 , 在不同条件下达到平衡时,NH3的体积分数变化如图丁所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:W、Y、Z、T、M为前四周期元素,且原子半径依次增大.请填空:
(1)W,Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图;
(2)化合物YW3极易溶于水的原因;YW3的分子构型为 . YW3属于(填“极性”或“非极性”)分子,其中Y的化合价为 .
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表周期族.T的化合物TY熔融时不导电,常用作砂轮及耐高温材料,由此推知,它属于(填编号字母);
a.离子晶体 b.原子晶体 c.分子晶体 d.无法判断
(4)M3+的3d轨道为半充满,则M的原子的电子排布式为 , M位于周期表的区(按电子的填入顺序划分),M的晶体中的粒子采用的是体心立方堆积,则该种堆积方式的配位数为 , 若其晶胞的边长为acm,M的摩尔质量为Mr g/mol,阿伏加德罗常数的值为NA , 则其密度为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com