
【题目】25℃时,醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+ H+,下列说法正确的是
CH3COO-+ H+,下列说法正确的是
A.向体系中加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降
B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小
C.加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D.升高体系温度(忽略醋酸挥发),溶液中H+数目增多,平衡一定向左移动
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】次磷酸钴[Co(H2PO2)2]广泛应用于化学电镀,工业上利用电渗析法制取次磷酸钴的原理图如图所示。
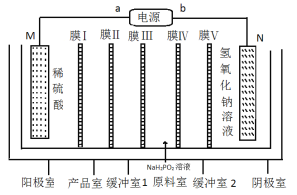
已知:①该装置的电极材料分别为金属钴和不锈钢。
②Co(H2PO2)2溶液在强碱性条件下通过自身催化发生氧化还原反应,实现化学镀钴。
下列说法中正确的是( )
A.膜Ⅱ、膜Ⅲ均为阴离子交换膜
B.M电极反应为Co-2e-+2H2PO2-=Co(H2PO2)2
C.a为电源的负极
D.Co(H2PO2)2溶液化学镀钴过程中反应可能为Co2++H2PO2-+3OH=Co+HPO3-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,X、Y、Z分别处于立方体的顶点、棱边的中点、立方体的体心。则下面关于该化合物的说法正确的是( )
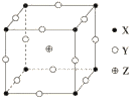
A. 该晶体的化学式为ZXY3
B. 该晶体的熔点一定比金属晶体熔点高
C. 每个X周围距离最近的Y有8个
D. 每个Z周围距离最近的X有16个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是盛放液溴的试剂瓶剖面图,仔细观察分成了明显的气相、溴溶液相和液溴相三相,下列说法错误的是( )

A.气相呈现红棕色,因为其中含有Br2的蒸汽
B.溴溶液相中显酸性,主要因为HBr电离出了H![]()
C.液溴保存时加水形成水封的目的是减少Br2的挥发
D.液溴保存时不可敞口放置,应保存在细口瓶中并塞上橡胶塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用有机含碘![]() 主要以I2和IO3-的形式存在
主要以I2和IO3-的形式存在![]() 废水制备单质碘的实验流程如下:
废水制备单质碘的实验流程如下:

已知:Ⅰ.碘的熔点为113℃,但固态的碘可以不经过熔化直接升华;
Ⅱ.粗碘中含有少量的硫酸钠杂质。
下列说法正确的是( )
A.操作②中发生反应的离子方程式为IO3-+3SO32-=I-+3SO42-
B.操作①和③中的有机相从分液漏斗上端倒出
C.操作④为过滤
D.操作⑤可用如图所示的水浴装置进行

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应Cu(s) + 2Ag+(aq)![]() Cu2+(aq) + 2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是 ( )
Cu2+(aq) + 2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是 ( )
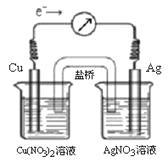
A. KNO3盐桥中的K+移向Cu(NO3)2溶液
B. 当电流计指针为0时,该反应达平衡,平衡常数K=0
C. 若此时向AgNO3溶液中加入NaCl固体,随着NaCl量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转
D. 若此时向Cu(NO3)2溶液中加入NaOH固体,随着NaOH量的增加电流计指针向右偏转幅度减小→指针指向0→向左偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法错误的是( )

A. 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
B. 电池工作时,外电路中流过 0.02 mol 电子,负极材料减重 0.14 g
C. 石墨烯的作用主要是提高电极a的导电性
D. 电池充电时间越长,电池中Li2S2的量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示。根据该表,回答下列问题:
化学式 | HF | CH3COOH | H2SO3 | H2CO3 | H2S |
电离平衡 常数(Ka) | 4.0×10-4 | 1.8×10-5 | K1=1.54×10-2 K2=1.02×10-7 | K1=4.4×10-7 K2=4.7×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
(1)同浓度的F-、CO32-、CH3COO-、HS-结合H+的能力最强的为__________
(2)溶液中不可能大量共存的离子组是__________
a.HS-、SO32- b.HF、CH3COO- c.HS-、HCO3- d. HSO3-、HCO3-
(3)Na2CO3溶液通入过量H2S的离子方程式是:_____。
(4)OH-浓度相同的等体积的两份溶液HCl(A)和 CH3COOH(E),分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_______(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
(5)向 0.l molL-1 CH3COOH溶液中滴加 NaOH 溶液至c(CH3COOH) : c(CH3COO-) =2 : 36,此时溶液pH = __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g) + nB(g)![]() pC(g) H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g) H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
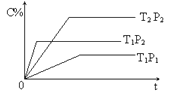
A. T1<T2 P1>P2 m+n<P Q<0B. T1>T2 P1<P2 m+n>P Q>0
C. T1<T2 P1<P2 m+n<P Q>0D. T1>T2 P1<P2 m+n>P Q<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com