
����Ŀ��������ʵĵ���ƽ�⡢�����ˮ��ƽ������������Һƽ������ڻ�ѧƽ�⡣
(1)��֪H2A��ˮ�д�������ƽ�⣺H2A=H++HA-��HA-![]() H++A2-��
H++A2-��
��NaHA��Һ��pH_____Na2A��Һ��pH(����ڡ�С�ڻ����)��
��ij�¶��£�����0.1mol/L��NaHA��Һ����εμ�0.1mol/L��KOH��Һ����Һ�����ԡ���ʱ�û����Һ�����й�ϵ�У�һ����ȷ���� _____________��
A.c(H+).c(OH-)=1��10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-) C.c(Na+)��c(K+) D.c(Na+)+c(K+)=0.05mol/L
(2)�����£�����0.1mol/L����ͭ��Һ�м�����������ϡ��Һ��ֽ��裬��dz��ɫ������ͭ�������ɣ�����Һ��pH=8ʱ��c(Cu2+)=_________ (Ksp[Cu(OH)2]=2.2��10-20)��
(3)��HI(g)�����ܱ������У�ij�¶��·������б仯��2HI(g)![]() H2(g)+I2(g) ��H<0
H2(g)+I2(g) ��H<0
�ٸ÷�Ӧƽ�ⳣ���ı���ʽΪK=____����H2(g)+I2(g)![]() 2HI(g)ƽ�ⳣ���ı���ʽΪK1=_____(��K��ʾ)��
2HI(g)ƽ�ⳣ���ı���ʽΪK1=_____(��K��ʾ)��
�ڵ���Ӧ�ﵽƽ��ʱc(I2)=0.5mol/L��c(HI)=4mol/L����c(H2)Ϊ_______��HI�ķֽ���Ϊ______��
�����жϸ÷�Ӧ�ﵽƽ��״̬��������______
A.������ѹǿ���� B.���������c(HI)���� C.c(I2)=c(H2) D.v(I2)��=v(H2)��
(4)���÷�Ӧ800��ﵽƽ��״̬����ƽ�ⳣ��Ϊ1.0��ijʱ�̣���������ڸ����ʵ��ܶȷֱ�Ϊc(HI)=2mol/L��c(I2)=1mol/L��c(H2)=1mol/L�����ʱ�̣���Ӧ��______(������������������������ͬ)���У��������¶ȣ���Ӧ��______���С�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ճ������ũҵ������Ӧ�ü�Ϊ�㷺��һ�ֽ�������ش��������⣺
��1��ij�о���ѧϰС��Ϊ��֤�����Ľ����Ա�ͭ��ǿ����������¼��ַ��������к�������___������ţ���
A.��Ƭ��������ͭ��Һ���û���ͭ
B.����ͭ��������Ӧ�ֱ�����FeCl3��CuCl2
C.ͭƬ����FeCl3��Һ�У�ͭƬ���ܽ�
D.��Ƭ��ͭƬ�ֱ�����ʢ��ϡ������ձ��У���Ƭ�������ݲ�������ͭƬ�������ݲ���
E.�����£�����Ƭ��ͭƬ�ֱ�����Ũ�����У���Ƭ���ܽ⣬��ͭƬ�ܽ�
��2�����������һ����֤�����Ľ����Ա�ͭ��ǿ��ʵ�顣Ҫ��ʵ�鷽����ԭ����ͬ�ڣ�1�����κ�һ��������
�ٻ���ʵ��װ��ͼ��ע������ҩƷ___��
��д��ʵ������е���Ҫ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������֮���ת����ϵ����ͼ������������ʡ�ԡ�C��D����X��Y��Z������Ԫ����ɵĻ����X��Y��Z��ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С��Y��Zԭ������������֮��Ϊ10��DΪ��ɫ�ǿ�ȼ�����壬GΪ����ɫ�������壬J��MΪ������I��Ư�����ã���Ӧ![]() ����������ӡˢ��·�塣
����������ӡˢ��·�塣
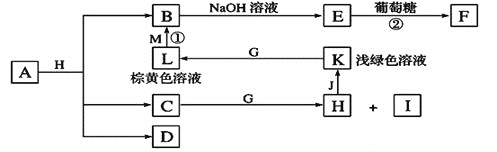
��ش��������⣺
(1)![]() Ԫ�������ڱ��е�λ��______________________��C�ĵ���ʽ______________��
Ԫ�������ڱ��е�λ��______________________��C�ĵ���ʽ______________��
(2)�Ƚ�Y��Z��ԭ�Ӱ뾶��С��___________________![]() ��дԪ�ط���
��дԪ�ط���![]() ��
��
(3)д��ʵ�����Ʊ�G�����ӷ�Ӧ����ʽ��_________________________________��
(4)����D��NaOH��Һ��Ӧ������������P��Q����P��Na����������Ϊ![]() ��������Ϊ____________��
��������Ϊ____________��
(5)ʵ�����м���L��Һ�е������ӳ�ѡ��__________![]() �ѧʽ
�ѧʽ![]() ��Һ��������__________________________________________��
��Һ��������__________________________________________��
(6)![]() �а���X��Y��ZԪ�أ�A�Ļ�ѧʽΪ_________________________________��
�а���X��Y��ZԪ�أ�A�Ļ�ѧʽΪ_________________________________��
(7)�о�����������D��һ�������¿ɱ���ԭΪ��Ө���ľ���N����ṹ��ԭ�ӵ�����Ϊ�������壬��д��N����һ��ͬ�������������______________��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ѵ�������ķ�Ӧ��4H2(g)��2NO(g)��SO2(g)![]() N2(g)��S(l)��4H2O(g)��H��0�������й�˵����ȷ���ǣ� ��
N2(g)��S(l)��4H2O(g)��H��0�������й�˵����ȷ���ǣ� ��
A.��v(H2)��v(H2O)ʱ���ﵽƽ��
B.�����¶ȣ�����Ӧ���ʼ�С���淴Ӧ��������ѧƽ�������ƶ�
C.ʹ�ø�Ч���������NO��ƽ��ת����
D.��ѧƽ�ⳣ������ʽΪK��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѱ���Ϊ��δ����������������Ӳ�ȴ��۵�ߣ���ʴ���ص㡣ij������������(��Ҫ�ɷ�FeTiO3)Ϊ��Ҫԭ�ϣ�ұ������Ti���乤ҵ����������ͼ��
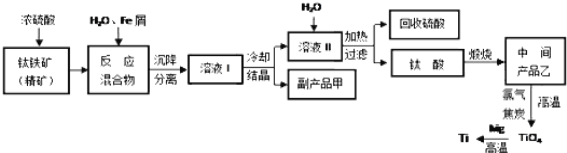
��֪��FeTiO3+2H2SO4=TiOSO4+FeSO4+2H2O
�ش��������⣺
(1)�������������м�����м��Ŀ����___�����鸱��Ʒ���Ƿ���ʵ�ʵ�鷽����___��
(2)����ҺI��ü��壬��Ҫ����___���������ձ���©���⣬���˲�����Ҫ�õ���һ�ֲ����������������ڴ˲����е���Ҫ������___��
(3)TiO2��ΪTiCl4�Ļ�ѧ����ʽ___������������ڷ�ֱ�ӵ���м��Ʒ����ȡ�����ѻ�óɹ����ԱȽ��õ�ⷨ�����ѱ�ԭ���յ�����___��
(4)�ù���������33.6LCl2(���)�����ٿɵ�___�˼��塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I������P(s)��Cl2(g)������Ӧ����PCl3��PCl5����Ӧ���̺�������ϵ��ͼ��ʾ(ͼ�е���H��ʾ����1mol���������)��������ͼ�ش��������⣺

(1)PCl5�ֽ�����PCl3��Cl2���Ȼ�ѧ����ʽ____________________�������ֽⷴӦ��һ�����淴Ӧ���¶�T1ʱ�����ܱ������м���0.8molPCl5����Ӧ�ﵽƽ��ʱ��ʣ��0.6molPCl5����ֽ�����1����________������Ӧ�¶���T1���ߵ�T2��ƽ��ʱPCl5�ķֽ�����2����2________��1(��������������С��������������)��
(2)��ҵ���Ʊ�PCl5ͨ�����������У��Ƚ�P��Cl2��Ӧ�����м����PCl3��Ȼ���£��ٺ�Cl2��Ӧ����PCl5��ԭ����_________________________________________________��
(3)P��Cl2��������Ӧ����1molPCl5����H3��____________��
����ijѧ����Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ���ʵ��ʱ����2֧�Թܱ��Ϊ�٢ڣ������±������ʵ�������ʵ�飬��¼��ʱ�������ǣ�16s��28s���뽫2�����������±����ʵ�λ�ã���д��ʵ����ۡ�
�Թܱ�� | ����3%Na2S2O3 | ��H2O | ��ϡ����(1��5) | ���ֻ���ʱ�� |
�� | 3mL | 3mL | 5�� | a._____s |
�� | 4mL | 2mL | 5�� | b._____s |
(1)����Ӧ�٢ڵ�ʱ��ֱ�д����a.____________��b.____________��
(2)ʵ�����____________________________________��
(3)д����Ӧ�Ļ�ѧ����ʽ_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��̽�������ڲ�ͬ��Һ�е�������ʴ��
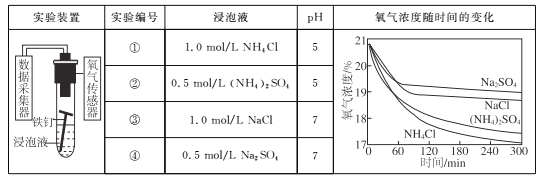
����˵������ȷ����
A. ����������Ӧ��ΪO2+4e-+2H2O=4OH-
B. �ڲ�ͬ��Һ�У�Cl��Ӱ��������ʴ���ʵ���Ҫ����
C. ��ʵ����м�������(NH4)2SO4���壬������ʴ���ʼӿ�
D. ��300 min�ڣ�������ƽ��������ʴ����������Һ����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�һ���̽���¼�����CO2�����ۺ�����, CO2�������ϳɵ�̼����
CO2(g) +4H2(g) ![]() CH4(g) + 2H2O(g) ��H= a kJ/mol
CH4(g) + 2H2O(g) ��H= a kJ/mol
(1)��֪����4H2��g��+ 2O2��g��=4H2O��g�� ��H=-967.2kJ/mol��
��CH4(g) + 2O2(g) =CO2(g) + 2H2O(g) ��H=-802.0 kJ/mol��
��ش��٢���������Ӧ������ѧ�����ƾ��ܴ���ԭ����__________________�� a=____________kJ/mol��
(2)�����Ϊ1L���ܱո��������У�����4mol H2��1mol CO2������¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ1��ʾ��
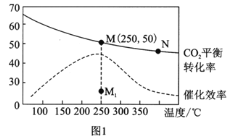
����֪M����ѹΪ1MPa���÷�Ӧ�ڴ��¶��µ�ƽ�ⳣ��Kp=______MPa-2��(Kp����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ���������ѹ=������ѹ�������������
�������Ӷ�����̼��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��__________��
A��ͨ��������� B������¶�
C�����Ӷ�����̼Ũ�� D����������Ũ��
������˵����ȷ����_________��
A��ƽ�ⳣ����С��KN>KM
B�������������䣬����ʹ�ô�������250�� ʱCO2��ƽ��ת���ʿ���λ�ڵ�M1
C��ͼ1��M��ʱ��������������Ϊ12.5%
D����ѹǿ��n( H2)/n(CO2)����ʱ����֤����ѧ��Ӧ�Ѵﵽƽ��״̬
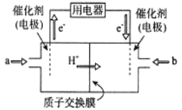
(3)����Ч�ļ���ȼ�ϵ�ع���ʱ�ܷ�Ӧʽ��CH4+2O2=CO2+2H2O��
���õ�صĸ�����___________(��a��b)���������缫��ӦʽΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. ��100 mL 3 mol��L��1��H2SO4��100 mL H2O��ϣ���������ʵ���Ũ��Ϊ1.5 mol��L��1
B. ��100 g 20%��NaCl��Һ��100 g H2O��Ϻ�NaCl��Һ������������10%
C. ��200 mL 3 mol��L��1��BaCl2��Һ��100 mL 3 mol��L��1��KCl��Һ��Ϻ���Һ�е�c(Cl��)��Ȼ��3 mol��L��1
D. ��100 mL 20%��NaOH��Һ��100 mL H2O��Ϻ�NaOH��Һ������������10%
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com