
ЁОЬтФПЁПЯжгаВПЗжЖЬжмЦкжїзхдЊЫиЕФаджЪЛђдзгНсЙЙШчЯТБэЃК
дЊЫиБрКХ | дЊЫиаджЪЛђдзгНсЙЙ |
T | MВуЩЯЕчзгЪ§ЪЧKВуЩЯЕчзгЪ§3БЖ |
X | зюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ2БЖ |
Y | ГЃЮТЯТЕЅжЪЮЊЫЋдзгЗжзгЃЌЦфЧтЛЏЮяЫЎШмвКГЪМюад |
Z | дЊЫизюИпе§МлЪЧ+7Мл |
(1)дЊЫиXЕФвЛжжЭЌЮЛЫиПЩВтЖЈЮФЮяФъДњЃЌетжжЭЌЮЛЫиЕФЗћКХЪЧ____ЁЃ
(2)дЊЫиYгыЧтдЊЫиаЮГЩвЛжжРызгYH4+ЃЌаДГіИУЮЂСЃЕФЕчзгЪН____ЃЈгУдЊЫиЗћКХБэЪОЃЉЁЃ
(3)дЊЫиZгыдЊЫиTЯрБШЃЌЗЧН№ЪєадНЯЧПЕФЪЧ____ЃЈгУдЊЫиЗћКХБэЪОЃЉЃЌЯТСаБэЪіжаФмжЄУїетвЛЪТЪЕЕФЪЧ____ЁЃ
aЃЎГЃЮТЯТZЕФЕЅжЪКЭTЕФЕЅжЪзДЬЌВЛЭЌ
bЃЎZЕФЧтЛЏЮяБШTЕФЧтЛЏЮяЮШЖЈ
cЃЎвЛЖЈЬѕМўЯТZКЭTЕФЕЅжЪЖМФмгыЧтбѕЛЏФЦШмвКЗДгІ
(4)TЕФвЛжжбѕЛЏЮяФмЪЙZЕЅжЪЕФЫЎШмвКЭЪЩЋЗДгІЕФРызгЗНГЬЪНЮЊ______ЁЃ
(5)TдкжмЦкБэжаЕФЮЛжУЪЧЕк________жмЦкЃЌЕк_________зхЁЃ
ЁОД№АИЁП 14C 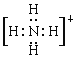 Cl b Cl2+SO2+2H2OЃНSO42Ѓ+2ClЃ+4H+ Ш§ ЕкЂіAзх
Cl b Cl2+SO2+2H2OЃНSO42Ѓ+2ClЃ+4H+ Ш§ ЕкЂіAзх
ЁОНтЮіЁП
ЖЬжмЦкдЊЫижаЃЌTдЊЫиMВуЩЯЕчзгЪ§ЪЧKВуЩЯЕчзгЪ§3БЖЃЌЙЪTЮЊSдЊЫиЃЛXдЊЫидзгзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ2БЖЃЌдзгжЛФмга2ИіЕчзгВуЃЌзюЭтВуЕчзгЪ§ЮЊ4ЃЌЙЪXЮЊCдЊЫиЃЛГЃЮТЯТYЕЅжЪЮЊЫЋдзгЗжзгЃЌЦфЧтЛЏЮяЫЎШмвКГЪМюадЃЌПЩжЊYЪЧNдЊЫиЃЛдЊЫиZзюИпе§МлЪЧ+7МлЃЌдђZЪЧClЃЌвдДЫНтД№ИУЬтЁЃ
ИљОнвдЩЯЗжЮіПЩжЊTЮЊSЃЌXЮЊCЃЌYЪЧNЃЌZЪЧClЃЌдђ
ЃЈ1ЃЉЬМдЊЫиЕФвЛжжЭЌЮЛЫиПЩВтЖЈЮФЮяФъДњЃЌИУЭЌЮЛЫиКЌга8ИіжазгЃЌдђжазгЪ§ЮЊ6+8=14ЃЌетжжЭЌЮЛЫиЕФЗћКХЪЧ14CЃЛ
ЃЈ2ЃЉдЊЫиYгыЧтдЊЫиаЮГЩвЛжжРызгNH4+ЃЌИУЮЂСЃЕФЕчзгЪНЮЊ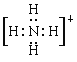 ЃЛ
ЃЛ
ЃЈ3ЃЉSКЭClЮЛгкжмЦкБэЯрЭЌжмЦкЃЌClдЊЫиЗЧН№ЪєадНЯЧПЃЌПЩИљОнЧтЛЏЮяЕФЮШЖЈадЁЂзюИпМлКЌбѕЫсЕФЫсадЧПШѕЁЂЕЅжЪжЎМфЯрЛЅжУЛЛЕШНјааХаЖЯЃЌЕЅжЪЖМФмгыЧтбѕЛЏФЦЗДгІЁЂЕЅжЪзДЬЌЕШЖМВЛФмгУгкБШНЯЗЧН№ЪєадЃЌД№АИбЁbЃЛ
ЃЈ4ЃЉTЕФвЛжжбѕЛЏЮяФмЪЙZЕЅжЪЕФЫЎШмвКЭЪЩЋЃЌИУбѕЛЏЮяЪЧЖўбѕЛЏСђЃЌЗДгІЕФРызгЗНГЬЪНЮЊCl2+SO2+2H2OЃНSO42Ѓ+2ClЃ+4H+ЁЃ
ЃЈ5ЃЉСђдЊЫиЮЛгкдЊЫижмЦкБэЕФЕкШ§жмЦкЕкЂіAзхЁЃ


 Ек1ОэЕЅдЊдТПМЦкжаЦкФЉЯЕСаД№АИ
Ек1ОэЕЅдЊдТПМЦкжаЦкФЉЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
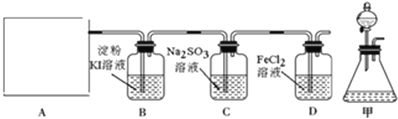
ЁОЬтФПЁПТШЦјЪЧвЛжжживЊЕФЙЄвЕдСЯЃЌФГбаОПадбЇЯАаЁзщВщдФзЪСЯЕУжЊЃЌЦЏАзЗлгыСђЫсЗДгІПЩжЦШЁТШЦјЃЌЛЏбЇЗНГЬЪНЮЊЃКCaЃЈClOЃЉ2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2Ёќ+2H2OЁЃЫћУЧРћгУИУЗДгІЩшМЦШчЭМЫљЪОжЦШЁТШЦјВЂбщжЄЦфаджЪЕФЪЕбщЁЃ
2CaSO4+2Cl2Ёќ+2H2OЁЃЫћУЧРћгУИУЗДгІЩшМЦШчЭМЫљЪОжЦШЁТШЦјВЂбщжЄЦфаджЪЕФЪЕбщЁЃ
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉИУЪЕбщжаAВПЗжЕФзАжУЪЧ______ЃЈЬюБъКХЃЉЁЃ
ЃЈ2ЃЉзАжУBжаВњЩњЕФЯжЯѓЮЊ______ЁЃ
ЃЈ3ЃЉЧыЩшМЦЪЕбщбщжЄзАжУCжаЕФNa2SO3вбБЛбѕЛЏ______ЁЃ
ЃЈ4ЃЉаДГіDзАжУжаЗЂЩњЗДгІЕФРызгЗНГЬЪН______ЁЃ
ЃЈ5ЃЉИУЪЕбщДцдкУїЯдЕФШБЯнЃЌЧыФуЬсГіИФНјЕФЗНЗЈ______ЁЃ
ЃЈ6ЃЉШєНЋЩЯЪізАжУИФЮЊжЦШЁSO2ВЂЗжБ№бщжЄSO2ЕФЦЏАзадЁЂбѕЛЏадКЭЛЙдадЕШаджЪЁЃBжа______ШмвКЭЪЩЋЃЌдђЫЕУїВњЩњЕФЦјЬхЮЊSO2ЃЛCжаNa2SШмвКГіЯж______ЃЛDжа______ШмвКЭЪЩЋЃЌЫЕУїSO2гаЛЙдадЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
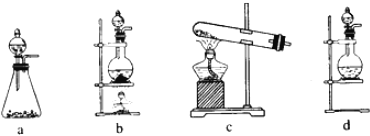
ЁОЬтФПЁПЮвЙњдЄМЦдк2020ФъЧАКѓНЈГЩздМКЕФдиШЫПеМфеОЁЃЮЊСЫЪЕЯжПеМфеОЕФСуХХЗХЃЌбЛЗРћгУШЫЬхКєГіЕФCO2ВЂЬсЙЉO2ЃЌЮвЙњПЦбЇМвЩшМЦСЫвЛжжзАжУЃЈШчЯТЭМЃЉЃЌЪЕЯжСЫЁАЬЋбєФмвЛЕчФмвЛЛЏбЇФмЁБзЊЛЏЃЌзмЗДгІЗНГЬЪНЮЊ2CO2=2CO+O2 ЁЃЙигкИУзАжУЕФЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
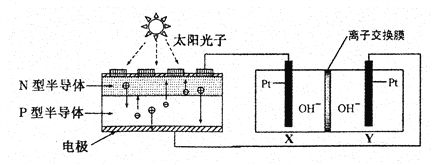
зАжУa зАжУb
ИНЃКЈБэЪОбєРызгЃЌІЈБэЪОвѕРызг
A. зАжУaНЋЬЋбєФмзЊЛЏЮЊЕчФмЃЌзАжУbНЋЕчФмзЊЛЏЮЊЛЏбЇФм
B. ЙЄзїЙ§ГЬжаOHЃЯђYЕчМЋжмЮЇвЦЖЏ
C. ШЫЬхКєГіЕФЦјЬхВЮгыXЕчМЋЕФЗДгІЃКCO2+2eЃ+H2O=CO+2OHЃ
D. ЗДгІЭъБЯКѓЛжИДЕНдЮТЖШЃЌзАжУbжаЕчНтжЪШмвКЕФМюадМѕШѕ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈЬтЮФЃЉI. ЮвУЧвбОбЇЯАСЫЭЌЮЛЫиЁЂЭЌЯЕЮяЁЂЭЌЫивьаЮЬхЁЂЭЌЗжвьЙЙЬхЃЌЯТУцСаГіСЫМИзщЮяжЪЃЌЧыгУЮяжЪЕФзщКХЬюаДЯТБэЃК
гаЯТСаИїзщЮяжЪЃК
AЃЎO2КЭO3ЃЈГєбѕЃЉ BЃЎ12CКЭ13C CЃЎCH3CH2CH2CH3КЭCH3CHЃЈCH3ЃЉ2
D. CH4КЭC6H14 EЃЎ  КЭ
КЭ  F. H+КЭD+
F. H+КЭD+
РрБ№ | ЭЌЮЛЫи | ЭЌЯЕЮя | ЭЌЫивьаЮЬх | ЭЌЗжвьЙЙЬх |
зщКХ | _______ | _______ | _______ | _______ |
ЂђЃЎЯТЭМЮЊЫФжжЬўЕФЧђЙїФЃаЭЃЌАДвЊЧѓЬюПе

ЃЈ1ЃЉЕШжЪСПЕФвдЩЯЫФжжЬўЭъШЋШМЩеЃЌЯћКФO2зюЖрЕФЪЧ_______ЃЈЬюзжФИађКХЃЉ
ЃЈ2ЃЉФмЫЕУїDЗжзгжаЕФЬМЬММќВЛЪЧЕЅЫЋМќНЛЬцЕФЪТЪЕЪЧ_________ЃЈЬюађКХЃЉ
ЂйDВЛФмЪЙЫсадKMmO4ШмвКЭЪЩЋ ЂкDжаЬМЬММќЕФМќГЄМќФмЖМЯрЕШ
ЂлСкЖўдЊШЁДњВњЮяжЛгавЛжж ЂмМфЖўдЊШЁДњжЛгавЛжж
ЂндквЛЖЈЬѕМўЯТDгыH2ЗЂЩњМгГЩЗДгІЩњГЩЛЗвбЭщ
Ђѓ.АДвЊЧѓЭъГЩЯТСаЮЪЬтЃК
ЃЈ1ЃЉБћЯЉЭЈШыЕНфхЕФЫФТШЛЏЬМШмвКжаЕФЛЏбЇЗНГЬЪНЃК_________ЁЃ
ЃЈ2ЃЉЮьЭщЕФФГжжЭЌЗжвьЙЙЬхЕФвЛТШДњЮяжЛгавЛжжЃЌЦфНсЙЙМђЪНЮЊ_____________ЁЃ
ЃЈ3ЃЉгУЯЕЭГУќУћЗЈИјЯТСагаЛњЮяУќУћЃК
Ђй ____________ЁЃ
____________ЁЃ
Ђк ________ЁЃ
________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИљОнЯУУХЦјЯѓЬЈБЈЕРЃЌНќФъУПЕНДКМОЃЌЯУУХЪаОГЃГіЯжДѓЮэЬьЦјЃЌжТЪЙИпЫйЙЋТЗЙиБеЃЌКНАрЭЃЗЩЃЎЮэЪєгкЯТСаЗжЩЂЯЕжаЕФЃЈ ЃЉ
A.ШмвК
B.аќзЧвК
C.ШщзЧвК
D.НКЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋ30mL0.5molЁЄLЃ1Ba(OH)2ШмвКМгЫЎЯЁЪЭЕН500mLЃЌЯЁЪЭКѓЕФШмвКжаOHЃЕФЮяжЪЕФСПХЈЖШЮЊЃЈ ЃЉ
A.0.3molЁЄLЃ1B.0.06molЁЄLЃ1C.0.03molЁЄLЃ1D.0.02molЁЄLЃ1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаБэЪОЛЏбЇЙ§ГЬЕФЛЏбЇгУгяЪщаДе§ШЗЕФЪЧ
A. BaSO4ЭЖШыЫЎжаКѓНЈСЂЕФГСЕэШмНтЦНКт:BaSO4![]() Ba2++SO42-
Ba2++SO42-
B. AlCl3ШмвКгыNaAlO2ШмвКЛьКЯ:A13++A1O2-+3H2O![]() 2Al(OH)3Ё§
2Al(OH)3Ё§
C. HCO3-ЕФЕчРы:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D. Na2SO3ЕФЫЎНт:SO32-+2H2O![]() H2SO3+2OH-
H2SO3+2OH-
ЁОД№АИЁПC
ЁОНтЮіЁПбЁЯюAЕФЦНКтгІИУБъзЂИїЮяжЪЕФзДЬЌЃЌМДЮЊЃКBaSO4ЃЈsЃЉ![]() Ba2+ЃЈaqЃЉ+SO42-ЃЈaqЃЉЃЌбЁЯюAДэЮѓЁЃбЁЯюBЕФЕчКЩВЛЪиКуЃЌгІИУЮЊA13++3A1O2-+6H2O
Ba2+ЃЈaqЃЉ+SO42-ЃЈaqЃЉЃЌбЁЯюAДэЮѓЁЃбЁЯюBЕФЕчКЩВЛЪиКуЃЌгІИУЮЊA13++3A1O2-+6H2O![]() 4Al(OH)3Ё§ЃЌбЁЯюBДэЮѓЁЃНЋбЁЯюCЕФЗНГЬЪНСНБпИїШЅЕєвЛИіЫЎЗжзгЃЌМДЕУЕН:HCO3-
4Al(OH)3Ё§ЃЌбЁЯюBДэЮѓЁЃНЋбЁЯюCЕФЗНГЬЪНСНБпИїШЅЕєвЛИіЫЎЗжзгЃЌМДЕУЕН:HCO3-![]() CO32-+H+ЃЌБэЪОЕФЪЧЬМЫсЧтИљЕФЕчРыЃЌбЁЯюCе§ШЗЁЃбЧСђЫсИљРызгЕФЫЎНтгІИУЗжВННјааЃЌбЁЯюDДэЮѓЁЃ
CO32-+H+ЃЌБэЪОЕФЪЧЬМЫсЧтИљЕФЕчРыЃЌбЁЯюCе§ШЗЁЃбЧСђЫсИљРызгЕФЫЎНтгІИУЗжВННјааЃЌбЁЯюDДэЮѓЁЃ
ЁОЬтаЭЁПЕЅбЁЬт
ЁОНсЪјЁП
17
ЁОЬтФПЁПЯТСаЩњЛюжаЕФЛЏбЇЯжЯѓНтЪЭВЛе§ШЗЕФЪЧ
A. ЩњЪЏЛвПЩзїЪГЦЗЫйШШМСЪЧРћгУдЕчГидРэ
B. ХнФУ№Л№ЦїЪЧдЫгУЫЋЫЎНтдРэВњЩњCO2
C. ТСбЮПЩзїОЛЫЎМСЪЧРћгУТСРызгЫЎНтВњЩњНКЬх
D. НЋУКЦјжаЖОЕФШЫвЦЕНЭЈЗчДІЃЌЪЧдЫгУЦНКтРэТл
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУШлШкМюБКЩеЙЄвеПЩДгТСШШЗЈЩњВњН№ЪєИѕЕФИѕдќЃЈAlЁЂAl2O3ЁЂCr2O3ЕШЃЉжаНўГіИѕКЭТСЃЌЮЊЪЕЯжИѕКЭТСЕФдйЩњРћгУЁЃЦфЙЄзїСїГЬШчЯТЃК

ЃЈ1ЃЉТСШШЗЈвБСЖН№ЪєИѕЃЌЪЧРћгУСЫН№ЪєТСЕФ__________ЃЈЬюЁАбѕЛЏадЁБЛђЁАЛЙдадЁБЃЉЁЃ
ЃЈ2ЃЉШмвК1жаЕФвѕРызггаCrO42-ЁЂ__________ЁЃ
ЃЈ3ЃЉЙ§ГЬIЃЌдкCr2O3ВЮгыЕФЗДгІжаЃЌШєЩњГЩ0.4molCrO42-ЃЌЯћКФбѕЛЏМСЕФЮяжЪЕФСПЪЧ__________ЁЃ
ЃЈ4ЃЉЭЈШыCO2ЕїНкШмвКpHЪЕЯжЮяжЪЕФЗжРыЁЃ
ЂйТЫдќAьбЩеЕУЕНAl2O3ЃЌдйгУЕчНтЗЈвБСЖAlЁЃвБСЖAlЕФЛЏбЇЗНГЬЪНЪЧ____________________ЁЃ
ЂкТЫдќBЪмШШЗжНтЫљЕУЮяжЪЕФбЛЗРћгУЃЌBЪЧ__________ЁЃ
ЂлвбжЊЃК2CrO42-+2H+![]() Cr2O72-+H2O K=4.0ЁС1014
Cr2O72-+H2O K=4.0ЁС1014
ТЫвК3жаCr2O72-ЕФШмЖШЪЧ0.04mol/LЃЌдђCrO42-ЕФХЈЖШЪЧ__________mol/LЁЃ
ЃЈ5ЃЉЙ§ГЬIIЕФФПЕФЪЧЕУЕНK2Cr2O7ДжЦЗЁЃВЛЭЌЮТЖШЯТЛЏКЯЮяЕФШмНтЖШЃЈg/100gH2OЃЉ
ЛЏКЯЮяУћГЦ | 0Ёц | 20Ёц | 40Ёц | 60Ёц | 80Ёц |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 |
K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
НсКЯБэжаЪ§ОнЗжЮіЃЌЙ§ГЬIIЕФВйзїЪЧЃК____________________ЃЌЙ§ТЫЃЌЕУЕНK2Cr2O7ДжЦЗЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮТЖШЮЊTЪБЃЌЯђЬхЛ§ЮЊ2 LЕФКуШнУмБеШнЦїжаМгШызуСПЬњЗлКЭ0.08 mol H2O(g)ЃЌЗЂЩњЗДгІ3Fe(s)ЃЋ4H2O(g)![]() Fe3O4(s)ЃЋ4H2(g)ЃЌвЛЖЮЪБМфКѓДяЦНКтЁЃt1ЪБПЬЯђШнЦїжадйГфШывЛЖЈСПЕФH2ЃЌдйДЮДяЦНКтЪБH2ЕФЬхЛ§ЗжЪ§ЮЊ20%ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
Fe3O4(s)ЃЋ4H2(g)ЃЌвЛЖЮЪБМфКѓДяЦНКтЁЃt1ЪБПЬЯђШнЦїжадйГфШывЛЖЈСПЕФH2ЃЌдйДЮДяЦНКтЪБH2ЕФЬхЛ§ЗжЪ§ЮЊ20%ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
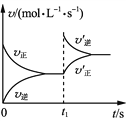
A. t1ЪБПЬГфШыH2ЃЌvЁфе§ЁЂvЁфФцБфЛЏШчгвЭМ
B. ЕквЛДЮДяЦНКтЪБЃЌH2ЕФЬхЛ§ЗжЪ§аЁгк20%
C. ЮТЖШЮЊTЪБЃЌЦ№ЪМЯђдШнЦїжаГфШы0.1 molЬњЗлЁЂ0.04 mol H2O(g)ЁЂ0.1 mol Fe3O4(s)ЁЂ0.005 mol H2(g)ЃЌЗДгІЯђе§ЗДгІЗНЯђНјаа
D. ЮТЖШЮЊTЪБЃЌЯђКубЙШнЦїжаМгШызуСПFe3O4(s)КЭ0.08 mol H2 (g)ЃЌДяЦНКтЪБH2(g)зЊЛЏТЪЮЊ20%
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com