
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为__(填“吸热”或“放热”)反应,且m+n_(填“>”“=”或“<”)p。
(2)减压使容器体积增大时,A的质量分数__。(填“增大”“减小”或“不变”,下同)
(3)若升高温度,则平衡时B、C的浓度之比![]() 将___。
将___。
(4)若加入催化剂,平衡时气体混合物的总物质的量____。
【答案】放热 > 增大 减小 不变
【解析】
(1)升高温度,平衡向吸热方向移动;减小压强,平衡向气体系数和增大的方向移动;
(2) 减小压强时,平衡向逆反应方向移动;
(3)升高温度,平衡正向移动;
(4)催化剂不能使平衡移动。
(1)对反应:mA(g)+nB(g)![]() pC(g)达平衡后,升高温度时,B的转化率变大,说明平衡向正反应方向移动,正反应为吸热反应;减小压强时,混合体系中C的质量分数减小,说明平衡向逆反应方向移动,即m+n>p;
pC(g)达平衡后,升高温度时,B的转化率变大,说明平衡向正反应方向移动,正反应为吸热反应;减小压强时,混合体系中C的质量分数减小,说明平衡向逆反应方向移动,即m+n>p;
(2)减小压强时,混合体系中C的质量分数减小,说明平衡向逆反应方向移动,A的质量分数增大;
(3)升高温度时,平衡向正反应方向移动,c(C)增大,c(B)减小,即![]() 减小;
减小;
(2)加入催化剂,平衡不移动,混合物的总物质的量不变。


科目:高中化学 来源: 题型:
【题目】氨的催化氧化是工业制硝酸的重要反应:4NH3+5O2![]() 4NO+6H2O,对于该反应判断正确的是
4NO+6H2O,对于该反应判断正确的是
A. 氧气被还原B. 该反应是置换反应
C. 氨气是氧化剂D. 若有17 g氨参加反应,反应中转移10 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、![]() 的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是( )
的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是( )
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)t℃时,关于N2、NH3的两个反应的信息如下表所示:
化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
N2(g)+O2(g)=2NO(g) △H>0 | a kJ/mol | b kJ/mol | K1 |
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | c kJ/mol | d kJ/mol | K2 |
请写出t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式:______________________,t℃时该反应的平衡常数为__________ (用K1和K2表示)。
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
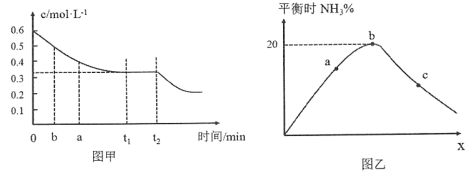
①图甲中0~t1 min内,v(N2)=_____mol·L-1·min-1;b点的v(H2)正_____a点的v(H2)逆(填“大于”“小于”或“等于”)。
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,保持温度和压强不变,又充入3 mol N2后,平衡________(填“向右移动”“向左移动”或“不移动”)。
(3)①科学家研究出以尿素为动力的燃料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,写出负极电极反应式:________________________________________________。
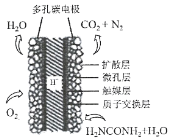
②理论上电池工作时,每消耗标准状况下2.24 L O2时,可产生的电量为________ (法拉第常数为96500C/ mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中两种气态物质M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
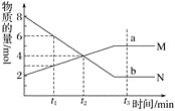
A. 反应的化学方程式为:2M![]() N
N
B. t2时,正逆反应速率相等,反应达到平衡状态
C. t3时,M上a点正反应速率等于N上b点的逆反应速率
D. t3后的单位时间段内,无论是用M表示还是用N表示,反应速率均为0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH的电离常数K=1.6×10-5,该温度下向20 mL 0.01 mol·L-1CH3COOH溶液中逐滴加入0.01 mol·L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化),请回答有关问题:
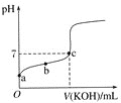
(1)a点溶液中c(H+)为____mol·L-1。
(2)b点溶液中溶质__,CH3COOH的电离常数___1.6×10-5(“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质X、Y与化合物甲、乙有如图所示的转化关系(必要的反应条件未标出),回答下列问题:

(1)若该反应用于工业上制取粗硅,反应的化学方程式为______________
(2)若X、Y为日常生活中常见的两种金属,且甲为红棕色粉末,相应的化学方程式为_____。
(3)若X、乙的焰色反应均呈黄色,甲是一种常见的无色无味的液体,则乙物质中所含的化学键类型有_________
(4)若X是黄绿色气体,甲、乙两种气体相遇会产生白烟,则X与甲反应的化学方程式为__________。
(5)若X中的元素是海水中含量最多的金属元素,甲是相对分子质量为46且常温下能使酸性KMnO4溶液褪色的烃的含氧衍生物,则X与甲反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中不能用化合反应的方法制得的是
①SO2 ②H2SiO3 ③Fe(OH)3 ④ Mg(OH)2 ⑤ FeCl2 ⑥CaSiO3
A.①③④⑥B.①②④C.②④⑤D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com