
����Ŀ��2019�꡶��ѧ�������ڿ����濯����ͼ��ʾ���л���M(ֻ��C��H��O)�����ģ��ͼ����ͬ��С����ɫ��С�������ͬ��ԭ�ӣ�С��֮�����������ʾ���ۼ����ȿ��Ա�ʾ������Ҳ���Ա�ʾ˫���������Ա�ʾ�����������й�M���ƶ���ȷ����
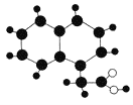
A.M�ķ���ʽΪC12H12O2
B.M������������һ�������·�Ӧ�IJ���Ļ���һ�ȴ�����7��
C.M�ܷ����кͷ�Ӧ��ȡ����Ӧ���ӳɷ�Ӧ
D.һ��M���������11��ԭ�ӹ���
���𰸡�C
��������
�������ģ�ͣ��Ƴ����л���ṹ��ʽΪ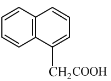 ���ݴ˷�����
���ݴ˷�����
A.���������ģ���Ƴ�M�Ļ�ѧʽΪC12H10O2����A����
B.��M������������һ�������·����ӳɷ�Ӧ���õ�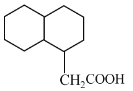 ��������10�ֲ�ͬ���⣬��˻���һ�ȴ�����10�֣���B����
��������10�ֲ�ͬ���⣬��˻���һ�ȴ�����10�֣���B����
C.��M�����Ȼ��ͱ������ܷ����кͷ�Ӧ��ȡ����Ӧ���ӳɷ�Ӧ����C��ȷ��
D.�����Ŀռ乹����ƽ���������Σ�M�����к���2�����������һ��M���������22��ԭ�ӹ��棬��D����
�𰸣�C��


 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10�֣�Ǧ�����dz��õĻ�ѧ��Դ����缫���Ϸֱ���Pb��PbO2�����ҺΪϡ���ᡣ�ŵ�ʱ���õ���ܷ�ӦʽΪ��Pb��PbO2��2H2SO4 ![]() 2PbSO4��2H2O���������������жϣ�
2PbSO4��2H2O���������������жϣ�
��1�������صĸ���������_________���ŵ�ʱ����_________�����������ԭ������Ӧ��
��2�������طŵ�ʱ���������Һ������_________�����������С�����䡱�����������Һ������������_________�����������������
��3����֪����ǦΪ������ˮ�İ�ɫ���壬����ʱ�����ڵ缫�ϡ���д���õ�طŵ�ʱ�������ĵ缫��Ӧ_______________________________________�������ӷ���ʽ��ʾ����
��4������ȼ�ϵ�ؾ��������졢Ч�ʸߵ��ŵ㣬�������ܶȸ���Ǧ���ء��������ΪKOH��Һ��������ȼ�ϵ�صĸ�����ӦʽΪ____________________���õ�ع���ʱ�����·ÿ����1��103 mol e�������ı��������_________m3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ȼ�ѧ����ʽ��˵����ȷ����
A. H2��ȼ����Ϊ285.8 kJ��mol1�����ʾH2ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��H2(g)+ ![]() O2
O2![]() H2O(g) ��H=285.8 kJ��mol1
H2O(g) ��H=285.8 kJ��mol1
B. �к���Ϊ57.3 kJ��mol1����NaOH����ᷴӦ���к��ȿ��Ա�ʾ���£�NaOH(aq)+CH3COOH(aq)![]() CH3COONa(aq)+H2O(l) ��H=57.3 kJ��mol1
CH3COONa(aq)+H2O(l) ��H=57.3 kJ��mol1
C. ��֪��C(s�����ʯ)+O2(g)![]() CO2(g) ��H=395.4 kJ��mol1��C(s��ʯī)+O2(g)
CO2(g) ��H=395.4 kJ��mol1��C(s��ʯī)+O2(g)![]() CO2(g) ��H=393.5 kJ��mol1����C(s�����ʯ)
CO2(g) ��H=393.5 kJ��mol1����C(s�����ʯ)![]() C(s��ʯī)��H=1.9 kJ��mol1
C(s��ʯī)��H=1.9 kJ��mol1
D. ��֪1 mol CH4��ȫȼ������CO2��Һ̬ˮ�ų�890.4 kJ����������÷�Ӧ��ת��1 mol����ʱ�ų�������Ϊ222.6 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ҫ��Ni������Al��Fe��SiO2�������������ᡢ������ʡ����÷��������Ʊ�NiSO4��7H2O���壬��������ͼ��
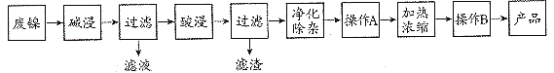
��֪��Ksp[Fe(OH)3]=8.0��10��38��Ksp[Fe(OH)2]=8.0��10��16��Ksp[Al(OH)3]=3.2��10��34��Ksp[Ni(OH)2]=2.0��10��15��1g2=0.3��
�ش���������
��1�������ʱ���������ӷ���ʽΪFe+2H+=Fe2++H2����____��
��2��������������Ҫ�ȼ���H2O2��Һ��������Ӧ�����ӷ���ʽΪ___��
��3��Ni2+��ǿ������Һ�л��ɱ�NaClO����ΪNiOOH���÷�Ӧ���ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о��������ˮ��Һ�е�ƽ�����˽����Ĵ�����ʽ��
(1)�����£���100mL0.01molL-1HA����Һ����μ���0.02molL-1MOH��Һ��������Һ��pH��MOH��Һ������仯��ͼ��ʾ����Һ����仯���Բ��ƣ���

�ٳ����£�0.01molL-1HA��Һ����ˮ�������c��H+��=______molL-1��
�ڳ�����һ��Ũ�ȵ�MAϡ��Һ��pH=a����a__7�����������������=�����������ӷ���ʽ��ʾ��ԭ��Ϊ_______________________________________��
��X��ʱ����Һ��c��H+����c��M+����c��A�����ɴ�С��˳����___________________��
��K��ʱ����Һ��c��H+��+c��M+����c��OH����=____molL-1��
��20��ʱ����c��H2C2O4��+c��HC2O4����+c��C2O42����=0.100molL��1��H2C2O4��NaOH�����Һ�У�H2C2O4��HC2O4-��C2O42-�����ʵ�������������ҺpH�仯�Ĺ�ϵ��ͼ��ʾ��

��Q�㣺c��H2C2O4��______c��HC2O4���������������������=����
�ڸ��¶���HC2O4-�ĵ��볣��K=___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⻯��(NaBH4)��������ԭ�������Ϸ��ݼ������ڴ�����������ˮ��Ӧ��ȡ�������۹�����ͼ��ʾ������˵������ȷ����
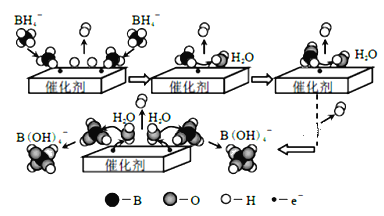
A.NaBH4����Ԫ�صĻ��ϼ�Ϊ+1��
B.����D2O����H2O����Ӧ�����ɵ������к���H2��HD��D2
C.ͨ�����ƴ����������ͱ���������Կ��������IJ�������
D.NaBH4 ��ˮ��Ӧ�����ӷ���ʽΪ��BH4��+4H2O=B(OH)4��+4H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H3PO2)��һ�־�ϸ������Ʒ������һԪ���ᣬ���н�ǿ�Ļ�ԭ�ԡ�����˵����ȷ����( )
A. �ö��Ե缫���NaH2PO2��Һ����������ӦʽΪ2H2O+4e-=O2��+4H+
B. ��H3PO2��Һ���뵽���Ը��������Һ�У�H3PO2�Ļ�ԭ�������ΪH3PO4
C. H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪH3PO2+3OH-= PO23-+3H2O
D. H3PO2����ˮ�ĵ��뷽��ʽΪH3PO2![]() H++H2PO2-
H++H2PO2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������NH3����Ρ�N2H4��N2O4������ѧ��ѧ��������ҵ������������ռ����Ҫ��λ��
��1����֪��ӦNO2(g)+CO(g)=NO(g)+CO2(g)�������仯��ͼ��ʾ������˵����ȷ����___��
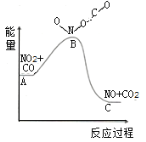
A��ͼ��A��B�Ĺ���Ϊ���ȹ���
B��1molNO2��1molCO�ļ����ܺʹ���1molNO��1molCO2�ļ����ܺ�
C���÷�ӦΪ������ԭ��Ӧ
D��1molNO2(g)��1molCO(g)������������1molNO(g)��1molCO2(g)��������
��2��N2O4��NO2֮����ڷ�ӦN2O4(g)![]() 2NO2(g)����һ������N2O4��������ܱ������У������ƽ��ת����[a(N2O4)]���¶ȵı仯��ͼ��ʾ��
2NO2(g)����һ������N2O4��������ܱ������У������ƽ��ת����[a(N2O4)]���¶ȵı仯��ͼ��ʾ��
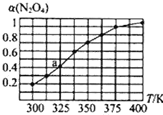
����ͼ�Ʋ�÷�Ӧ�ġ�H___0������>������<����������Ϊ___��
��ͼ��a���Ӧ�¶��£���֪N2O4����ʼѹǿΪ108kPa������¶��·�Ӧ��ƽ�ⳣ��Kp=__kPa����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
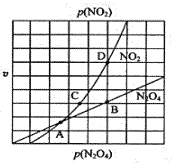
����һ�������£��÷�ӦN2O4��NO2����������������ѹǿ����ڹ�ϵv(N2O4)=k1p(N2O4)��v(NO2)=k2p2(NO2)������k1��k2���뷴Ӧ�¶��йصij�������Ӧ������ѹǿ��ϵ��ͼ��ʾ��һ���¶��£�k1��k2��ƽ�ⳣ��Kp�Ĺ�ϵ��k1=__��
��3�����ļ��Ȼ��[(CH3)4NCl]ˮ��ҺΪԭ�ϣ�ͨ����ⷨ�����Ʊ��ļ��������[(CH3)4NOH]��װ����ͼ��ʾ��
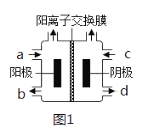
���ռ���(CH3)4NOH��������___(��a��b��c��d)��
��д�������ܷ�Ӧ(��ѧ����ʽ)___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ��������ȷ����
A.��˹����ʵ�����������غ㶨�ɵ�����
B.�ڼ��������½��еķ�Ӧ��һ�������ȷ�Ӧ
C.��3O2(g)=2O3(g)H=+284.2kJ/mol����֪O2��O3�ȶ�
D.��֪��H2(g)��ȼ������H=-285.8kJ/mol����2H2O(l)=2H2(g)+O2(g) H=+285.8kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com