
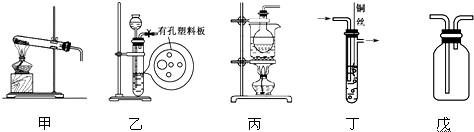
分析 (1)氨气的密度比空气小,采取向上排空气法收集;实验室用氯化铵与氢氧化钙在加热条件下制备氨气;
(2)丙中Cu与稀硝酸反应生成硝酸铜、NO与水,乙中大理石与盐酸反应生成CO2,排出装置中的空气,防止丙中NO与氧气反应;
(3)①由元素守恒可知,生成酸式盐为和KHSO4,反应的方程式为:2KClO3+H2C2O4+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+2CO2↑+2KHSO4+2H2O,氧化产物为CO2,还原产物为ClO2;
②该实验需要保持在60~80℃之间,所以缺少的一种必需的玻璃仪器名称是温度计;
③将二氧化氯溶液加入到硫化氢溶液中,所得溶液中加入少量氯化钡溶液,有白色沉淀生成,说明二氧化氯和硫化氢发生氧化还原生成SO42-.
解答 解:(1)氨气的密度比空气小,采取向上排空气法收集,所以应从短管进气,制备氨气的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:短;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)大理石与盐酸反应生成CO2,能够排出装置中的空气,防止丙中NO与氧气反应,所以装置乙的作用是:利用碳酸钙与盐酸产生的CO2排尽装置中的空气,丙中产生NO的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,
故答案为:利用碳酸钙与盐酸产生的CO2排尽装置中的空气;3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)①由元素守恒可知,生成酸式盐为和KHSO4,反应的方程式为:2KClO3+H2C2O4+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+2CO2↑+2KHSO4+2H2O,氧化产物为CO2,还原产物为ClO2,该反应中氧化产物与还原产物的物质的量之比为1:1,
故答案为:1:1;
②该实验需要保持在60~80℃之间,所以缺少的一种必需的玻璃仪器名称是温度计,
故答案为:温度计;
③将二氧化氯溶液加入到硫化氢溶液中,所得溶液中加入少量氯化钡溶液,有白色沉淀生成,说明二氧化氯和硫化氢发生氧化还原生成SO42-,白色沉淀的化学式为BaSO4,
故答案为:BaSO4.
点评 本题考查实验室制氨气、实验基本操作、离子方程式、氧化还原反应等知识,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
| A | B | |
| C | D |
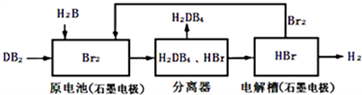
| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式CH2CH2 | |
| B. | 化学名词:乙酸乙脂、笨、油酯、坩埚 | |
| C. | 如图是某一种物质的结构简式是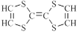 ,则该物质是一种烃 ,则该物质是一种烃 | |
| D. | 聚乙烯的化学组成表示式为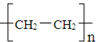 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、SO32-、S2-、K+ | B. | Fe3+、Cl-、S2-、Ba2+ | ||
| C. | Cu2+、Cl-、S2-、K+ | D. | Na+、K+、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石与盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 氯化铝溶液与氨水反应:Al3++3OH-=Al(OH)3↓ | |
| C. | 铁粉与硝酸银溶液反应:Fe+3Ag+=Fe3++3Ag | |
| D. | 醋酸与氢氧化钠溶液反应:CH3COOH+OH-=CH3COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为延长食品保质期,可向其中大量添加苯甲酸钠等防腐剂 | |
| B. | 催化转化机动车尾气为无害气体,能消除酸雨和雾霾的发生 | |
| C. | PM2.5是指空气中氮氧化物和硫氧化物含量之和 | |
| D. | “地沟油”可以制成肥皂,从而提高资源的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
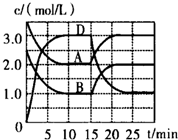 温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)?C(s)+xD(g)△H>0,容器中A、B、D的物质的量浓度随时间的变化如图所示,下列说法不正确的是( )
温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)?C(s)+xD(g)△H>0,容器中A、B、D的物质的量浓度随时间的变化如图所示,下列说法不正确的是( )| A. | 反应在前10min的平均反应速率v(B)=0.15mol/(L•min) | |
| B. | 该反应的平衡常数表达式K=$\frac{{c}^{2}(D)}{c(A)•c(B)}$ | |
| C. | 若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动 | |
| D. | 反应至1.5min时,改变的反应条件是降低温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com