
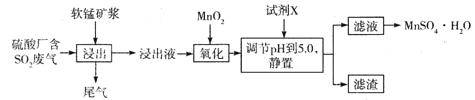

 Mn2++2Fe3++2H2O(2分) 得到的产品中含有FeSO4杂质(2分)
Mn2++2Fe3++2H2O(2分) 得到的产品中含有FeSO4杂质(2分) Mn2++2Fe3++2H2O; 得到的产品中含有FeSO4杂质
Mn2++2Fe3++2H2O; 得到的产品中含有FeSO4杂质

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.强酸性溶液中:K+、Al3+、CH3COO-、SO42- | ||
B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO
| ||
| C.室温下,pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl- | ||
| D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.在含有大量OH-的溶液中:NO3-、Na+、Cl-、AlO
| ||
| B.在强酸性溶液中:Na+、K+、CO32-、SO42- | ||
| C.在含有大量SO42-的无色溶液中:Mg2+、Na+、MnO4-、Cl- | ||
D.在含有大量Fe2+的溶液中:H+、Na+、Cl-、NO
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- |
| B.c(H+)=1×10-13mol/L的溶液:Na+、Ca2+、SO42-、CO32- |
| C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- |
| D.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由水电离产生的c(H+)=1×10-2mol?L-1溶液中,可能存在:CO32-、NH4+、Cl-,Na+ |
| B.某醋酸稀溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| C.Ba(OH)2溶液中加人过量的Al2(SO4)3溶液,其离子方程式为:3Ba2++60H-+2Al3++3SO42-=3BaS04↓+2Al(0H)3↓ |
| D.物质的量浓度均为1mol?L-1的NaCl和MgCl2混合液中,含有Cl-的数目为3NA(NA表示阿伏加德罗常数的值) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.011 mol/L | B.0.22 mol/L | C.0.022 mol/L | D.0.11 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质 |
| B.根据反应H3PO3+2NaOH(足量)===Na2HPO3+2H2O可知:H3PO3属于三元酸 |
| C.根据反应3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性 |
| D.根据反应CuSO4+H2S===CuS↓+H2SO4可知:H2S的酸性比H2SO4强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将Al条投入NaOH溶液中:Al+OH-+H2O=AlO2—+H2↑ |
| B.铜溶于稀硝酸中:Cu+4H++2NO3—=Cu2++2NO2↑+2H2O |
| C.碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO3—+OH-=CO32—+H2O |
| D.向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32—+CH3COOH=CH3COO-+HCO3— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.既能溶解Al(OH)3,又能溶解H2SiO3的溶液:Na+、Fe2+、SO42-、Cl- |
| B.能使酚酞溶液变红的溶液:Na+、NO3-、S2-、Br- |
| C.投入铁片能产生H2的无色溶液:H+、Mg2+、SO42-、NO3- |
| D.含有大量Fe3+的溶液:Na+、Al3+、NO3-、SCN- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com