
【题目】(1) 与氢气反应的化学方程式是__________;
与氢气反应的化学方程式是__________;
(2)写出正戊烷CH3(CH2)3CH3的两种同分异构体的结构简式和名称(系统命名法):
①结构简式:_____________、名称:_____________
②结构简式:_____________、名称:_____________。
(3)某一氯代烷烃分子中有2个“-CH3”、2个“-CH2-”、1个“ ”和1个“-Cl”,符合上述条件的有机物共四种,写出它们的结构简式:
”和1个“-Cl”,符合上述条件的有机物共四种,写出它们的结构简式:![]() 、
、 、_________、_________。
、_________、_________。
【答案】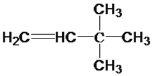 +H2
+H2![]() CH3CH2C(CH3)3 :CH3CH(CH3)CH2CH3 2-甲基丁烷 CH3C(CH3)3 2,2-二甲基丙烷 CH3CH2CHClCH2CH3 CH2ClCH(CH3)CH2CH3
CH3CH2C(CH3)3 :CH3CH(CH3)CH2CH3 2-甲基丁烷 CH3C(CH3)3 2,2-二甲基丙烷 CH3CH2CHClCH2CH3 CH2ClCH(CH3)CH2CH3
【解析】
(1)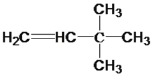 与氢气反应的化学方程式为:
与氢气反应的化学方程式为: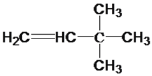 +H2
+H2![]() CH3CH2C(CH3)3。本小题答案为:
CH3CH2C(CH3)3。本小题答案为: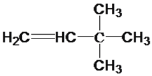 +H2
+H2![]() CH3CH2C(CH3)3。
CH3CH2C(CH3)3。
(2)戊烷有3种同分异构体,分别为CH3(CH2)3CH3、CH3CH(CH3)CH2CH3、CH3C(CH3)3。
①正戊烷的一种同分异构体为CH3CH(CH3)CH2CH3 ,名称为2-甲基丁烷。本小题答案为:CH3CH(CH3)CH2CH3 2-甲基丁烷。
②正戊烷的另外一种同分异构体为CH3C(CH3)3,名称为2,2-二甲基丙烷。本小题名称为:CH3C(CH3)3 2,2-二甲基丙烷。
(3)5个碳的烷烃碳骨架异构有①![]() ②
②![]() ③
③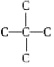 。①中的一氯代烃符合题意的有CH3CHClCH2CH2CH3、CH3CH2CHClCH2CH3两种;②中符合题意的有CH2ClCH(CH3)CH2CH3、(CH3)2CHCH2CH2Cl。③中没有符合题意的情况。本小题答案为: CH3CH2CHClCH2CH3 ;CH2ClCH(CH3)CH2CH3。
。①中的一氯代烃符合题意的有CH3CHClCH2CH2CH3、CH3CH2CHClCH2CH3两种;②中符合题意的有CH2ClCH(CH3)CH2CH3、(CH3)2CHCH2CH2Cl。③中没有符合题意的情况。本小题答案为: CH3CH2CHClCH2CH3 ;CH2ClCH(CH3)CH2CH3。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】将15.66g镁铝合金加入到800mL稀硝酸中,恰好完全反应(假设反应中还原产物只有NO),向所得溶液中加入足量的3mol·L-1NaOH溶液,测得生成沉淀的质量与原合金的质量相等,则下列有关叙述不正确的是
A. 原稀硝酸的浓度为2.6mol·L-1 B. 生成NO的体积为11.648L(标准状况)
C. 反应过程中共消耗1.56molNaOH D. 合金中Al的质量分数约为58.6%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示实验合理的是
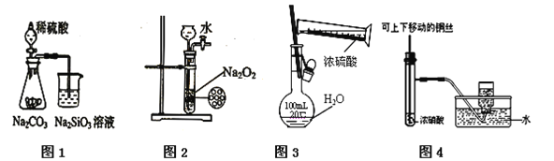
A. 图1为证明非金属性强弱:S > C > Si
B. 图2为制备少量氧气
C. 图3为配制一定物质的量浓度的硫酸溶液
D. 图4为制备并收集少量NO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定体积的酸性KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.2000 mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为( )
A.0.0176B.0.1600C.0.1200D.0.2400
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化变成绿色;见光分解变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl)生产CuCl的流程:
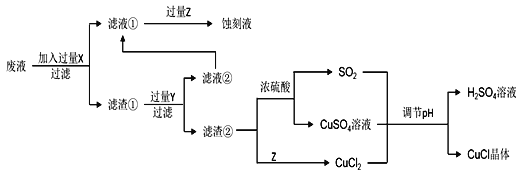
根据以上信息回答下列问题:
(1)生产过程中X的化学式为____。
(2)写出产生CuCl的离子方程式:____。
(3)实验探究pH对CuCl产率的影响如表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为____,当pH较大时CuCl产率变低原因是____。调节pH时,___(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是____。
(4)氯化亚铜的定量
①称取样品0.25g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10mol·L1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如表(平行实验结果相差不能超过1%):
平行实验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为_____。(结果保留三位有效数字)。
(5)由CuCl水解再热分解可得到纳米Cu2O。第一步CuCl水解的离子方程式为:CuCl(s)+H2O(l)![]() CuOH(s)+Cl (aq)+H+(aq),第二步CuOH热分解的化学方程式为____。第一步CuCl水解反应的平衡常数K与此温度下KW、Ksp(CuOH)、Ksp(CuCl)的关系为K=____。
CuOH(s)+Cl (aq)+H+(aq),第二步CuOH热分解的化学方程式为____。第一步CuCl水解反应的平衡常数K与此温度下KW、Ksp(CuOH)、Ksp(CuCl)的关系为K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4-CO2催化重整不仅可以得到合成气CO和H2,还对温室气体的减排具有重要意义。
已知:C(s)+2H2(g)=CH4(g) △H1 K1 C(s)+O2(g) =CO2(g) △H2 K2 ;C(s)+![]() O2(g) =CO(g) △H3 K3;CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H K(其中△H为焓变,K为平衡常数)下列说法正确的是
O2(g) =CO(g) △H3 K3;CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H K(其中△H为焓变,K为平衡常数)下列说法正确的是
A. △H=2△H3-2△H2-△H1
B. K=2K3-K2-K1
C. 若平衡时c(CH4):c(CO2):c(CO):c(H2)=1:1:1:1,则K一定等于1(mol/L)2
D. 减小压强可增大CH4(g)和CO2(g)的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资源化利用CO具有重要意义。
(1)CO可设计成燃料电池,熔融Li2CO3和Na2CO3的混合物作为燃料电池的电解质,氧化剂是含CO2的O2,工作时正极反应为__________________,以该燃料电池为电源处理含氮氧化物废气,可回收硝酸,同时制得副产物氢气,装置如图所示(电极均为石墨电极)。该装置中应选用_______(填“阴”或“阳”)离子交换膜,写出电解时NO2发生反应的电极反应式:___________________。

(2)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
反应 | △H(kJ/mol) |
I. Fe2O3(s)+3C(s) | +489 |
II. Fe2O3(s)+3CO(g) | -27 |
III. C(s)+CO2(g) | X |
试计算,试计算,X=_________。
T1℃时,向某恒温密闭容器中加入一定量的Fe2O3和C,发生反应I,反应达到平衡后,在t1时刻改变某条件,v(逆)随时间(t)的变化关系如图所示,则t1时刻改变的条件可能是_____________________。
a.保持温度、体积不变,使用催化剂 b.保持体积不变,升高温度
c.保持温度不变,压缩容器体积 d.保持温度、体积不变,充入CO

(3)在一定温度下,向某体积可变的恒压(P总)密闭容器中加入1mol CO2与足量的碳发生反应III,平衡时体系中气体体积分数与温度的关系如图所示。
①650℃时,反应达平衡后CO2的转化率为____________。
②T℃时,该反应达到平衡时下列说法不正确的是__________________。
a.气体密度保持不变
b.2v正(CO2)=v正(CO)
c.若保持其它条件不变再充入等体积的CO2和CO,平衡向逆反应方向移动
d.若保持其它条件不变再充入惰性气体,v正、v逆均减小,平衡不移动
e.若其它条件不变将容器体积压缩至一半并维持体积不变,再次达平衡时压强小于原平衡的2倍
③根据图中数据,计算反应III在T℃时用平衡分压代替平衡浓度表示的化学平衡常数KP=___________(设总压强为P总,用含P总的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月国际期刊eLife上发表了浙江医科大学第二医院和浙江大学肿瘤研究的晁明和胡汛等人的一片论文,引发轰动。媒体以廉价的小苏打协助饿死了癌细胞予以报道。在实验室中模拟工业制取NaHCO3的实验步骤如下:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让某一装置发生反应,直到产生的气体不能再在C中溶解,再通入另一装 置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:分离C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的某固体粉末,有NH4Cl晶体析出。
(1)下图所示装置的连接顺序是:a接______;_____接________;b接________(填接口编号)
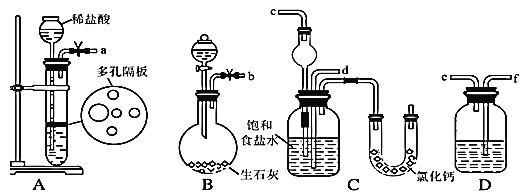
(2)检查A装置气密性的具体操作是___________。
(3)A中常选用的固体反应物为_________;D中应选用的液体为______。
(4)装有无水CaCl2的U形管的作用是 _______。
(5)第四步所得的晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单实验,不使用其他任何试剂,证明所得晶体大部分是NH4C1。简要写出操作和现象________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值,下列说法正确的是
A. 在标准状况下,11.2L HF含有的分子数目为0.5NA
B. 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子
C. 常温下,0.2 L 0.5 mol·L-1 NH4NO3溶液中含有的氮原子数小于0.2NA
D. 18g葡萄糖(C6H12O6)分子含有的羟基数目为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com