
����Ŀ��ʵ������Ҫ0.3mol/LNaOH��Һ480mL��������Һ����������ش��������⡣
��1����ͼ��ʾ������������Һ�����õ��IJ���������__(����������)��
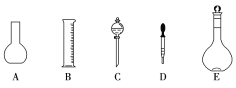
��2�����в����У�����ƿ�����߱��Ĺ�����___(�����)��
A������һ�����ȷŨ�ȵı���Һ
B��������Һ
C����������ƿ������µ����������Һ��
D��ȷϡ��ijһŨ�ȵ���Һ
E�����������ܽ��������
��3�����ݼ��㣬��������ƽ��ȡNaOH������Ϊ___g����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ���������ҺŨ��___(�ƫ�����䡱��ƫС����ͬ)����NaOH��Һ��ת��������ƿʱ����������������������ҺŨ��___��
���𰸡��ձ��Ͳ����� AD 6.0 ƫ�� ƫС
��������
(1)������Һ�����������ϸ�����������ѡȡ������
(2)�й�����ƿ�Ĺ����ʹ�ã�����ƿ����������һ��Ũ�ȵ���Һ��
(3)����m=cVM�����������Ƶ�������ע����Һ�����Ϊ500mL������480mL���м��㣬����c=![]() ��������ʵ����ʵ���n����Һ�����V�ı仯��������������
��������ʵ����ʵ���n����Һ�����V�ı仯��������������
(1)���Ʋ����м��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����һ����������ƽ��������ҩ��ȡ��ҩƷ�����ձ����ܽ�(������Ͳ��ȡˮ)����ȴ��ת�Ƶ�500mL����ƿ�У����ò���������������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�������Ҫ������Ϊ��������ƽ��ҩ�ס��ձ���Ͳ����������������ƿ����ͷ�ιܣ�������Ҫ��������BDE������Ҫ���������ձ��Ͳ�������
(2)A������ƿ��������һ������ġ�Ũ��ȷ����Һ����A��ȷ��
B������ƿֻ����������һ�����ȷŨ�ȵ���Һ����������������Һ����B����
C������ƿ�������ƻ��������ƿ������µ����������Һ�壬��C����
D������ƿ��ȷϡ��ijһŨ�ȵ���Һ����D��ȷ��
E������ƿֻ��һ���̶��ߣ��ʲ�����ȡһ�������Һ�壬��E����
F������ƿ�������ȣ��ʲ������������ܽ�������ʣ���F����
�ʴ�ΪAD��
(3)����n=c��V=0.3mol/L��0.5L=0.15mol��m=n��M��m=0.15mol��40g/mol=6.0g����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ�ʹ��������Һ�����ƫС����������ҺŨ�ȴ���0.3mol/L����NaOH��Һ��ת��������ƿʱ�����������������ʵ����ʵ���ƫС����������ҺŨ��С��0.3mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȼ�ϵ����CsHSO4����Ϊ����ʴ���H+��������ṹ����ͼ������ܷ�Ӧ�ɱ�ʾΪ��2H2+O2=2H2O�������й�˵����ȷ����
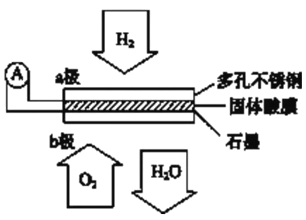
A. ����ͨ�����·��b������a��
B. b���ϵĵ缫��ӦʽΪ��O2+2H2O+4e--=4OH--
C. ÿת��0.1mol���ӣ�����1.12L��H2
D. H+��a��ͨ�����������ʴ��ݵ�b��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100 mL NaOH��Һ��ͨ��һ������CO2���壬��ַ�Ӧ������������Һ����μ���0.2 mol��L��1�����ᣬ����CO2������������������֮���ϵ��ͼ��ʾ�������ж���ȷ����(����)
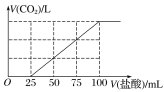
A. ԭNaOH��Һ��Ũ��Ϊ0.2 mol��L��1
B. ͨ��CO2�ڱ�״���µ����Ϊ448 mL
C. ������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaOH)��n(Na2CO3)��1��3
D. ������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaHCO3)��n(Na2CO3)��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C���ֻ������ȡ40g���ϣ���ȫ��Ӧ��������ֻ��18gB��49gC������D���ɣ���֪D����Է�������Ϊ106������˵���в���ȷ���ǣ� ��
A.��ѧ����ʽһ����A��B=C��D
B.����D�����ʵ���Ϊ0.5mol
C.����ѧ����ʽΪ2A��B=C��D����A��Ħ������Ϊ40g��mol��1
D.��D��̼���ƣ��������ӵ�����Ϊ23g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ���е����ʾ�������Ի�������ʽ���ڣ�Ϊ�˱����о������ã�����Ի������з�����ᴿ������A��B��C��D����ѧ�����Ļ���������ᴿ��װ�á�

I.����ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ������װ�á���A��B��C��D�����ʵ��Ŀո��С�
��1��̼�������Һ�з����̼���___��
��2���Ȼ�����Һ�з�����Ȼ���___��
��3������ֲ���ͺ�ˮ___��
��4����ˮ����___��
��5���ӵ�ˮ�з����I2___��
II.��ˮ����ȡ�ⵥ�ʵķ������£�
��1����ȡ��Һ
�����п���Ϊ��ˮ����ȡ�ⵥ����ȡ������___��
A���ƾ� B����
�ڷ�Һ©����ʹ��ǰ������___��
�۲����ϵ�֪������H2O��>��������>�����ƾ��������â�����ѡ��ȡ����ȡ��ˮ�еĵⵥ�ʣ���Һʱ��ˮ��Ӧ�ɷ�Һ©����___�˿ڷų����л���Ӧ�ɷ�Һ©����___�˿ڷų���������ϡ����ߡ��¡�����
��2������
��װ��A��a��������___������װ��������ˮӦ��___�ڽ�����ϡ����¡�������������Ŀ����___��
����֪������Ȼ�̼���۷е��������±�
�۵� | �е� | |
�� | 113.7�� | 184.3�� |
���Ȼ�̼ | -22.6�� | 76.8�� |
���������������Ȼ�̼�Ļ�����ƿ�����ռ��������ʵ�������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʯ��ˮ����500mL̼�����У����ˣ������õ�10g������
��1����̼������Һ�����ʵ���Ũ��___��
��2����ȡ����10g�����������м���������ϡ���ᣬ��ַ�Ӧ�������ղ����������ڱ�״���µ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϸ�۲�����2��װ�ã�����˵����ȷ����
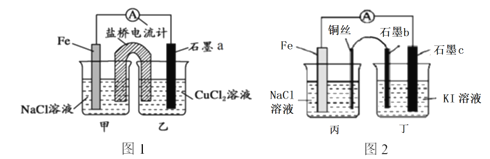
A. ͼ1ʯīaΪ������ͼ2ʯīcҲΪ����
B. ͼ1��ԭ���װ�ã����ŵ�������ʹ�������Һʼ�ձ��ֵ����ԣ����ṩ�����ȶ��ĵ�����ͼ2װ�ò����������
C. ͼ1ʯīa�缫�Ϸ����ķ�ӦΪ��O2��2H2O��4e��=4OH��
D. ͼ2ʯīb�ϵIJ�����ʹ������Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)��3B(g)![]() 2C(g)��2D(g)�����ֲ�ͬ����µķ�Ӧ�������£����б�ʾ��Ӧ����������
2C(g)��2D(g)�����ֲ�ͬ����µķ�Ӧ�������£����б�ʾ��Ӧ����������
A.v(A)��0.15 mol��L��1��min��1
B.v(B)��0.015 mol��L��1��s��1
C.v(C)��0.40 mol��L��1��min��1
D.v(D)��0.45 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3��
��1���ڸ÷�Ӧ����������___����ԭ����___��1Ħ��������ȫ���뷴Ӧ��ת�Ƶ�����Ŀ___��
��2����˫���ű���÷�Ӧ�ĵ���ת�Ʒ�����Ŀ_____________��4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3��
��3���÷�Ӧ���������������������������ǿ�����Ĺ�ϵ��__________��
��4����ҩ���й������Ĵ�����֮һ����Զֵ�������セ����Ҳ��Զ�ἤ��������ȥ�ܷ�ͼǿ���ڻ�ҩ�ڷ�����ըʱ���������µķ�Ӧ��2KNO3 + C��S = K2S + 2NO2�� + CO2�������б���ԭ��Ԫ����____����������Ԫ����____����������___����ԭ����____������������____����ԭ������_______ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com