
【题目】下列操作中,能使电离平衡H2O![]() H++OH-向右移动且溶液呈酸性的是
H++OH-向右移动且溶液呈酸性的是
A. 向水中加入NaHSO4溶液 B. 将水加热到100℃,使pH=6
C. 向水中加入Na2CO3溶液 D. 向水中加入Al2(SO4)3固体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用下列实验装置完成对应的实验,能达到实验目的的是
A. 制取并收集少量氨气 
B. 比较NaHCO3和Na2CO3的热稳定性
C. 制取并检验乙烯
D. 比较盐酸、碳酸、硅酸的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是2SO3(g)![]() 2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
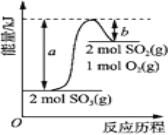
A. 该化学反应过程中既有能量的吸收又有能量的释放
B. 2SO3(g)![]() 2SO2(g)+O2(g) △H=-(a-b) kJ/mol
2SO2(g)+O2(g) △H=-(a-b) kJ/mol
C. 1 mol SO2的能量比1 mol SO3的能量高
D. 若某容器内有2 mol SO3充分反应,吸收(a-b) kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A. 1∶9 B. 1∶1 C. 1∶2 D. 1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。

回答下列问题:
(1)操作B是______________(填实验基本操作名称)。
(2)操作B需加入下列试剂中的一种,最合适的是_________。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)工业上制取金属镁时是电解熔MgCl2,电解反应方程式为_________________。
(4)上图中虚线框内流程的主要作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 3.0L0.1mol·L-1NaOH溶液中缓慢通入CO2至溶液增重8.8g时。溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B. 常温下,将CH3COONa溶液和盐酸混合至溶液pH=7:c(Na+)>c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)=c(OH-)
C. 常温下,pH=6的NaHSO3溶液中:c(SO32-)- c(H2SO3)=9.9×10-7mol·L-1
D. Ksp (Fe(OH)3)=1.0×10-38,Ksp (Mg(OH)2)=1.0×10-11,则浓度均为0.1 mol·L-1氯化铁、氯化镁混合溶液,若除去溶液中的Fe3+,应将pH调至3~11。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO3﹣、MnO4﹣
B.K+、Na+、Cl﹣、SO42﹣
C.K+、Na+、Br﹣、Cu2+
D.Na+、Ba2+、OH﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应:aA(g)+bB(g)![]() cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是
cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是
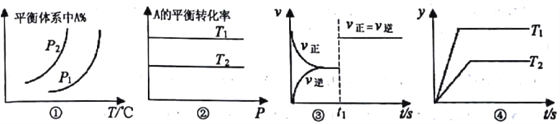
A. 图①中,若P1>P2,则该反应在较低温度下有利于自发进行
B. 图②中,若T2>T1,则△H<0 且a+b=c+d
C. 图③中t1时刻改变的条件一定是使用了催化剂
D. 图④中,若△H<0,则纵坐标不可能表示的是反应物的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com