
【题目】下表是元素周期表的一部分,用化学用语回答:
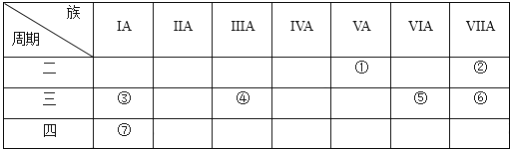
(1)②的元素符号为_________。
(2)比较元素③和⑦的原子半径大小:③_____⑦(填“>”或“<”)。
(3)绘出元素⑤的离子结构示意图_________________。
(4)元素①的氢化物的电子式为____________,将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为___________________________________。
【答案】 F < 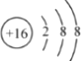
![]() Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+
Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+
【解析】根据元素在周期表中的位置可知,①为N元素,②为F元素,③为Na元素,④为Al元素,⑤为S元素,⑥为Cl元素,⑦为K元素。
(1)②的元素符号为F,故答案为:F;
(2)同一主族从上到下,原子半径逐渐增大,元素③和⑦的原子半径大小:③<⑦,故答案为:<;
(3)元素⑤为S元素,为16号元素,离子结构示意图为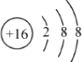 ,故答案为:
,故答案为: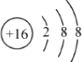 ;
;
(4)元素①的氢化物的电子式为![]() ,将氨气通入氯化铝的水溶液中,反应生成氢氧化铝沉淀,反应的离子方程式为Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+,故答案为:
,将氨气通入氯化铝的水溶液中,反应生成氢氧化铝沉淀,反应的离子方程式为Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+,故答案为:![]() ;Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+。
;Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对于反应CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下下列说法正确的是( )
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下下列说法正确的是( )
A. 加入催化剂,改变了反应的途径,反应的ΔH也随之改变
B. 改变压强,平衡不发生移动,反应放出的热量变大
C. 升高温度,反应速率加快,反应放出的热量不变
D. 增加反应物的浓度,反应速率加快,原因是单位体积内增加了活化分子的数目。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锰(MnCO3)常用于脱硫的催化剂。工业上利用软锰矿(主要成分是MnO2,还含有钙、铁、铝镁的氧化物及一些重金属的氧化物)制备无水碳酸锰的工艺流程如下:
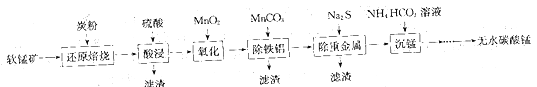
回答下列问题:
(1)为了提高“酸浸”步骤中原料的浸出率,可以采取的措施有___________(填字母)。
a.适当升温 b.连续搅拌 c.研磨矿石 d.加入足量的水
(2)“氧化”步骤中利用MnO2将溶液中Fe2+氧化为Fe3+,反应的离子方程式为_____________。
(3)“除铝铁”步骤中用MnCO3调节溶液pH的优点是___________________(写出一点),也可以用(填化学式)_____________代替MnCO3。
(4)“沉锰”步骤中反应温度需要控制在30~35℃以下,反应温度控制在35℃以下的原因是____,写出“沉锰”步骤中发生反应的化学方程式:________________________。
(5)25℃时,Ksp(MnCO3)=2.2×10-11,Ksp(MgCO3)=6.8×10-6。“沉锰”步骤中当Mn2+刚好沉淀完全[c(Mn2+)=1×10-5mol·L-1]时,若不析出MgCO3沉淀,则此时c(Mg2+)不能超过_____________mol·L-1(计算结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要除去碳酸氢钠溶液中混有的少量碳酸钠,最好采用
A.加入少量的澄清石灰水 B.加入适量的氢氧化钠溶液
C.将溶液加热蒸干并灼烧 D.通入足量的CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得
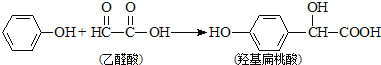
下列有关说法正确的是
A. 苯酚和羟基扁桃酸互为同系物
B. 标准状况下,22.4L羟基扁桃酸中共用电子对的数目为24NA
C. 乙醛酸只存在一种不同环境的氢原子
D. 羟基扁桃酸分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。

(1)在上图构想的物质和能量循环中太阳能最终转化为____________能。
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)![]() 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。
一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
①用CH3OH表示0~3 min内该反应的平均反应速率为______________________。
②能说明该反应已达到平衡状态的是_______________。
a.v正(H2O)=2v逆(CO2)
b.n(CH3OH) :n(O2)=2 :3
c.容器内密度保持不变
d.容器内压强保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的____极(填“正”或“负”),通入氧气的一极的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在标准状况下,1mol水的体积是22.4L
B.1molH2所占的体积一定是22.4L
C.在标准状况下,NA个任何分子所占的体积约为22.4L
D.在标准状况下,28g的N2体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.熔融状态下或在水溶液中能自身电离出自由移动的离子的化合物是电解质
B.凡是在水溶液里和熔化状态下都不能导电的物质叫非电解质
C.能导电的物质一定是电解质
D.某物质若不是电解质,就一定是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”就是因为酒在贮存过程中生成了有香味的乙酸乙酯。在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题。

(1)乙烯制取乙醇的化学方程式:__________________________。
(2)写出制取乙酸乙酯的化学反应方程式:________________________。
(3)浓硫酸的作用:_______________________________。
(4)饱和碳酸钠溶液的主要作用是________________________________________。
(5)装置中导管要在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是__________。
(6)若要把制得的乙酸乙酯分离出来,应该采用的实验操作是___________________。
(7)做此实验时,有时还要向盛有乙酸乙酯的试管里加入几块碎瓷片,其目的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com