
硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
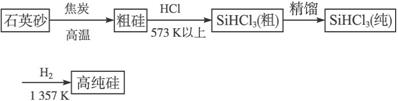
①写出由纯SiHCl3制备高纯硅的化学反应方程式____________________________。
②整个制备过程必须严格控制无水无氧。SiHCl3遇 水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式_________________;H2还原SiHCl3过程中若混入O2,可能引起的后果是_________________________。
水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式_________________;H2还原SiHCl3过程中若混入O2,可能引起的后果是_________________________。
(2)下列有关硅材料的说法正确的是__________________(填字母)。
A.碳化硅化学性质稳定,可用于生产耐高温水泥
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.高纯度的二氧化硅可用于制造高性能通讯材料——光导纤维
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。写出实验现象并给予解释__________________________ _____。
_____。
【答案】
(1)①SiHCl3+H2 Si+3HCl
Si+3HCl
②SiHCl3+3H2O H2SiO3+H2↑+3HCl 高温下,H2遇O2发生爆炸
H2SiO3+H2↑+3HCl 高温下,H2遇O2发生爆炸
(2)ABCD
(3)生成白色絮状沉淀,有刺激性气味的气体生成;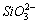 与
与 发生双水解反应,
发生双水解反应,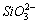 +2
+2 +2H2O
+2H2O 2NH3·H2O+H2SiO3↓
2NH3·H2O+H2SiO3↓
【解析】(2)SiC和Si3N4均为原子晶体,熔点高,性质稳定,A、B正确。光导纤维的材料为SiO2,C正确。普通玻璃的主要成分为Na2SiO3和CaSiO3,它是以石英砂(SiO2)、石灰石(CaCO3)和纯碱(Na2CO3)为主要原料反应制成的。Na2CO3+SiO2 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2 CaSiO3+CO2↑,D正确,常温下,Si只能与唯一一种酸HF反应不与HCl反应,E错。
CaSiO3+CO2↑,D正确,常温下,Si只能与唯一一种酸HF反应不与HCl反应,E错。


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
科研、生产中常涉及钠、硫及其化合物。
(1)实验室可用无水乙醇处理少量残留的金属钠,化学反应方程式为 。要清洗附着在试管壁上的硫,可用的试剂是 。
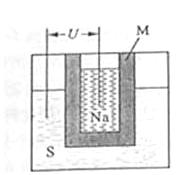
(2)下图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+ S=Na2
S=Na2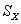 ,正极的电极反应式为 。M(由Na2O和Al2O3制得)的两个作用是 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
,正极的电极反应式为 。M(由Na2O和Al2O3制得)的两个作用是 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
(3)Na2S溶液中离子浓度由大到小的顺序为 ,向该溶液中加入少量固体CuSO4,溶液PH
(填“增大”“减小”或“不变”),Na2S溶液长期放置有硫析出,原因为 (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
O3和H2O2都是常见的氧化剂,下列有关说法错误的是( )
A.O3和O2互为同位素
B.O3和H2O2的分子内都含有共价键
C.H2O2具有氧化性,可以用于消毒杀菌
D.高空中的O3层保护人类免受紫外线 伤害
伤害
查看答案和解析>>
科目:高中化学 来源: 题型:
酸碱中和滴定常用于测定酸碱溶液的浓度。
(1)实验中,在正式测定前,常常用已知浓度的酸(或碱)滴定已知浓度的碱(或酸),测定滴定曲线,然后选择合适的指示剂指示滴定终点,以保证数据的准确性。如:用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.1 mol·L-1醋酸(CH3COOH)溶液,有关数据记录如下表:
|
| 0.00 | 10.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| 溶液pH | 2.87 | 4.74 | 5.70 | 6.74 | 7.74 | 8.72 | 9.70 | 10.70 | 11.70 | 12.50 |
①根据上表数据在下图中绘制0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.1 mol·L-1醋酸(CH3COOH)溶液的滴定曲线。
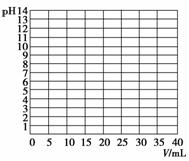
②根据你所绘制的曲线,确定pH的突变范围是______。
③下列指示剂中适合于本实验的是________。
A.甲基橙 B.石蕊 C.酚酞
(2)用酸式滴定管准确量取0.1 mol·L-1的醋酸溶液。在调节酸式滴定管的起始读数时,要使滴定管的尖嘴部分充满醋酸,如果滴定管内部有气泡,赶走气泡的操作是________。
(3)滴定过程中,眼睛应重点观察________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于ⅣA族元素,下列叙述中不正确的是
A.SiO2和CO2中,Si和O,C和O之间都是共价键
B.C、Si和Ge的最外层电子数都是4,次外层电子数都是8
C.CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应
D.该族元素的主要化合价是+4和+2
查看答案和解析>>
科目:高中化学 来源: 题型:
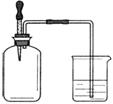
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是
①CO、O2 ②Cl2、CH4 ③NO2、O2 ④N2、H2
A.①② B.②④
C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的下列化合物在相应条件下完全分解后得到氧气最多的是
A.KClO3(加MnO2催化剂,加热) B.KMnO4(加热)
C.H2O2(水溶液,加MnO2催化剂) D.HgO(加热)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上对海水资源综合开发利用的部分工艺流程如下图所示。

(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽。离子膜和隔膜均允许通过的分子或离子是______________。电解槽中的阳极材料为__________________。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2和CaSO4的顺序制备?______________________原因是______________________。
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
近期,北京大学的两位教授率先发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用。下列叙述正确的是( )
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外电子层都达到8电子结构
C.将硫化氢通入溴水,溴水褪色
D.硫化氢是电解质,其电离方程式是H2S===2H++S2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com