
将KClO3、I2各0.02 mol加入12 g 36.5%的盐酸中,I2恰好完全溶解,没有气体产生(不考虑盐酸的挥发)。将反应后的溶液用冰水冷却,析出橙红色晶体A(A在常温下就有升华现象),将过滤后的溶液蒸干,收集到KCl固体、8.7g液态水和极少量的A蒸气。则A的化学式可能是
| A.IClO | B.ICl3 | C.I2Cl6 | D.KIO3 |
科目:高中化学 来源: 题型:单选题
一定条件下,向含HNO3的废水中加入CH3OH进行污水处理,发生反应
 下列说法正确的是
下列说法正确的是
| A.CH3OH被氧化,表现氧化性 |
| B.此条件下还原性强弱为:N2>CH3OH |
| C.若氧化产物比还原产物多0.2 mol,则该反应中转移3 mole- |
| D.该反应过程中断裂的化学键既有极性键又有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
制备Fe3O4纳米颗粒的总反应如下:3Fe2++ 2S2O32-+O2+4OH-= Fe3O4 + S4O62-+2H2O。下列说法正确的是
| A.当转移1mol电子时,消耗56g S2O32- |
| B.在反应中硫元素被氧化,铁元素被还原 |
| C.还原剂是Fe2+,氧化剂是S2O32-和O2 |
| D.每生成1mol Fe3O4,转移3mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )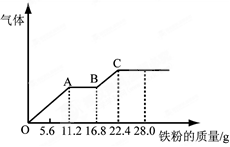
| A.H2SO4浓度为2.5 mol·L-1 |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.混合酸中NO3-物质的量为0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
往AgNO3、Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,发现有少量金属析出,过滤后往滤液中滴加盐酸有白色沉淀生成,则析出的少量金属一定是
| A.Ag | B.Cu | C.Fe | D.Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学工业是国民经济的支柱产业,下列生产过程中不涉及氧化还原反应的是
| A.氮肥厂用氮气和氢气合成氨气 | B.硝酸厂用氨氧化法制硝酸 |
| C.从海水中提溴 | D.纯碱厂用NaCl、NH3、CO2等制纯碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A.浓硫酸的质量增加 | B.铝的表面生成致密的氧化物薄膜 |
| C.澄清的石灰水变浑浊 | D.氢氧化钠固体发生潮解 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。湿法制备的离子反应方程式: 2Fe(OH)3+3ClO-+4OH-→ 2FeO42-+3Cl-+5H2O;干法制备化学反应方程式:2FeSO4+4Na2O2→2Na2FeO4+2Na2SO4。有关分析错误的是
| A.等物质的量Na2FeO4氧化能力优于次氯酸钠 |
| B.湿法中氢氧化铁被氧化 |
| C.干法中每生成1 mol Na2FeO4转移3 mol电子 |
| D.高铁酸钠的氧化性大于次氯酸钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com