
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,违反了泡利原理的是___________,违反了洪特规则的是__________。
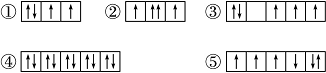
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为____________________;其最高价氧化物对应水化物的化学式是_____________。
(3)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na______Mg,Mg______Ca。
②电负性:O______F,F______Cl。
③能量高低:ns______(n+1)s, ns______np。
(1)②; ③⑤
(2)1s22s22p63s23p4 H2SO4
(3)①< > ②< > ③< <
解析:(1)同一个原子轨道中不应有自旋状态相同的电子,②违反了泡利原理;对于基态原子,电子在能量相同的轨道上排布时,将尽可能分占不同的轨道并且自旋状态相同,③⑤违反了洪特规则。
(2)3p能量小于3d,激发态为1s22s22p63s13p33d2,基态应为1s22s22p63s23p4。此原子核外电子数为16,其质子数也为16,该元素为硫元素,其最高价氧化物对应水化物的化学式是H2SO4。(3)同周期中主族元素从左到右第一电离能有增大的趋势,电负性逐渐增大;同主族中自上而下电负性与第一电离能均逐渐减小。由构造原理可知,能量ns<(n+1)s,ns<np。


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
下列叙述与图像对应符合的是
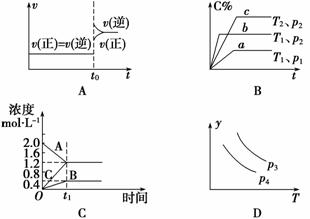
A.对于达到平衡状态的N2(g)+3H2(g)2NH3(g)在t0时刻充入了一定量的NH3,平衡逆向移动
B.p2>p1,T1>T2
C.该图像表示的化学方程式为:2A===B+3C
D.对于反应2X(g)+3Y(g)  2Z(g) ΔH<0,y可以表示Y的百分含量
2Z(g) ΔH<0,y可以表示Y的百分含量
查看答案和解析>>
科目:高中化学 来源: 题型:
生活中使用的购物袋的材料多为聚乙烯,工农业生产中使用的塑料也是聚乙烯制品。下列有关说法正确的是( )
A.聚乙烯的单体能够使溴的四氯化碳溶液褪色
B.聚乙烯可以人工合成,也可以是天然高分子化合物
C.聚乙烯高温分解,生成其单体——乙烯
D.用纯净的乙烯合成的聚乙烯是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
A.SO2和SiO2 B.CCl4和KCl C.NaCl和HCl D.CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
简单原子的原子结构可用下图形象地表示:
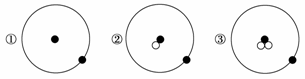
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( )
a.①②③互为同位素 b.①②③互为同素异形体
c.①②③是三种化学性质不同的粒子 d.①②③具有相同的质量数
e.①②③具有相同的质量 f.①②③是三种不同的原子
A.a、f B.b、c C.d、e D.e、f
查看答案和解析>>
科目:高中化学 来源: 题型:
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )
A.正极反应为:O2+2H2O+4e-===4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,不正确的是
A.某特定反应的平衡常数仅是温度的函数
B.催化剂不能改变平衡常数的大小
C.平衡常数发生变化,化学平衡不一定发生移动
D.化学平衡发生移动,平衡常数不一定发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
[实验一] 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题。
mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题。
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、________和 ________。
________。
(2)为标定某醋酸溶液的准确浓度,用0.200 0 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液 的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
则该醋酸溶液的准确浓度为________ (保留小数点后四位)。
(保留小数点后四位)。
[实验二] 探究浓度对醋酸电离程度的影响
用pH计测定25 ℃时不同浓度的醋酸的pH,结果如下:
| 醋酸浓度 (mol·L-1) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:__________________________________ _
_ _____________________________________。
_____________________________________。
(2)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将________(填“增大”、“减小”或“不变”)。
[实验三] 探究温度对醋酸电离程度的影响
请你设计一个实验完成该探究,请简述你的实验方案:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com