
����Ŀ���������ң���Ҫ�ɷ�ΪAl��Al2O3��AlN��FeO�ȣ��Ʊ�������[��Ҫ�ɷ�ΪAl��OH2Cl��]��һ�ֹ������£� 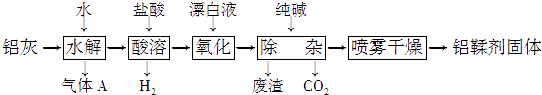
��1������A��ʹʪ��ĺ�ɫʯ����ֽ������������90��ˮ������A�Ļ�ѧ����ʽΪ����ˮ�⡱����90������������½��е�ԭ���� ��
��2�������ܡ�ʱ��Al2O3������Ӧ�����ӷ���Ϊ ��
��3����������ʱ��������Ӧ�����ӷ���ʽΪ ��
��4�����������ɷ�Ϊ���ѧʽ����
��5�������������������������ԭ���� ��
��6������������茶��壬��������Ҫ��Ӧ�ǣ�4[NH4Al��SO4��212H2O] ![]() 2Al2O3+2NH3��+N2��+5SO3��+3SO2��+53H2O��������������ͨ����ͼ��ʾ��װ�ã���
2Al2O3+2NH3��+N2��+5SO3��+3SO2��+53H2O��������������ͨ����ͼ��ʾ��װ�ã���
�ټ���ƿ���ռ��������������ѧʽ����
����������NaHSO3��Һ���յ����ʳ���H2O��g��������ѧʽ��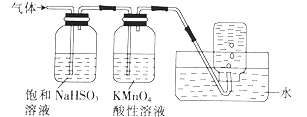
���𰸡�
��1��+3H2O ![]() ?Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ�
?Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ�
��2��Al2O3+6H+�T2Al3++3H2O
��3��2Fe2++2H++ClO���T2Fe3++Cl��+H2O
��4��Fe��OH��3
��5����ֹAl��OH��2Clˮ������Al��OH��3
��6��N2��NH3��SO3
���������⣺������Ҫ�ɷ�ΪAl��Al2O3��AlN��FeO�ȼ���ˮ������Ӧ��AlN��ˮ��Ӧ�������������Ͱ����������������ܺ������Ȼ�����Һ���Ȼ�������Һ������Ư��������������Ϊ�����ӣ����봿�������ҺPHʹ������ȫ���������������������Ʊ���������
��1.������A��ʹʪ��ĺ�ɫʯ����ֽ������˵�����ɵ��ǰ����������е�AlN��ˮ����ˮ�ⷴӦ�����������������Ͱ�������Ӧ�Ļ�ѧ����ʽΪ��AlN+3H2O ![]() Al��OH��3+NH3�������ȿ��Դٽ�������ˮ�����ɰ���������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ������Դ��ǣ�+3H2O
Al��OH��3+NH3�������ȿ��Դٽ�������ˮ�����ɰ���������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ������Դ��ǣ�+3H2O ![]() Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ���
Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ���
��2.������������������������ʱ�����ᷢ����Ӧ�����Ȼ�����Һ���������ܡ�ʱ��Al2O3������Ӧ�����ӷ���ʽΪ��Al2O3+6H+�T2Al3++3H2O�����Դ��ǣ�Al2O3+6H+�T2Al3++3H2O��
��3.������Ư��Һ�����������ô����������������Һ�е�ǿ������������������Ϊ�����ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++2H++ClO���T2Fe3++Cl��+H2O�����Դ��ǣ�2Fe2++2H++ClO���T2Fe3++Cl��+H2O��
��4.������������֪���������ɷ�Ϊ����������������ѧʽΪ��Fe��OH��3 �� ���Դ��ǣ�Fe��OH��3��
��5.����������Ҫ�ɷ�ΪAl��OH��2Cl���ڼ�������ʱ�ᷢ��ˮ�⣬Ϊ��ֹˮ�����������������������ˮ�⣬���Դ��ǣ���ֹAl��OH��2Clˮ������Al��OH��3��
��6.�������������У��������������ƿ����հ���������������������ն�������������յ��������Դ��ǣ�N2����NH3��SO3�ܹ������������Ʒ�Ӧ��������������NaHSO3��Һ���յ����ʳ���H2O��g�����NH3��SO3 ��
���Դ��ǣ�NH3��SO3 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᣨ��ʽ�е�A����ij�ֿ��������ɷ�֮һ��A��FeCl3��Һ��Ӧ����ɫ�� 
��1���������к��������ŵ�����Ϊ ��
��2����������Է����ķ�Ӧ������д��ţ�����������Ӧ �ڼӳɷ�Ӧ ��������Ӧ �ܼӾ۷�Ӧ ����ȥ��Ӧ
��3��������ɿ���1��3��4����ȡ����������������ͬ�Ĺ�����λ����λ��ȡ�����в���֧��������Ľṹ��ʽΪ ��
��4��3.6g������������̼�����Ʒ�Ӧ�������壨��״����mL��
��5���佺����Ҫ���Գɷ�ΪCPAE������ʽΪC17H16O4 �� ��������һ�������¿�ˮ�����ɿ������һ�ִ����ô�Ϊ���㴼���ҷ��ӽṹ������������÷��㴼��һ�������·�Ӧ����CPAE�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϵIJ��Ϸ�չ���Դٽ����Ľ����� �١��칬���š��ڴ���ʹ����̼��ά���ϲ��ϣ���̼��ά���ϲ����У�̼��ά���������ǿ���ϡ�������ϡ�������Դ�մ���������﮺Ͻ�ѡ����﮺Ͻ����ѡ�����Ͻ����Ҫԭ���� ��
�ڡ��칬���š��˿�ϵͳʹ���ͷ���ʯӢ������Ϊ��ѧ���ϣ�ʯӢ������Ҫ�ɷֵĻ�ѧʽΪ ��
�۾���ϩ���ϳ�����ʳƷ��װ������ϩ�Ľṹ��ʽΪ �� ����ϩ������������ȹ��ԡ��������ԡ������ϣ�
��2015��ij�о�������һ���²�����������������������������̼�������ڼ���������ת��Ϊ���飬�÷�Ӧ�Ļ�ѧ����ʽΪ �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ϩ�;���ϩ����������ȷ���ǣ� ��
A.���߶���ʹ��ˮ��ɫ
B.����Ϊͬϵ��
C.�������ʽ��ͬ
D.����ʽ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�д��ڽ϶��H����SO42����NO3���������Һ�л����ܴ������ڵ���������
A. Mg2+��NH4+��Cl�� B. Mg2+��Ba2+��Br��
C. Na+��Cl����I�� D. Al3+��HCO3����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�������п��γ�˳���칹���ǣ� ��
A.CH3CH=CHBr
B.CH3��Cl
C.CH3CH=CH2
D.CH3CH=C��CH3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ú������ʣ�FeO��Fe2O3���ķ�CuO�Ʊ��������壬���������й��̣���֪ Fe3+�� pH=5ʱ������ȫ�������з���������ǣ� �� 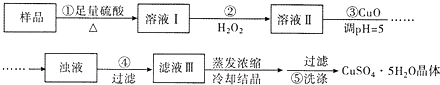
A.����ڷ�������Ҫ��ӦΪ��2Fe2++H2O2+2H+=2Fe3++2H2O
B.����ڿ�����ˮ�������ǿ����������H2O2
C.������� CuCO3����CuOҲ�ɵ�����Һ��pH
D.����ݵIJ���Ϊ����©���м��������������ˮ����û���壬��ˮ��Ȼ���£��ظ����� 2��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС��Թ���̿������������Ӧ���������ɷֽ����о���
��1���������
�ٸ÷�Ӧ�����������CO2 ��
�ڸ÷�Ӧ�����������CO��
�۸÷�Ӧ����������� ��
��2����Ʒ���
��ͼ��ʾ����һ�������������ڸ��������������������̿����ȫ��Ӧ���ⶨ�μӷ�Ӧ��̼Ԫ������Ԫ�ص������ȣ�
��������
��������̼��������������Ӧ��ʵ���ҿ������Ȼ�隣�����Һ���������ƣ�NaNO2��������Һ��ϼ��ȷ�Ӧ�Ƶõ�������д���÷�Ӧ�����ӷ���ʽ�� ��
��3��ʵ�鲽��
�ٰ�ͼ����װ�ã������װ�õ������ԣ���ȡ3.20g��������2.00g̼�ۻ�Ͼ��ȣ�����48.48g��Ӳ�ʲ������У�
�ڼ���ǰ����ͨһ��ʱ�䴿������ĵ�����
��ֹͣͨ��N2�н����ɼУ�����һ��ʱ�䣬����ʯ��ˮ������������ǣ�
�ܴ���Ӧ�������ٻ���ͨ��һ��ʱ��ĵ�������ȴ�����£��Ƶ�Ӳ�ʲ����ܺ���������Ϊ52.24g��
�ݹ��˳�ʯ��ˮ�еij�����ϴ�ӡ���ɺ�Ƶ�����Ϊ2.00g��
����ڡ����ж��ֱ�ͨ��N2 �� �����÷ֱ�Ϊ ��
��4�����ݴ���
�Ը���ʵ�����ݷ�����д����ʵ������������̼������Ӧ�Ļ�ѧ����ʽ�� ��
��5��ʵ���Ż�
ѧϰС����ͬѧ��ΪӦ��ʵ��װ�ý�һ�����ƣ�
�ټ�ͬѧ��Ϊ��Ӧ������ʯ��ˮ����Ba��OH��2��Һ���������� ��
�ڴӻ��������ĽǶȣ����������һ���Ż���������ʵ��װ�ý�һ�����ƣ� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com