
【题目】化合物H具有似龙延香、琥珀香气息,香气淡而持久,广泛用作香精的稀释剂和定香剂.合成它的一种路线如图:
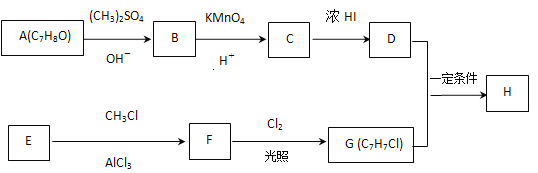
已知以信息:
①![]() ;
;
②核磁共振氢谱显示A的苯环上有四种化学环境不同的氢原子,且取代基的位置相邻;
③在D中滴加几滴FeCl3溶液,溶液呈紫色;
④芳香烃 F的相对分子质量介于90~100之间,0.1 mol F充分燃烧可生成7.2 g水;
⑤R1COOH+RCH2Cl![]() R1COOCH2R+HCl。
R1COOCH2R+HCl。
回答下列问题:
(1)A的化学名称是____,由C生成D的反应的化学方程式为______________。
(2)由F生成G的反应的化学方程式为____________,反应类型为____。
(3)H的结构简式为_________。
(4)苯环上有三个取代基且其中两个与A中所含的官能团相同,同时又能发生银镜反应的C的同分异构体有 (不考虑立体异构)_____种,其中核磁共振氢谱中有5组峰,且峰面积之比为1∶2∶2∶2∶1的同分异构体的结构简式是________(任写一种即可)。
(5)由苯酚和已有的信息经以下步骤可以合成化合物
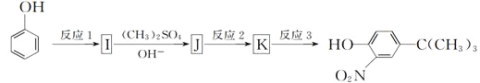
反应1所用的试剂为___,K的结构简式为____,反应3所用的试剂为___。
【答案】2-甲基苯酚(或邻甲苯酚) 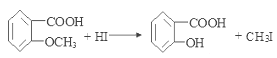
![]() 取代反应
取代反应 ![]() 6
6 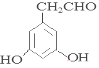 、
、 C(CH3)3CCl/AlCl3
C(CH3)3CCl/AlCl3 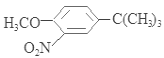 浓HI
浓HI
【解析】
本题是有机物的合成题。核磁共振氢谱显示A苯环上有四种化学环境的氢,且取代基的位置相邻,结合A的分子式及信息反应①可知A为邻甲基苯酚: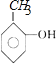 ;A发生信息反应①生成B,则B为
;A发生信息反应①生成B,则B为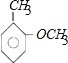 ;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为
;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为![]() ;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为:
;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为:![]() ;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:
;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:![]() ,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯:
,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯:![]() ,故G为:
,故G为:![]() ;E与一氯甲烷在氯化铝存在条件下反应生成F,则E为
;E与一氯甲烷在氯化铝存在条件下反应生成F,则E为![]() ;D和G按照信息⑤反应生成H,则H为:
;D和G按照信息⑤反应生成H,则H为: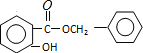 ,据此进行解答.
,据此进行解答.
核磁共振氢谱显示A的苯环上有四种化学环境不同的氢原子,且取代基的位置相邻,结合A的分子式及信息反应①可知A为邻甲基苯酚: ;A发生信息反应①生成B,则B为
;A发生信息反应①生成B,则B为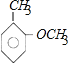 ;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为:
;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为:![]() ;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为:
;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为:![]() ;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:
;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:![]() ,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯:
,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯:![]() ,故G为:
,故G为:![]() ;E与一氯甲烷反应生成F,则E为
;E与一氯甲烷反应生成F,则E为![]() ;D和G按照信息⑤反应生成H,则H为:
;D和G按照信息⑤反应生成H,则H为: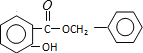 。
。
(1)A的结构简式为 ,其名称为2-甲基苯酚;由C生成D的化学方程式为:
,其名称为2-甲基苯酚;由C生成D的化学方程式为: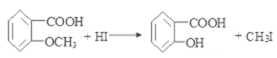 。本小题答案为:2-甲基苯酚(或邻甲苯酚);
。本小题答案为:2-甲基苯酚(或邻甲苯酚); 。
。
(2)F为甲苯:![]() ,甲苯在光照条件下与氯气发生取代反应生成
,甲苯在光照条件下与氯气发生取代反应生成![]() ,反应的化学方程式为
,反应的化学方程式为![]() 。本小题答案为:
。本小题答案为:![]() ;取代反应。
;取代反应。
(3)根据分析可知,H的结构简式为:![]() 。本小题答案为:;
。本小题答案为:;![]() 。
。
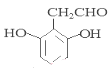
(4)C为![]() ,其同分异构体中含有三取代苯结构和两个A中的官能团,A中官能团为酚羟基,说明该有机物分子中含有两个羟基;又可发生银镜反应,其分子中一定含有醛基,所以满足条件的C的同分异构体中含有2个酚羟基、1个-CH2CHO,①当3个取代基都相邻时,中间为羟基或醛基,有2种结构;②当两个羟基相邻时,存在1种结构;③当1个羟基与-CH2CHO相邻时,另一个羟基可以在间位,有2种结构;④3个取代基都不相邻时有1种结构,所以总共存在6种同分异构体;其中核磁共振氢谱为5组峰,且面积比为1:2:2:2:1,该有机物分子中含有5种H原子,且具有一定的对称结构,满足条件的有机物的结构简式为:
,其同分异构体中含有三取代苯结构和两个A中的官能团,A中官能团为酚羟基,说明该有机物分子中含有两个羟基;又可发生银镜反应,其分子中一定含有醛基,所以满足条件的C的同分异构体中含有2个酚羟基、1个-CH2CHO,①当3个取代基都相邻时,中间为羟基或醛基,有2种结构;②当两个羟基相邻时,存在1种结构;③当1个羟基与-CH2CHO相邻时,另一个羟基可以在间位,有2种结构;④3个取代基都不相邻时有1种结构,所以总共存在6种同分异构体;其中核磁共振氢谱为5组峰,且面积比为1:2:2:2:1,该有机物分子中含有5种H原子,且具有一定的对称结构,满足条件的有机物的结构简式为: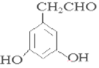 或
或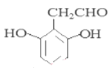 。本小题答案为:6;
。本小题答案为:6; (或
(或 )。
)。
(5)根据初始原料苯酚、最终产物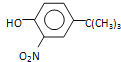 可知,反应过程中需要引进硝基、-C(CH3)3,结合信息反应可知,I转化成J是为了保护酚羟基,反应1中一定引进了-C(CH3)3,所以反应条件1为(CH3)3CCl/AlCl3,I为
可知,反应过程中需要引进硝基、-C(CH3)3,结合信息反应可知,I转化成J是为了保护酚羟基,反应1中一定引进了-C(CH3)3,所以反应条件1为(CH3)3CCl/AlCl3,I为![]() ;再利用逆推法,反应条件3应该为将酚羟基还原,则K为
;再利用逆推法,反应条件3应该为将酚羟基还原,则K为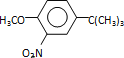 ,反应条件3为浓HI;反应2通过硝化反应引进硝基。本小题答案为:(CH3)3CCl/AlCl3;C(CH3)3CCl/AlCl3 ;
,反应条件3为浓HI;反应2通过硝化反应引进硝基。本小题答案为:(CH3)3CCl/AlCl3;C(CH3)3CCl/AlCl3 ; 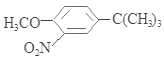 ;浓HI。
;浓HI。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如右图所示。下列说法不正确的是

A. 该反应的化学方程式为5A+4B![]() 4C
4C
B. 2min前,正反应速率逐渐减小,逆反应速率逐渐增大
C. 用B的浓度变化表示2min内的速率为2mol/(L·min)
D. 2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 某可逆反应在某体积为2L的密闭容器中进行,在从0~3min各物质的量的变化情况如图所示(A、B、C均为气体)。

(1)该反应的化学方程式为______。
(2)反应开始至2min时,B的平均反应速率为______。
(3)能说明该反应已达到平衡状态的是______。
A. c(A)= c(B)= c(C) B.容器内压强保持不变
C .v逆(A)= v正(C) D. c(C)不再变化
(4)由图求得A的平衡时的转化率为______。
Ⅱ.(5)已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表
共价键 | H—H | N—H | N≡N |
能量变化/kJ·mol-1 | a | b | c |
则合成氨反应:N2(g) + 3H2 (g)= 2NH3(g) ![]() H = ______kJ·mol-1
H = ______kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。

(1)X的转化率是______;
(2)由图中所给数据进行分析,该反应的化学方程式为______;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________;
(4)当反应进行到第____min,该反应是达到平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )

A. 先a通入CO2,然后b通入NH3,c中放碱石灰
B. 先b通入NH3,然后a通入CO2,c中放碱石灰
C. 先a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. 先b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是

A. 该装置将化学能转化为电能
B. 催化剂b表面O2发生还原反应,其附近酸性增强
C. 催化剂a表面的反应是:SO2+2H2O-2e-===SO42-+4H+
D. 若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO2(红棕色)![]() N2O4(无色),分别进行如下两个实验:
N2O4(无色),分别进行如下两个实验:
实验ⅰ:将NO2球分别浸泡在热水和冰水中,现象如图1。
实验ⅱ:将一定量的NO2充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),如图2。下列说法不正确的是

A. 图1现象说明该反应为放热反应
B. 图2中b点的操作是压缩注射器
C. c点:v(正)>v(逆)
D. 若不忽略体系温度变化,且没有能量损失,则T(d)<T(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量且足量的两份锌a、b,分别加入等量的稀H2SO4,同时向a中加入少量的CuSO4溶液,下列各图表示产生H2的体积(V)与时间(t)的关系,其中正确的是 ( )
A. 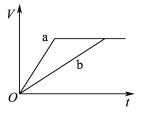 B.
B. 
C. 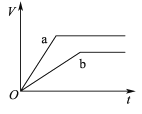 D.
D. 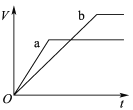
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钪(Sc)及其化合物在电子、宇航、超导等方面有着广泛的应用。某工厂的钛白水解工业废酸中,Sc3+浓度为18mg/L,还含有大量的TiO2+、Fe3+、H+、SO42-等。下图为从该工业废酸中提取Sc2O3的一种流程。

回答下列问题:
(1)在钛白水解工业废酸中,加入双氧水是为了使TiO2+转化为难萃取的[Ti(O2)(OH(H2O)4]+。[Ti(O2)(OH(H2O)4]+中Ti的化合价为+4,其中非极性键的数目为_______。
(2)钪的萃取率(E%)与O/A值[萃取剂体积(O)和废酸液体积(A)之比]的关系如左下图,应选择的最佳O/A值为_______;温度对钪、钛的萃取率影响情况见右下表,合适的萃取温度为10-15℃,其理由是_____________________。

(3)洗涤“油相“可除去大量的钛离子。洗染水是用浓硫酸、双氧水和水按一定比例混合而成。混合过程的实验操作为________________。
(4)25℃时,用氨水调节滤液的pH,当pH=3.5时,滤渣II的主要成分是_______;当pH=6时,滤液中Sc3+的浓度为________。(Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(5)写出用草酸(H2C2O4)“沉钪”得到Sc2(C2O4)3的离子方程式_____________。
(6)若从1m3该工厂的钛白水解度酸中提取得到24.4gSc2O3,则钪的提取率为______(保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com