
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )

A. 先a通入CO2,然后b通入NH3,c中放碱石灰
B. 先b通入NH3,然后a通入CO2,c中放碱石灰
C. 先a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. 先b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】已知常温时HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4。现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
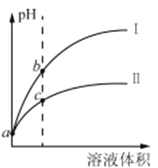
A. 曲线I为次氯酸稀释时pH变化曲线
B. 取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗次氯酸的体积较小
C. a点时,若都加入相同大小的锌粒,此时与氢氟酸反应的速率大
D. b点溶液中水的电离程度比c点溶液中水的电离程度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是( )
A. 用Fe电极电解NaCl溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B. 四氧化三铁溶于氢碘酸:Fe3O4+8H+ +2I-=3Fe2+ +4H20+I2
C. 碳酸氢钠溶液中加入足量澄清石灰水:Ca2++OH-+HCO3-=CaCO3↓+H2O
D. 硫酸氢钠溶液与氢氧化钡溶液混合显中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中进行反应:3H2(g) + N2(g)![]() 2NH3(g),经过一段时间后,NH3物质的量增加0.8 mol,这段时间内用N2表示的平均反应速率为0.01 mol·L-1·s-1。则这段时间为
2NH3(g),经过一段时间后,NH3物质的量增加0.8 mol,这段时间内用N2表示的平均反应速率为0.01 mol·L-1·s-1。则这段时间为
A. 10 sB. 20 sC. 30 sD. 40 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,不能通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)已知2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
![]()
反应②的化学方程式为____________________________________。工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为_______________,反应类型是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H具有似龙延香、琥珀香气息,香气淡而持久,广泛用作香精的稀释剂和定香剂.合成它的一种路线如图:
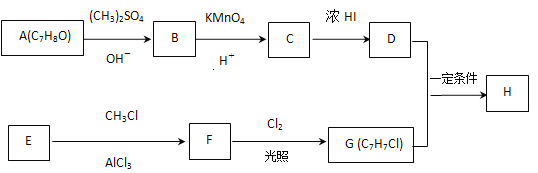
已知以信息:
①![]() ;
;
②核磁共振氢谱显示A的苯环上有四种化学环境不同的氢原子,且取代基的位置相邻;
③在D中滴加几滴FeCl3溶液,溶液呈紫色;
④芳香烃 F的相对分子质量介于90~100之间,0.1 mol F充分燃烧可生成7.2 g水;
⑤R1COOH+RCH2Cl![]() R1COOCH2R+HCl。
R1COOCH2R+HCl。
回答下列问题:
(1)A的化学名称是____,由C生成D的反应的化学方程式为______________。
(2)由F生成G的反应的化学方程式为____________,反应类型为____。
(3)H的结构简式为_________。
(4)苯环上有三个取代基且其中两个与A中所含的官能团相同,同时又能发生银镜反应的C的同分异构体有 (不考虑立体异构)_____种,其中核磁共振氢谱中有5组峰,且峰面积之比为1∶2∶2∶2∶1的同分异构体的结构简式是________(任写一种即可)。
(5)由苯酚和已有的信息经以下步骤可以合成化合物
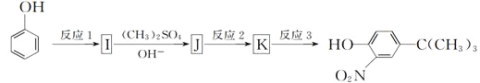
反应1所用的试剂为___,K的结构简式为____,反应3所用的试剂为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元索M、N、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系。甲、丁为二元化合物(两种元素形成的化合物),乙、戊为单质,丙、己为三元化合物。已知25℃时,0.1mol/L的甲、丙两溶液的pH分别为l、13 ,丁、己两溶液混合时产生白色沉淀。下列推断正确的是

A. M分别与N、X、Z形成的简单化合物中,M与N形成的化合物熔点最高
B. 原子半径:Z>Y>X>M>N
C. X、Y、Z的最高价氧化物对应的水化物能相互反应
D. Z的阴离子结合质子的能力比N的阴离子强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,冰醋酸(纯醋酸)加水稀释过程中,溶液的导电能力如图所示,则:
(1)起点导电能力为0的理由是__________________.
(2)用湿润的pH试纸测量a处溶液的pH,测量结果______(偏大、偏小或不变)
(3)比较a、b、c三点的下列数据大小或等量关系:(如a>b>c、c=a>b、a=b=c等)

①pH:________;
②醋酸的电离程度:_________;
③醋酸的电离平衡常数:____________;
④a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:______.
(4)若使c点溶液中c(CH3COO﹣)增大,c(H+)减小,可采用的措施有(答二类不同的物质):①_________,②__________.
(5)在稀释过程中,随着c(CH3COOH)的降低,下列始终保持增大趋势的量是______.
A.c(H+) B.H+个数 C.CH3COOH个数 D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的甲、乙、丙三种金属,分别与足量的溶质质量分数相同的稀硫酸完全反应后,都生成+2价的硫酸盐,其产生氢气的体积与反应时间的关系如图所示,则下列说法正确的是

A. 三种金属的活动性顺序为甲>乙>丙
B. 反应结束消耗硫酸的质量一定相同
C. 三种金属的相对原子质量是甲>乙>丙
D. 甲先反应完,乙最后反应完
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com