
| A、1:9 | B、1:1 |
| C、1:2 | D、1:4 |
| 2x×10-2-x×10-2 |
| x+y |


科目:高中化学 来源: 题型:
| A、△H1=△H2<0 |
| B、△H1>△H2.>0 |
| C、△H1<△H2<0 |
| D、△H2<△H1<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有相同氧原子数的SO2和CO的质量相等 |
| B、2g氢气所含原子数目为NA |
| C、lmol氨气含有的原子数目为2NA |
| D、l7g氨气所含电子数目为l0NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
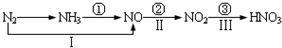
| A、路线①②③是工业生产硝酸的主要途径 |
| B、路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C、上述所有反应都是氧化还原反应 |
| D、氮气可在足量的氧气中通过一步反应生成NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0 | B、14 | C、15 | D、1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、去除CaCO3中含有少量CaSO4杂质:加入饱和Na2CO3溶液充分浸泡、洗涤、过滤 |
| B、焰色反应:用NaOH溶液洗涤并灼烧铂丝后,再沾上药品在火焰上灼烧 |
| C、海水蒸馏:冷却水从冷凝管的上口进,下口出 |
| D、测定溶液pH:用玻璃棒沾取溶液,点在湿润的pH试纸上,再与标准比色卡对照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、46 g NO2 和 N2O4混合气体中含有原子总数为3NA |
| B、标准状况下22.4L H2中含原子数为NA |
| C、7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA |
| D、1mol Fe与足量的稀HNO3反应,转移2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com