
【题目】白藜芦醇的结构简式为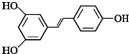 。根据要求回答下列问题:
。根据要求回答下列问题:
(1)白藜芦醇的分子式为 _______________
(2)所含官能团的名称为____________
(3)下列关于白藜芦醇的分类判断正确的是_________
A.它属于链状烯烃 B.它属于脂环化合物
C.它属于芳香化合物 D.它属于烃的衍生物
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题。
(1)写出下列有机物的结构简式:
①2,2,3,3-四甲基戊烷_________;
②2,5-二甲基庚烷____________;
③2,3-二甲基-6-乙基辛烷__________。
(2)写出下列物质的分子式:
①![]() ___________;
___________;
②![]() ___________;
___________;
(3)写出下列物质的键线式:
①![]() ___________;
___________;
②CH3CH=CHCH3___________;
(4)按系统命名法命名有机物CH3CH(C2H5)CH(CH3)2的名称是___________;
(5)![]() 所含官能团的名称是___________;该有机物发生加聚反应后,所得产物的结构简式为__________________。
所含官能团的名称是___________;该有机物发生加聚反应后,所得产物的结构简式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应①Fe(s)+CO2(g) ![]() FeO(s)+CO(g)△H1,平衡常数为K1;反应②Fe(s)+H2O(g)
FeO(s)+CO(g)△H1,平衡常数为K1;反应②Fe(s)+H2O(g) ![]() FeO(s)+H2(g)△H2,平衡常数为K2。在不同温度时K1、K2的值如下表:
FeO(s)+H2(g)△H2,平衡常数为K2。在不同温度时K1、K2的值如下表:

反应 CO2(g) + H2(g) ![]() CO(g) + H2O(g) △H,平衡常数K,则△H=_____________________(用△H1和△H2表示),K=____________________________________(用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g)
CO(g) + H2O(g) △H,平衡常数K,则△H=_____________________(用△H1和△H2表示),K=____________________________________(用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g) ![]() CO(g) + H2O(g)是___________________反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是___________________反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g) △H >0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) △H >0,CO2的浓度与时间的关系如图所示:
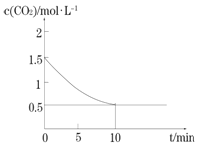
①该条件下反应的平衡常数为________________________________________;
②下列措施中能使平衡时c(CO)/c(CO2)增大的是______________________________________(填序号)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是________________________________(填字母)。
a.容器中压强不变 b.气体的密度不再改变 c.υ正(CO2)= υ逆(CO)
d.c(CO2)= c(CO) e.容器内气体总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室从海带中提取碘的流程如下:
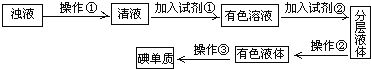
①指出过程中有关的实验操作①和②名称:①___,②___。
②下列物质中,能使湿润的KI-淀粉试纸变蓝的是___。
A.碘蒸气 B.Cl2 C.KI溶液 D.饱和氯化钠溶液
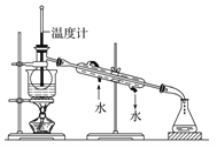
③有同学试图利用蒸馏方法来实现第③步操作,该同学设计了如图蒸馏实验装置,此装置中的明显错误之处为____、____。
④试剂①若用H2O2溶液和稀硫酸,请写出发生反应的离子方程式___。
(2)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。为进一步研究酸雨的成分,该同学取某一时段的这种雨水VL加入0.50mol/LBa(OH)2溶液至不再产生沉淀时,恰好消耗40.00mLBa(OH)2溶液。请完成
①该酸雨pH随时间的增加而减小的原因是___(用化学方程式解释),
②若生成沉淀物的质量为4.50g,则沉淀物的组成为___(填写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
物质 | 沸点/℃ | 密度 / gcm-3 | 水中溶解性 |
|
正丁醇 | 117.2 | 0.8109 | 微溶 | |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟侯氏制碱法的部分装置。下列操作正确的是![]()
![]()
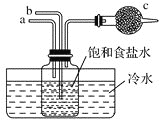
A.b通入![]() ,然后a通入
,然后a通入![]() ,c中放碱石灰
,c中放碱石灰
B.a通入![]() ,然后b通入
,然后b通入![]() ,广口瓶中析出
,广口瓶中析出![]()
C.a通入![]() ,然后b通入
,然后b通入![]() ,c中放蘸稀硫酸的脱脂棉
,c中放蘸稀硫酸的脱脂棉
D.b通入![]() ,然后a通入
,然后a通入![]() ,c中放蘸NaOH溶液的脱脂棉
,c中放蘸NaOH溶液的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(写出计算步骤)已知可逆反应:M(g)+N(g)![]() P(g)+Q(g),△H>0请回答下列问题:
P(g)+Q(g),△H>0请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol·L-1,c(N)=2.4mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为多少______?平衡常数?__
(2)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2mol·L-1,a=?;________
(3)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=bmolL-1,,达到平衡后,M的转化率为多少?________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z 的原子序数依次增大,W、X 原子的最外层电子数之比为 4:3,Z 原子比 X 原子的核外电子数多 4。下列说法正确的是
A.W、Y、Z 的电负性大小顺序一定是 Z>Y>W
B.W、X、Y、Z 的原子半径大小顺序可能是 W>X>Y>Z
C.Y、Z 形成的分子空间构型可能是正四面体
D.WY2 分子中![]() 键与π键的数目之比是 2:1
键与π键的数目之比是 2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com